Condições dos tecidos peri-implantares em implantes tratados com a técnica de Camada Aumentada Sub-periosteal: Uma série de casos retrospectiva
Tradução automática
O artigo original está escrito em EN language (link para lê-lo) .
Resumo
Objetivos: Avaliar as condições dos tecidos peri-implantares a curto prazo em pacientes que receberam a técnica de Camada Aumentada Sub-periosteal Peri-implantar (SPAL) e em pacientes com espessura adequada (≥2 mm) da placa óssea bucal peri-implantar (PBBP) no momento da colocação.
Métodos: Pacientes em que um defeito de deiscência ou PBBP fina na colocação do implante foi corrigido pela técnica SPAL (grupos SPALdehiscence e SPALthin, respectivamente) e pacientes apresentando uma espessura residual de PBBP ≥2 mm na colocação do implante (grupo controle) foram selecionados retrospectivamente. O número de locais peri-implantares positivos para sangramento à sondagem (BoP) aos 6 meses após a carga protética foi o desfecho primário. Além disso, a altura da mucosa queratinizada, nível do tecido mole marginal, Índice de Placa, profundidade de sondagem peri-implantar, supuração à sondagem e nível ósseo radiográfico interproximal (RBL) foram avaliados.
Resultados: Trinta e quatro pacientes (11 no grupo SPALdeiscência, 11 no grupo SPALfino e 12 no grupo controle) foram incluídos. Em cada grupo SPAL, 10 pacientes (90,9%) apresentaram espessura do tecido peri-implantar ≥2 mm na porção mais coronal do implante na exposição. A prevalência (número) de locais positivos para BoP foi de 2, 1 e 0 nos grupos SPALdeiscência, SPALfino e controle, respectivamente. A RBL foi de 0,3 mm no grupo SPALdeiscência, 0,2 mm no grupo SPALfino e 0 mm no grupo controle.
Conclusão: Após 6 meses de carga protética, pacientes tratados com a técnica SPAL apresentam inflamação mucosa peri-implantar limitada em associação com PD superficial e KM adequada. Nos implantes que receberam a técnica SPAL, no entanto, a RBL interproximal foi encontrada apical à sua posição ideal.
Introdução
A colocação de implantes orientada prosteticamente em uma dimensão óssea horizontal reduzida muitas vezes resulta em uma deiscência óssea peri-implantar ou fenestração. Mesmo na presença de uma placa cortical bucal intacta, mas fina, o trauma cirúrgico e o consequente remodelamento ósseo após a colocação do implante podem levar a uma perda óssea vertical com a exposição da parte coronária do implante durante a descoberta (Merheb et al., 2017, Monje, et al., 2019, Spray, Black, Morris, 2000). Embora a quantidade de remodelamento ósseo após a inserção do implante tenha mostrado ser semelhante em placas ósseas bucais finas e grossas (Merheb et al., 2017), tal remodelamento pode ter um impacto diferente na integridade da placa óssea bucal peri-implantar (PBBP). Nesse sentido, um risco aumentado de complicações estéticas e biológicas após a colocação do implante em locais com defeito de deiscência ou uma PBBP fina em comparação com PBBP grossa foi demonstrado em estudos pré-clínicos (Monje, et al., 2019) e clínicos (Schwarz, Sahm, Becker, 2012, Jung et al., 2017). Coletivamente, essas descobertas ressaltam a relevância da integridade e espessura da PBBP na colocação do implante, favorecendo condições estáveis e saudáveis dos tecidos peri-implantares ao longo do tempo (Sanz-Sánchez et al., 2018).
O procedimento mais documentado e eficaz para corrigir cirurgicamente um defeito do tipo deiscência é baseado no uso de membranas de barreira combinadas com enxertos de substituição óssea de acordo com os princípios de regeneração óssea guiada (GBR) (Sanz-Sánchez, Ortiz-Vigón, Sanz-Martín, Figuero, Sanz, 2015). A redução ou resolução da deiscência óssea peri-implante relatada após GBR (Thoma, Bienz, Figuero, Jung, Sanz-Martín, 2019) parece impactar positivamente nas condições de implante a longo prazo, em termos de taxa de sobrevivência do implante e estabilidade dos tecidos peri-implantes (Sanz-Sánchez et al., 2018). Infelizmente, se e em que medida um aumento na espessura do osso peri-implante associado à cobertura completa da superfície exposta do implante pode apoiar a saúde peri-implante não foi totalmente elucidado.
Recentemente, um procedimento simplificado de aumento ósseo, denominado técnica da Camada Aumentada Sub-periosteal Peri-implante (SPAL), baseado no uso do periosto como uma membrana de barreira e um enxerto como “dispositivo” para criação de espaço para aumento ósseo concomitante à colocação do implante, foi descrito (Trombelli, Severi, Pramstraller, Farina, 2018). A eficácia dessa técnica para corrigir uma deiscência óssea peri-implante e/ou aumentar a espessura do osso peri-implante foi relatada anteriormente (Trombelli, Severi, Pramstraller, Farina, 2019), e sua aplicação também foi explorada no tratamento de defeitos de peri-implantite (Trombelli et al. 2020). O objetivo da presente série de casos retrospectivos foi avaliar as condições dos tecidos peri-implantes a curto prazo em pacientes que receberam a técnica SPAL em comparação com pacientes com espessura adequada (≥2 mm) de PBBP na colocação do implante.
Material e métodos
2.1 Desenho do estudo e aspectos éticos
O presente estudo foi elaborado de acordo com a diretriz STROBE Apêndice S1. O protocolo foi aprovado pelo Comitê de Ética da Área Vasta Emilia Centro, Itália (número do protocolo 637/2018/ Oss/UniFe, data de aprovação 12.12.2018). Cada paciente forneceu um consentimento informado por escrito antes do tratamento cirúrgico. Todos os procedimentos clínicos foram realizados de acordo com a Declaração de Helsinque e as Diretrizes de Boas Práticas Clínicas (GCP).
2.2 População do estudo
Os prontuários dos pacientes que passaram por reabilitação protética suportada por implantes no período de dezembro de 2015 a julho de 2018 no Centro de Pesquisa para o Estudo de Doenças Periodontais e Peri-implantares, Universidade de Ferrara, e em um consultório odontológico privado em Ferrara foram analisados para determinar a elegibilidade dos pacientes para o estudo. A inclusão dos pacientes no estudo estava subordinada aos seguintes critérios:
- Não fumantes ou fumantes ≤10 cigarros/dia no momento da cirurgia;
- Não diabéticos ou diabéticos bem controlados (HbA1c ≤ 7%) no momento da cirurgia;
- Disponibilidade de parâmetros clínicos e exames radiográficos para o estudo (veja “Parâmetros do estudo” para detalhes).
- Não estar tomando medicamentos que influenciam o metabolismo ósseo (por exemplo, bisfosfonatos, corticosteroides);
- Submetido à colocação de implante inteiramente em osso nativo (com uma espessura residual de PBBP ≥2 mm após a inserção do implante) ou concomitantemente com a técnica SPAL.
A inclusão do implante no estudo estava subordinada aos seguintes critérios:
- Colocação em crista cicatrizada (implantes tipo IV, Hämmerle, Chen, Wilson, 2004);
- Estabilidade primária, conforme avaliado pela torque de inserção.
Com base nas condições de PBBP no momento da colocação do implante e em seu manejo clínico, os pacientes foram categorizados em três grupos:
- Pacientes com implante/s apresentando uma espessura residual de PBBP ≥2 mm após a inserção do implante (grupo controle);
- Pacientes com implante/s tratados com a técnica SPAL para corrigir uma deiscência óssea peri-implantar ≥3 mm concomitantemente à colocação do implante (grupo SPALdehiscence);
- Pacientes com implante/s tratados com a técnica SPAL para aumentar um PBBP fino (≤1 mm) concomitantemente à colocação do implante (grupo SPALthin).
2.3 Procedimentos clínicos
Antes da colocação do implante, todos os pacientes haviam passado por terapia ativa para tratar lesões cariosas e doenças periodontais e foram inscritos em uma manutenção profissional com frequência de retornos agendada de acordo com a ferramenta de avaliação PerioRisk (Trombelli, Farina, Ferrari, Pasetti, Calura, 2009, Trombelli et al., 2017).
Todos os procedimentos cirúrgicos foram realizados por dois periodontistas experientes (L.T. e M.P.). Os pacientes receberam 2 g de amoxicilina + ácido clavulânico (Augmentin, GlaxoSmithKline) uma hora antes da cirurgia. A anestesia local foi obtida utilizando articaína com 1:100.000 de epinefrina administrada por infiltração local.
2.3.1 Procedimentos cirúrgicos—grupos SPAL
Em pacientes onde um defeito de deiscência ou PBBP fino na colocação foi corrigido pela técnica SPAL (Figuras 1 e 2, respectivamente), o acesso cirúrgico à crista óssea foi realizado conforme descrito anteriormente (Trombelli, Severi, Pramstraller, & Farina, 2018). Resumidamente, uma camada mucosa foi levantada na face bucal por dissecção de espessura dividida com uma lâmina 15C, bem como facas de tunelamento (KPAX, TKN1X e TKN2X, Hu-Friedy) com bordas afiadas anguladas variando de acordo com a localização anatômica. Em seguida, a camada periosteal foi elevada do osso com um elevador periosteal (PTROM, Hu-Friedy), criando um bolso que poderia acomodar um enxerto. Um retalho de espessura total foi elevado na face oral (lingual/palatina).
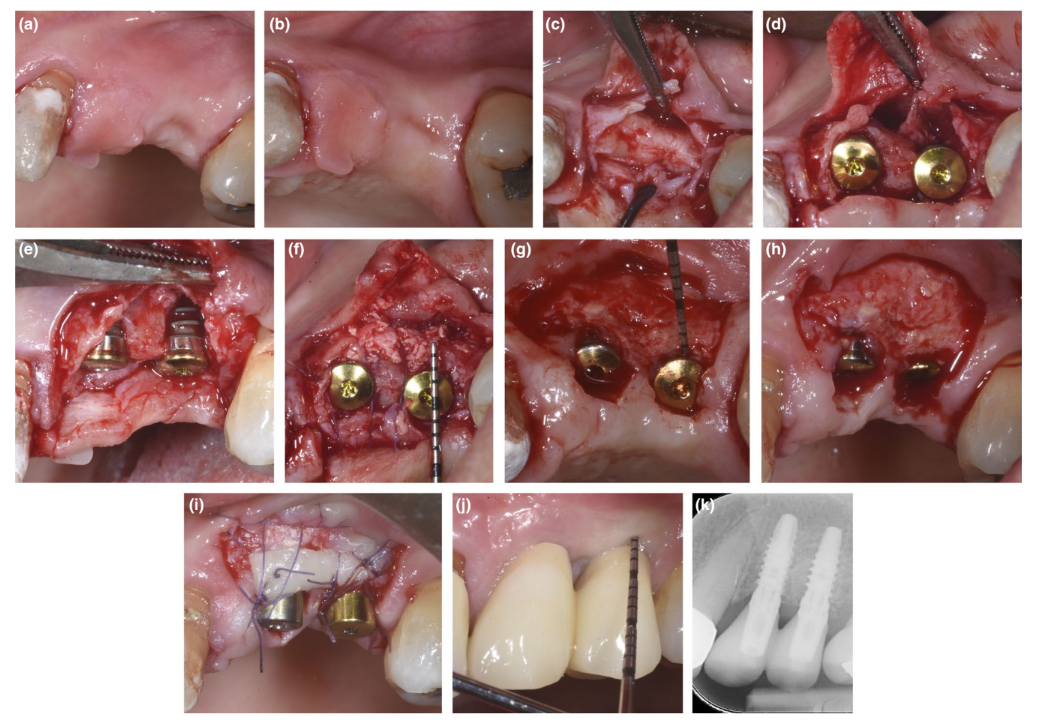
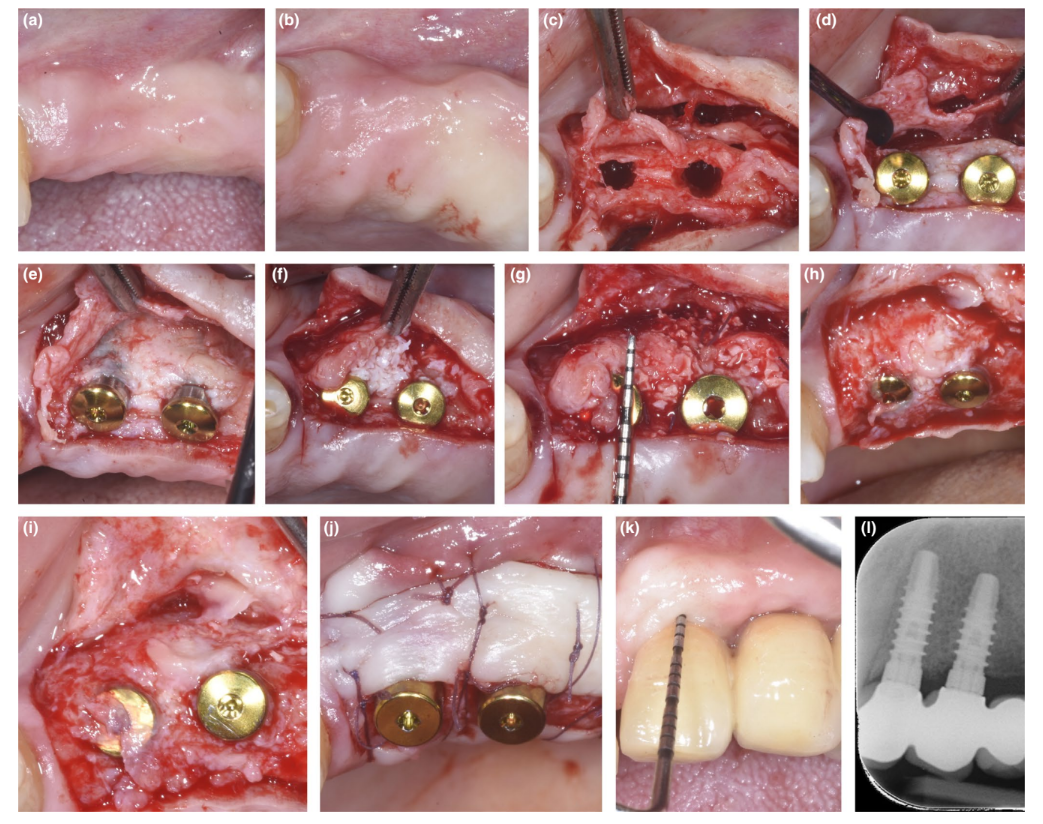
Implantes em nível de tecido (SPI Element™; Thommen Medical) foram inseridos. Um xenógeno derivado de bovino (Bio-Oss® grânulos de esponjosa, tamanho de partícula 0,25–1,0 mm; Geistlich Pharma, AG) foi utilizado sozinho ou em combinação com partículas de osso cortical autógeno para preencher o espaço criado cirurgicamente entre a camada periosteal e a placa óssea bucal fina ou a superfície do implante exposta. Na presença de uma deiscência, o enxerto foi realizado para corrigir completamente o defeito peri-implantar até o colar polido. Em todos os casos, o enxerto sub-periosteal forneceu pelo menos 2 mm de espessura na porção mais coronal do implante.
A porção coronal da camada periosteal foi estabilizada ao retalho mucoperiosteal oral por meio de suturas internas de colchão reabsorvíveis (Vicryl 6/0, Ethicon). A camada mucosa foi então avançada coronariamente e suturada sem tensão por suturas internas de colchão horizontal e suturas interrompidas para submergir tanto o enxerto quanto os implantes.
No procedimento de reentrada para a exposição do implante, um retalho bucal de espessura parcial foi dissecado para posicionar o pilar de cicatrização. Para fornecer dimensões adequadas de mucosa peri-implantar queratinizada, foi realizado um retalho posicionado apicalmente ou um enxerto gengival livre (Trombelli, Severi, Pramstraller, & Farina, 2019).
2.3.2 Procedimentos cirúrgicos—grupo controle
Um retalho bucal e lingual/palatino de espessura total foi levantado para expor a crista óssea. O local do implante foi preparado de acordo com as instruções do fabricante, e implantes de nível tecidual (SPI Element™; Thommen Medical) foram inseridos. Devido à presença de uma espessura residual de PBBP ≥2 mm, nenhum procedimento de aumento ósseo foi realizado. Em todos os casos, o retalho foi aparado e posicionado ao redor do pilar de cicatrização com suturas reabsorvíveis (Vicryl 6/0, Ethicon). O design e a manipulação do retalho, bem como a técnica de sutura, foram realizados para garantir dimensões adequadas (altura, espessura) da mucosa peri-implantar queratinizada.
2.3.3 Procedimentos pós-operatórios
Os pacientes foram instruídos a não usar próteses removíveis para evitar compressão no local cirúrgico por pelo menos 4 semanas e a não mastigar ou escovar na área tratada por aproximadamente 2 semanas.
O uso domiciliar de uma solução de clorexidina a 0,12% (Curasept ADS Trattamento Rigenerante®; Curaden Healthcare) foi prescrito para controle químico da placa (bochecho de 1 minuto duas vezes ao dia por 3 semanas). Os pontos foram removidos 2 semanas após a cirurgia.
2.3.4 Cronograma da reabilitação protética
A reabilitação protética foi iniciada de 3 a 4 meses após a colocação do implante no grupo controle, enquanto que pelo menos 4 semanas após a exposição do implante nos grupos SPAL.
2.4 Parâmetros do estudo
2.4.1 Parâmetros clínicos
Após 6 meses de carga protética, um examinador treinado (M.S.) que havia participado de estudos anteriores sobre a técnica SPAL (Trombelli, Severi, Pramstraller, Farina, 2019) realizou as seguintes medições clínicas com uma sonda periodontal UNC-15 na seguinte sequência cronológica:
- Altura da mucosa queratinizada (MQ): medida no aspecto médio-bucal do implante como a distância entre a margem mucosa peri-implantar bucal e a junção mucogengival, e registrada até o milímetro mais próximo;
- Nível de tecido mole marginal (NTMM) (Zitzmann, Schärer, Marinello, 2001): medido no aspecto médio-bucal do implante como a distância entre a margem mucosa peri-implantar bucal e a junção implante-abutment, e registrado até o milímetro mais próximo. O NTMM foi registrado como positivo ou negativo quando a margem do abutment estava localizada acima ou abaixo da margem mucosa, respectivamente;
- Índice de Placa (IP; O'Leary, Drake, Naylor, 1972): registrado nos aspectos mesio-bucal, médio-bucal, disto-bucal, e médio-lingual/palatino do implante como placa supragengival presente ou ausente após explorar a margem protética juxtagingival com a ponta da sonda;
- Profundidade de sondagem (PS): medida da margem mucosa até a penetração mais profunda da sonda em seis locais (mesio-bucal, médio-bucal, disto-bucal, disto-lingual, médio-lingual, e mesio-lingual) usando uma força de 0,2–0,3 N, e registrada até o milímetro mais próximo;
- Sangramento à sondagem (SaS; Ainamo e Bay, 1975): registrado como presente ou ausente na avaliação da PS;
- Supuração à sondagem (SuS): registrado como presente ou ausente na avaliação da PS.
2.4.2 Nível ósseo radiográfico
Radiografias periapicais não padronizadas obtidas com a técnica de cone longo paralelo 6 meses após a carga protética foram digitalizadas e analisadas usando um software especificamente projetado (NIS elements v4.2; Nikon Instruments, Campi Bisenzio). O nível ósseo radiográfico (RBL) foi medido como a distância (aproximada para o décimo de milímetro mais próximo) entre a margem apical do colar polido do implante e a crista óssea no aspecto mesial (mRBL) e distal (dRBL) de cada implante usando uma ampliação de 10x–15x. Uma marca de referência de 1 mm de altura presente na radiografia digital foi usada para calibração.
Um examinador (A.S.) realizou as medições radiográficas. O examinador participou de uma sessão de calibração em uma amostra de radiografias obtidas de pacientes não selecionados para o presente estudo. A sessão de calibração consistiu em duas sessões de medições de RBL, realizadas com um intervalo de 7 dias, e permitiu alcançar um excelente acordo intraexaminador (pontuação k = 0,89), com uma diferença média entre medições pareadas de 0,04 ± 0,15 mm.
2.5 Análise estatística
O paciente foi considerado a unidade estatística. Se dois ou mais implantes no mesmo paciente eram elegíveis para o estudo, apenas um implante foi incluído aleatoriamente para análise. Os dados foram descritos usando média e desvio padrão (DP), mediana e intervalo interquartil (IR), valores mínimo-máximo para variáveis quantitativas, e frequência e porcentagem para variáveis categóricas.
O número mediano de locais positivos para sangramento à sondagem (BoP) avaliado aos 6 meses após a carga do implante foi a variável de resultado primária do estudo. Os valores medianos de profundidade de sondagem (PD), mobilidade do dente (KM), perda de tecido marginal (MSTL), perda óssea residual (RBL), número de locais positivos para índice de placa (PlI) e número de locais positivos para sangramento (SoP) foram variáveis de resultado secundárias.
Devido ao tamanho limitado da amostra, nenhuma estatística inferencial foi realizada e os resultados foram relatados com uma abordagem narrativa. No entanto, o tamanho do efeito (ES) foi calculado para cada variável de resultado de acordo com o teste não paramétrico de Kruskal-Wallis. O ES foi classificado como pequeno (d = 0.1–0.3), médio (d = 0.3–0.5) ou grande (d ≥ 0.5) (Cohen, 1988).
Resultados
3.1 População do estudo
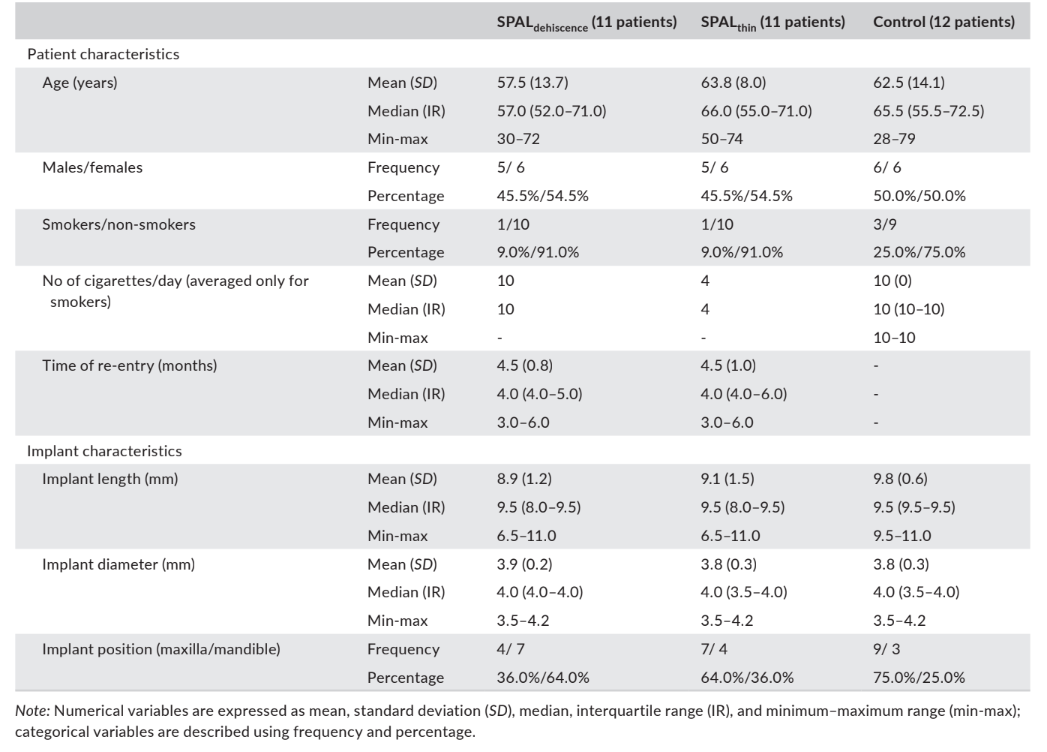
Trinta e quatro pacientes com 34 implantes (11 no grupo SPALdeiscência, 11 no grupo SPALfino, e 12 no grupo controle) foram incluídos para análise. A grande maioria dos pacientes eram não fumantes (90,9% no grupo SPALdeiscência, 90,9% no grupo SPALfino, e 75% no grupo controle). Os implantes no grupo SPALdeiscência estavam predominantemente localizados na mandíbula, enquanto os implantes nos grupos SPALfino e controle estavam predominantemente colocados na maxila (Tabela 1). Nenhum paciente ou implante foi perdido durante o período de acompanhamento.
No grupo SPALdeiscência, 1 paciente apresentou deiscência da ferida após 2 semanas, com exposição parcial das roscas do implante. O paciente foi visto mensalmente até a reentrada, e o local foi desinfetado localmente com uma solução de clorexidina a 0,12% em cada visita de retorno.
Nos grupos SPALdeiscência e SPALfino, a reentrada foi realizada de 3 a 6 meses após a colocação do implante (mediana: 4,0 meses em ambos os grupos; p = 1; Tabela 1). A espessura do osso peri-implantar e a altura e largura da deiscência óssea peri-implantar registradas para os grupos SPALdeiscência e SPALfino estão relatadas nas Tabelas 2 e 3, respectivamente. Em cada grupo SPAL, 10 pacientes (90,9%) mostraram ausência de deiscência peri-implantar combinada com espessura óssea peri-implantar ≥2 mm (Tabelas 2 e 3). Um paciente no grupo SPALdeiscência apresentou uma deiscência residual de 2 mm (Tabela 2), que foi coberta com um enxerto gengival livre. Um paciente no grupo SPALfino apresentou uma espessura óssea peri-implantar de 1 mm sem deiscência (Tabela 3).
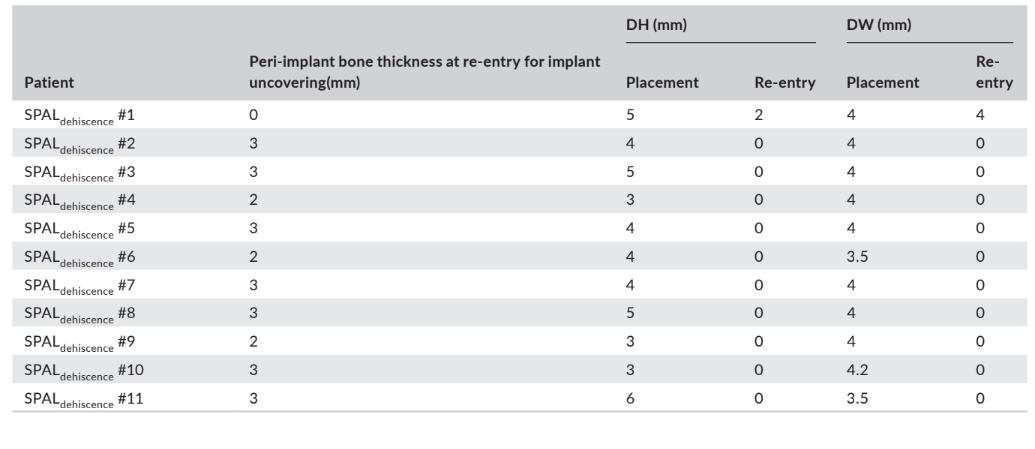
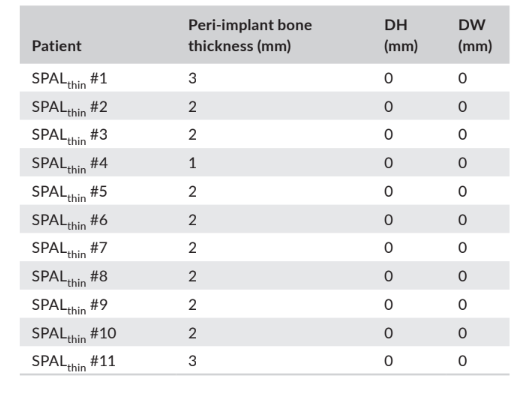
e largura da deiscência (DH e DW, respectivamente) avaliadas na reentrada para
descobrimento do implante em cada paciente do grupo SPALthin
No grupo SPALdehiscence, 8 implantes suportaram uma prótese parcial fixa, 2 implantes foram restaurados com uma coroa única, e 1 implante fazia parte de uma prótese sobre dentadura. No grupo SPALthin, 9 implantes suportaram uma prótese parcial fixa, 2 implantes foram restaurados com uma coroa única, e 1 fazia parte de uma prótese sobre dentadura. No grupo controle, 4 implantes faziam parte de uma prótese parcial fixa e 8 implantes foram restaurados com uma coroa única.
3.2 Resultados do estudo
Os dados relacionados aos resultados clínicos (ou seja, PD, BoP, SoP, PlI, MSTL e KM) e RBL, conforme avaliado 6 meses após a carga do implante, estão relatados na Tabela 4.
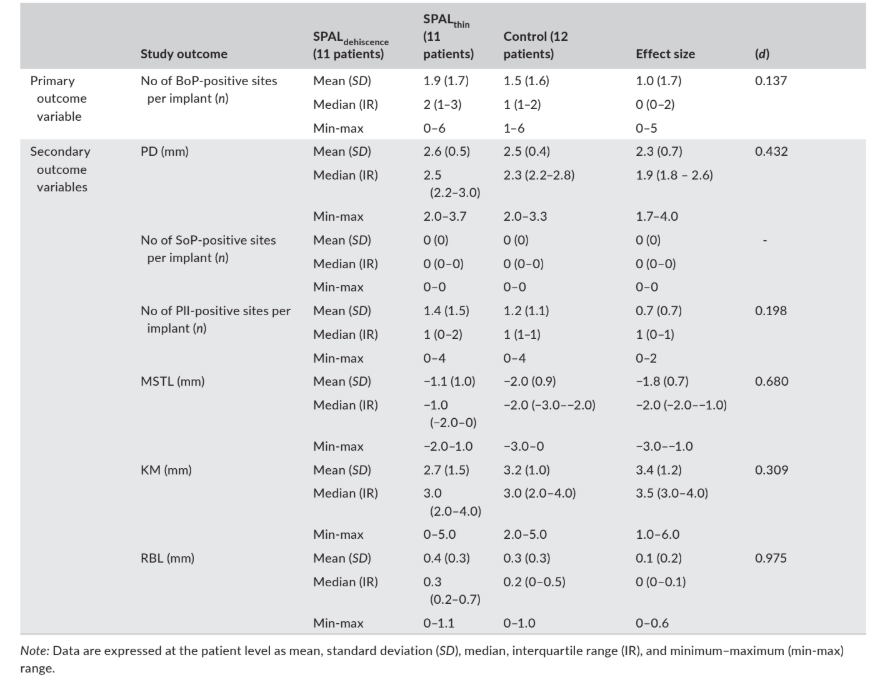
A prevalência mediana (número) de locais positivos para BoP foi de 2, 1 e 0 nos grupos SPALdeiscência, SPALfino e controle, respectivamente.
O número mediano de locais positivos para PlI foi de 1 em todos os grupos. SoP foi negativo em todos os locais de implante.
A margem mucosa estava localizada a 1 mm (grupo SPALdeiscência) ou 2 mm (grupos SPALfino e controle) acima da junção implante-abutment em todos os grupos, e os grupos de estudo apresentaram uma KM mediana de pelo menos 3 mm.
O nível ósseo radiográfico foi de 0,3 mm no grupo SPALdeiscência, 0,2 mm no grupo SPALfino e 0 mm no grupo controle.
ES foi pequeno para o número de locais positivos para BoP (d = 0,137) e PlI (d = 0,198), médio para KM (d = 0,309), PD (d = 0,432) e MSTL (d = 0,680), e grande para RBL (d = 0,975) (Tabela 4).
Discussão
O objetivo da presente série de casos retrospectiva foi avaliar as condições dos tecidos peri-implantares a curto prazo em pacientes que receberam a técnica SPAL e em pacientes com espessura adequada (≥2 mm) de PBBP na colocação do implante. Os resultados indicaram que os pacientes tratados com a técnica SPAL apresentaram baixo número de locais peri-implantares inflamados e PD superficial (<4 mm) aos 6 meses de carga protética. Além disso, o nível ósseo interproximal foi encontrado apical (embora em uma extensão limitada) ao colar polido do implante apenas nos grupos SPAL.
Sangramento à sondagem foi selecionado como resultado primário uma vez que (a) a avaliação de BoP é atualmente identificada como a medida clínica para distinguir entre saúde e doença peri-implantar, sendo um elemento diagnóstico invariável de mucosite peri-implantar e peri-implantite (Renvert, Persson, Pirih, Camargo, 2018, Berglundh et al., 2018), e (b) sua ausência está associada à estabilidade das condições dos tecidos peri-implantares (Jepsen, Rühling, Jepsen, Ohlenbusch, Albers, 1996, Luterbacher, Mayfield, Brägger, Lang, 2000). A proporção de locais peri-implantares inflamados, conforme registrado nos grupos do estudo, compara-se com descobertas anteriores que avaliaram a prevalência de BoP em 289 implantes (Farina, Filippi, Brazzioli, Tomasi, Trombelli, 2017). Além disso, condições inflamatórias peri-implantares semelhantes foram relatadas 18 meses após GBR (Jung et al., 2017).
Em nosso estudo, uma baixa frequência de locais de mucosa peri-implantar inflamada foi observada em todos os grupos de estudo. Isso pode ser parcialmente devido a características semelhantes para fatores que influenciam o BoP ao redor dos implantes, como baixa presença de placa juxtagingival (Pontoriero et al., 1994; Salvi et al., 2012), PD rasa (Farina, Filippi, Brazzioli, Tomasi, & Trombelli, 2017) e quantidade adequada de KM (Chung, Oh, Shotwell, Misch, Wang, 2006, Perussolo et al., 2018). Nossos achados são consistentes com aqueles provenientes de uma recente revisão sistemática sobre complicações biológicas de implantes dentários colocados em locais pristinos ou aumentados. A meta-análise mostrou uma prevalência semelhante de mucosite peri-implantar em pacientes que receberam (19,6%; IC 95%: 0%–40%) ou não receberam (22,4%; IC 95%: 6%–38%) procedimentos para preservação da crista alveolar e/ou aumento vertical/lateral da crista (Salvi, Monje, Tomasi, 2018). Além disso, condições inflamatórias semelhantes foram relatadas em implantes colocados em osso nativo em comparação com implantes colocados concomitantemente com um procedimento de GBR (Benic, Jung, Siegenthaler, Hammerle, 2009; Benic, Bernasconi, Jung, Hammerle, 2017).
É importante considerar que, na reentrada, a grande maioria dos pacientes que receberam a técnica SPAL apresentou uma espessura óssea peri-implantar ≥2 mm na porção mais coronária do implante. Embora a medição do PBBP não estivesse disponível na reentrada para o grupo controle (procedimento de uma etapa), a integridade do PBBP após o remodelamento ósseo peri-implantar pós-inserção pode ser assumida com base em dados pré-clínicos (Monje et al., 2019) e clínicos (Spray, Black, Morris, & Ochi, 2000) sobre dimensões críticas da placa óssea bucal. Coletivamente, os dados disponíveis parecem sugerir que dimensões verticais e horizontais adequadas dos tecidos peri-implantares alcançadas por meio de procedimentos de aumento podem favorecer condições para limitar a inflamação dos tecidos peri-implantares. No entanto, a associação da integridade do PBBP até a porção mais coronária do implante e a gravidade da inflamação mucosa peri-implantar não está totalmente clara (Jung et al., 2017).
Aos 6 meses de carga protética, uma posição diferente do nível ósseo peri-implantar interproximal foi observada entre os grupos, com uma RBL mais apical nos grupos SPAL. É notável que, nos grupos SPAL, os implantes de nível de tecido foram posicionados ligeiramente subcrestais (Figuras 1 e 2). Embora isso possa ter facilitado o enxerto do bolso periosteal até a parte mais coronal do implante, bem como o fechamento por primeira intenção, o posicionamento subcrestal também pode ter contribuído para o remodelamento ósseo interproximal (Saleh et al., 2018). Além disso, uma vez que os implantes que receberam a técnica SPAL passaram por cirurgia adicional para descoberta, incluindo um retalho posicionado apicalmente ou um enxerto gengival livre, o remodelamento ósseo interproximal nos grupos SPAL pode também ser parcialmente atribuído ao efeito prejudicial da elevação do retalho sobre o suprimento sanguíneo local. Consistentemente, a perda óssea marginal peri-implantar foi relatada entre a reentrada para descoberta e a entrega da prótese final por outros autores (Cardaropoli, Lekholm, Wennstrom, 2006, Nader et al., 2016). Também deve ser considerado que, em alguns pacientes do grupo SPALdeiscência, o enxerto foi estendido para os aspectos mesial e/ou distal do implante devido a uma extensão interproximal do defeito ósseo peri-implantar. No grupo SPALdeiscência, portanto, a extensão do remodelamento do enxerto em locais interproximais pode ter impactado negativamente os valores de RBL. Dados recentes mostraram que até mesmo biomateriais de enxerto de reabsorção lenta, como DBBM, estão associados a uma redução substancial da área enxertada na avaliação radiográfica de 12 meses após procedimentos de aumento endosinusal (Franceschetti et al., 2019). No entanto, a magnitude da RBL observada no presente estudo é limitada em comparação com a relatada para implantes colocados com GBR concomitante ou em osso nativo (Urban et al., 2019) e implantes apresentando uma deiscência bucal não tratada (Jung et al., 2017).
Foi observada uma KM e MSTL ligeiramente mais baixas para o grupo SPALdeiscência. Isso ocorreu apesar da manipulação do tecido mole peri-implante ter sido adequadamente realizada para fornecer dimensões adequadas de mucosa peri-implantar queratinizada e uma posição subgengival das margens protéticas. Essa descoberta pode estar um tanto correlacionada com o aumento do remodelamento ósseo (RBL) observado no grupo SPALdeiscência, que também pode ter envolvido a regeneração da placa óssea bucal. Uma revisão sistemática recente correlacionou o remodelamento do osso bucal com a ocorrência de recessão do tecido mole peri-implantar (Aizcorbe-Vicente, Peñarrocha-Oltra, Canullo, Soto-Peñaloza, & Peñarrocha-Diago, 2020). No grupo SPALdeiscência, 1 paciente (9,1%) apresentou uma deiscência de ferida em 2 semanas que levou à exposição parcial das roscas do implante na reentrada. Essa descoberta se compara à incidência de deiscência de ferida e consequente exposição da membrana após procedimentos de GBR para corrigir a deiscência óssea peri-implantar na colocação, conforme relatado em uma meta-análise recente realizada em estudos prospectivos e retrospectivos (Garcia et al., 2018). Em particular, a exposição da membrana ocorreu com uma incidência variando de 16,7% (Tawil, El-Ghoule, & Mawla, 2001) a 62,8% (Gher, Quintero, Assad, Monaco, & Richardson, 1994), e foi associada a uma cobertura de deiscência significativamente mais baixa (Garcia et al., 2018). As limitações deste relatório preliminar incluem o desenho retrospectivo, o pequeno tamanho da amostra e o curto tempo de acompanhamento de 6 meses após a restauração dos implantes. Além disso, o impacto de fatores relacionados ao paciente (por exemplo, espessura do tecido mole na área edêntula, hábito de fumar, diabetes) e complicações relacionadas à cirurgia (por exemplo, perfurações da camada periosteal e/ou mucosa) nos resultados clínicos não foi analisado de forma abrangente. Além disso, condições clínicas específicas (ou seja, PBBP fina ou deiscência óssea peri-implantar de dimensão vertical limitada) foram selecionadas para o tratamento SPAL. Mais estudos são necessários para avaliar quais condições/lesões clínicas podem ser efetivamente tratadas com a técnica SPAL ou se um tratamento mais convencional (por exemplo, GBR) deve ser preferido.
Em conclusão, os resultados do presente estudo mostraram que, após 6 meses de carga protética, pacientes tratados com a técnica SPAL apresentam inflamação mucosa peri-implantar limitada em associação com PD superficial e KM adequada. Nos implantes que receberam a técnica SPAL, no entanto, a RBL interproximal foi encontrada apical à sua posição ideal. Se e em que medida os resultados favoráveis de curto prazo observados após a técnica SPAL podem ser benéficos para as condições saudáveis de longo prazo dos tecidos peri-implantares e a estabilidade do perfil mucoso bucal precisam ser avaliados.
Leonardo Trombelli, Mattia Pramstraller, Mattia Severi, Anna Simonelli, Roberto Farina
Referências
- Ainamo, J., & Bay, I. (1975). Problemas e propostas para registrar gengivite e placa. International Dental Journal, 25, 229–235.
- Aizcorbe-Vicente, J., Peñarrocha-Oltra, D., Canullo, L., Soto-Peñaloza, D., & Peñarrocha-Diago, M. (2020). Influência da espessura do osso facial após a colocação de implantes em cristas cicatrizadas sobre o osso facial remodelado e considerando a recessão do tecido mole: Uma revisão sistemática. International Journal of Oral and Maxillofacial Implants, 35, 107–119. https://doi.org/10.11607/jomi.7259
- Benic, G. I., Bernasconi, M., Jung, R. E., & Hammerle, C. H. F. (2017). Comparação clínica e radiográfica intra-sujeito de implantes colocados com ou sem regeneração óssea guiada: resultados de 15 anos. Journal of Clinical Periodontology, 44, 315–325. https://doi.org/10.1111/jcpe.12665
- Benić, G. I., Jung, R. E., Siegenthaler, D. W., & Hämmerle, C. H. F. (2009). Comparação clínica e radiográfica de implantes em osso regenerado ou nativo: resultados de 5 anos. Clinical Oral Implant Research, 20, 507–513. https://doi.org/10.1111/j.1600-0501.2008.01583.x
- Berglundh, T., Armitage, G., Araujo, M. G., Avila-Ortiz, G., Blanco, J., Camargo, P. M., Zitzmann, N. (2018). Doenças e condições peri-implantares: Relatório de consenso do grupo de trabalho 4 do Workshop Mundial de 2017 sobre a Classificação de Doenças e Condições Periodontais e Peri-Implantares. Journal of Clinical Periodontology, 45(Suppl 20), S286–S291. https://doi.org/10.1034/j.1600-0501.1994.050409.x
- Cardaropoli, G., Lekholm, U., & Wennstrom, J. L. (2006). Alterações teciduais em substituições de dentes únicos suportadas por implantes: Um estudo clínico prospectivo de 1 ano. Clinical Oral Implant Research, 17, 165–171. https://doi.org/10.1111/j.1600-0501.2005.01210.x
- Chung, D. M., Oh, T. J., Shotwell, J. L., Misch, C. E., & Wang, H. L. (2006). Significado da mucosa queratinizada na manutenção de implantes dentários com superfícies diferentes. Journal of Periodontology, 77, 1410–1420. https://doi.org/10.1902/jop.2006.050393
- Cohen, J. (1988). Análise de poder estatístico para as ciências comportamentais, 2ª ed. Mahwah, NJ: Lawrence Erlbaum Associated Publishers.
- Farina, R., Filippi, M., Brazzioli, J., Tomasi, C., & Trombelli, L. (2017). Sangramento à sondagem ao redor de implantes dentários: Um estudo retrospectivo de fatores associados. Journal of Clinical Periodontology, 44, 115–122. https://doi.org/10.1111/jcpe.12647
- Franceschetti, G., Farina, R., Minenna, L., Riccardi, O., Stacchi, C., Di Raimondo, R., … Trombelli, L. (2019). O impacto do remodelamento do enxerto no suporte ósseo peri-implantar em implantes colocados concomitantemente com elevação do assoalho do seio transcrestal: Uma série de casos retrospectiva multicêntrica. Clinical Oral Implant Research, 31(2), 1–16. https://doi.org/10.1111/clr.13541
- Garcia, J., Dodge, A., Luepke, P., Wang, H. L., Kapila, Y., & Lin, G. H. (2018). Efeito da exposição da membrana na regeneração óssea guiada: Uma revisão sistemática e meta-análise. Clinical Oral Implants Research, 29, 328–338. https://doi.org/10.1111/clr.13121
- Gher, M. E., Quintero, G., Assad, D., Monaco, E., & Richardson, A. C. (1994). Enxertia óssea e regeneração óssea guiada para implantes dentários imediatos em humanos. Journal of Periodontology, 65, 881–891. https://doi.org/10.1902/jop.1994.65.9.881
- Hämmerle, C. H., Chen, S. T., & Wilson, T. G. Jr (2004). Declarações de consenso e procedimentos clínicos recomendados sobre a colocação de implantes em alvéolos de extração. International Journal of Oral and Maxillofacial Implants, 19(suppl), 26–28.
- Jepsen, S., Rühling, A., Jepsen, K., Ohlenbusch, B., & Albers, H. K. (1996). Peri-implantite progressiva. Incidência e previsão de perda de inserção peri-implantar. Clinical Oral Implants Research, 7, 133–142. https://doi.org/10.1034/j.1600-0501.1996.070207.x
- Jung, R. E., Herzog, M., Wolleb, K., Ramel, C. F., Thoma, D. S., & Hammerle, C. H. F. (2017). Um ensaio clínico controlado randomizado comparando pequenos defeitos de deiscência bucal ao redor de implantes dentários tratados com regeneração óssea guiada ou deixados para cicatrização espontânea. Clinical Oral Implants Research, 28, 348–354. https://doi.org/10.1111/clr.12806
- Luterbacher, S., Mayfield, L., Brägger, U., & Lang, N. P. (2000). Características diagnósticas de testes clínicos e microbiológicos para monitorar as condições dos tecidos mucosos periodontais e peri-implantares durante a terapia periodontal de suporte (SPT). Clinical Oral Implants Research, 11, 521–529. https://doi.org/10.1034/j.1600-0501.2000.011006521.x
- Merheb, J., Vercruyssen, M., Coucke, W., Beckers, L., Teughels, W., & Quirynen, M. (2017). O destino do osso bucal ao redor de implantes dentários. Um estudo de acompanhamento de 12 meses pós-carga. Clinical Oral Implants Research, 28, 103–108. https://doi.org/10.1111/clr.12767
- Monje, A., Chappuis, V., Monje, F., Muñoz, F., Wang, H. L., Urban, I. A., & Buser, D. (2019). A Espessura Crítica da Parede Óssea Bucal Peri-implantar Revisitada: Um Estudo Experimental no Cão Beagle. Int J Oral Maxillofac Implants, 34, 1328–1336. https://doi.org/10.11607/jomi.7657
- Nader, N., Aboulhosn, M., Berberi, A., Manal, C., & Younes, R. (2016). Remodelação óssea marginal ao redor do pilar de cicatrização vs colocação do pilar final na cirurgia de segundo estágio: Um ensaio clínico randomizado de 12 meses. Journal of Contemporary Dental Practice, 17, 7–15. https://doi.org/10.5005/jp-journals-10024
- O'Leary, T. J., Drake, R. B., & Naylor, J. E. (1972). O registro de controle de placa. Journal of Periodontology, 43, 38. https://doi.org/10.1902/jop.1972.43.1.38
- Perussolo, J., Souza, A. B., Matarazzo, F., Oliveira, R. P., & Araújo, M. G. (2018). Influência da mucosa queratinizada na estabilidade dos tecidos peri-implantares e desconforto ao escovar: Um estudo de acompanhamento de 4 anos. Clinical Oral Implant Research. Journal of Clinical Periodontology, 29, 1177–1185. https://doi.org/10.1111/clr.13381
- Pontoriero, R., Tonelli, M. P., Carnevale, G., Mombelli, A., Nyman, S. R., & Lang, N. P. (1994). Mucosite peri-implantar induzida experimentalmente. Um estudo clínico em humanos. Clinical Oral Implants Research, 5, 254–259. https://doi.org/10.1034/j.1600-0501.1994.050409.x
- Renvert, S., Persson, G. R., Pirih, F. Q., & Camargo, P. M. (2018). Saúde peri-implantar, mucosite peri-implantar e peri-implantite: Definições de caso e considerações diagnósticas. Journal of Clinical Periodontology, 45(Suppl 20), S278–S285. https://doi.org/10.1111/jcpe.12956
- Saleh, M. H. A., Ravidà, A., Suárez-López Del Amo, F., Lin, G.-H., Asa'ad, F., & Wang, H.-L. (2018). O efeito da posição da junção implante-pilar na perda óssea crestal: Uma revisão sistemática e meta-análise. Clinical Implant Dentistry and Related Research, 20, 617–633. https://doi.org/10.1111/cid.12600
- Salvi, G. E., Aglietta, M., Eick, S., Sculean, A., Lang, N. P., & Ramseier, C. A. (2012). Reversibilidade da mucosite peri-implantar experimental em comparação com gengivite experimental em humanos. Clinical Oral Implants Research, 23, 182–190. https://doi.org/10.1111/j.1600-0501.2011.02220.x
- Salvi, G. E., Monje, A., & Tomasi, C. (2018). Complicações biológicas de longo prazo de implantes dentários colocados em locais pristinos ou aumentados: Uma revisão sistemática e meta-análise. Clinical Oral Implant Research, 29(Suppl. 16), 294–310. https://doi.org/10.1111/clr.13123
- Sanz-Sánchez, I., Carrillo de Albornoz, A., Figuero, E., Schwarz, F., Jung, R., Sanz, M., & Thoma, D. (2018). Efeitos de procedimentos de aumento ósseo lateral na saúde ou doença peri-implantar: Uma revisão sistemática e meta-análise. Clinical Oral Implants Research, 29, 18–31. https://doi.org/10.1111/clr.13126
- Sanz-Sánchez, I., Ortiz-Vigón, A., Sanz-Martín, I., Figuero, E., & Sanz, M. (2015). Eficácia do aumento ósseo lateral na dimensão da crista alveolar: Uma revisão sistemática e meta-análise. Journal of Dental Research, 94, 1s–15s. https://doi.org/10.1177/0022034515594780
- Schwarz, F., Sahm, N., & Becker, J. (2012). Impacto do resultado da regeneração óssea guiada em defeitos do tipo deiscência na estabilidade a longo prazo da saúde peri-implantar: Observações clínicas em 4 anos. Clinical Oral Implants Research, 23, 191–196. https://doi.org/10.1111/j.1600-0501.2011.02214.x
- Spray, J. R., Black, C. G., Morris, H. F., & Ochi, S. (2000). A influência da espessura do osso na resposta óssea marginal facial: Colocação do estágio 1 através da descoberta do estágio 2. Annals of Periodontology, 5, 119–128. https://doi.org/10.1902/annals.2000.5.1.119
- Tawil, G., El-Ghoule, G., & Mawla, M. (2001). Avaliação clínica de uma membrana de colágeno bilaminada (bio-gide) suportada por autópsias no tratamento de defeitos ósseos ao redor de implantes. The International Journal of Oral & Maxillofacial Implants, 16, 857–863.
- Thoma, D. S., Bienz, S. P., Figuero, E., Jung, R. E., & Sanz-Martín, I. (2019). Efeitos de procedimentos de aumento de tecido mole na saúde ou doença peri-implantar: Uma revisão sistemática e meta-análise. Journal Clinical Periodontology, 46(Suppl 21), 257–276. https://doi.org/10.1111/jcpe.13050
- Trombelli, L., Farina, R., Ferrari, S., Pasetti, P., & Calura, G. (2009). Comparação entre dois métodos para avaliação de risco periodontal. Minerva Stomatologica, 58, 277–287.
- Trombelli, L., Minenna, L., Toselli, L., Zaetta, A., Checchi, L., Checchi, V., … Farina, R. (2017). Valor prognóstico de um método simplificado para avaliação de risco periodontal durante a terapia periodontal de suporte. Journal of Clinical Periodontology, 44, 51–57. https://doi.org/10.1111/jcpe.12645
- Trombelli, L., Severi, M., Farina, R., & Simonelli, A. (2020). Técnica de Camada Aumentada Sub-periosteal Peri-implantar para tratar lesões de peri-implantite. Clinical Advances in Periodontics. https://doi.org/10.1002/ cap.10107. [Epub ahead of print].
- Trombelli, L., Severi, M., Pramstraller, M., & Farina, R. (2018). Técnica de Camada Aumentada Sub-periosteal Peri-implantar para aumento ósseo horizontal na colocação de implantes. Minerva Stomatologica, 67, 217–224. https://doi.org/10.23736/S0026-4970.18.04161-4
- Trombelli, L., Severi, M., Pramstraller, M., & Farina, R. (2019). Uma gestão simplificada de tecido mole para aumento ósseo peri-implantar. International Journal of Oral and Maxillofacial Implants, 34, 197–204. https://doi.org/10.11607/jomi.6959
- Urban, I. A., Wessing, B., Alández, N., Meloni, S., González-Martin, O., Polizzi, G., … Zechner, W. (2019). Um ensaio clínico controlado randomizado multicêntrico usando uma nova membrana de colágeno para regeneração óssea guiada em locais de implantes únicos deiscente: Resultado na entrega protética e em acompanhamento de 1 ano. Clinical Oral Implant Research, 30, 487–497. https://doi.org/10.1111/clr.13426
- Zitzmann, N. U., Schärer, P., & Marinello, C. P. (2001). Resultados a longo prazo de implantes tratados com regeneração óssea guiada: Um estudo prospectivo de 5 anos. International Journal of Oral and Maxillofacial Implants, 16, 355–366.