Resultados do tratamento com implantes dentários em pacientes sob terapia ativa com alendronato: resultados de acompanhamento de 3 anos de um estudo observacional multicêntrico prospectivo.
Tradução automática
O artigo original está escrito em EN language (link para lê-lo) .
Resumo
Objetivo: Avaliar os dados clínicos e radiográficos de 3 anos de prótese dentária fixa suportada por implante entregues a pacientes que tomaram alendronato 35–70 mg semanalmente por pelo menos 3 anos antes da colocação do implante.
Materiais e Métodos: Quarenta pacientes consecutivos tratados com bisfosfonatos orais e que necessitavam de uma restauração suportada por implante foram recrutados em dois centros privados entre janeiro de 2008 e dezembro de 2011. Os implantes foram inseridos por meio de uma abordagem minimamente invasiva sob tratamento antibacteriano e antibiótico, 6 meses após a interrupção da administração de alendronato. Após 4 meses de cicatrização submersa, os implantes foram submetidos à carga protética. A manutenção da higiene e as avaliações clínicas foram agendadas a cada 4 meses durante 3 anos. As medidas de resultado foram as seguintes: sucesso do implante e da prótese, taxas de sobrevivência, quaisquer complicações clínicas observadas, remodelação óssea marginal, profundidade de sondagem e sangramento à sondagem.
Resultados: No final do estudo, oito pacientes desistiram. O tamanho da amostra final resultou em 32 pacientes parcialmente ou totalmente edêntulos (32 mulheres; idade média de 64,6 anos) com 98 implantes submersos. Em apenas um paciente, o implante maxilar falhou durante o período de cicatrização. Nenhuma prótese falhou durante todo o acompanhamento, e nenhuma complicação maior foi registrada. O sucesso dos implantes e próteses resultou em uma taxa de sobrevivência geral de 98, 98% e 100%, respectivamente. A perda óssea marginal média em três anos foi de 1,35 ± 0,21 (IC 95% 1,24–1,38). Parâmetros de tecido mole bem-sucedidos foram encontrados ao redor de todos os implantes.
Conclusões: A terapia com bisfosfonatos orais não pareceu afetar significativamente a sobrevivência e o sucesso dos implantes, caso haja seleção precisa do tempo de tratamento, abordagem cirúrgica minimamente invasiva e acompanhamento constante. Mais estudos prospectivos envolvendo tamanhos de amostra maiores e durações de acompanhamento mais longas são necessários para confirmar esses resultados.
Introdução
A osteoporose é uma doença esquelética sistêmica progressiva caracterizada por baixa massa óssea e deterioração microarquitetônica do tecido ósseo, com um consequente aumento da fragilidade óssea e suscetibilidade a fraturas (Kanis et al. 2008). O tratamento médico mais comum para a osteoporose envolve o uso de bisfosfonatos (BPs) (Bernabei et al. 2014). Em 2009, a Food and Drug Administration aprovou a injeção anual de ácido zoledrônico para a prevenção da osteoporose em populações menopáusicas (Khosla 2009). Os bisfosfonatos são análogos estáveis de pirofosfatos inorgânicos que ocorrem naturalmente e são classificados como medicamentos anti-reabsortivos (Fleisch et al. 1966), usados para diminuir a atividade dos osteoclastos, prevenir a reabsorção óssea e reduzir sua renovação (Reszka & Rodan 2004). Eles são comumente usados para tratar doenças que afetam o metabolismo ósseo, incluindo mieloma múltiplo, hipercalcemia secundária causada por tumores malignos, metástases ósseas em cânceres de próstata ou mama metastáticos, doença de Paget, bem como osteoporose (Sarzi Amadè et al. 2008).
A ação de um BP depende da estrutura química do medicamento. Tradicionalmente, os BPs são divididos em medicamentos que não contêm nitrogênio (non-N-BPs) e aqueles que contêm nitrogênio (N-BPs). Os bisfosfonatos não nitrogenados são metabolizados na célula em compostos que substituem o grupo pirofosfato terminal do ATP, formando uma molécula não funcional que compete com o trifosfato de adenosina (ATP) no metabolismo energético celular. O osteoclasto inicia a apoptose e morre, levando a uma diminuição geral na degradação do osso. A adição de um grupo amina ao final de uma cadeia lateral aumenta a potência do medicamento; no entanto, o mecanismo dos BPs que contêm nitrogênio é menos conhecido. De acordo com Reszka & Rodan (2004), os N-BPs inibem a enzima farnesil difosfato sintase da via de biossíntese do colesterol e interrompem a via de ramificação da isoprenilação, o que inibe proteínas e outros fatores que desempenham um papel limitante na reabsorção óssea pelos osteoclastos. Os N-BPs se acumulam em concentração máxima na matriz óssea e nos osteoclastos, principalmente durante as primeiras 24–48 h de medicação. O resultado final é a disfunção celular dos osteoclastos e a morte (Jones et al. 2001). A inibição resultante da reabsorção óssea normal leva a uma redução na renovação óssea, aumento da densidade óssea, melhora na mineralização e redução do risco de fratura (Jones et al. 2001).
O alendronato é um bisfosfonato contendo nitrogênio que tem sido amplamente utilizado para o tratamento da osteoporose (Tsetsenekou et al. 2012). Os efeitos do alendronato administrado localmente e/ou sistemicamente na osseointegração foram amplamente avaliados com experimentos realizados em animais (Abtahi et al. 2013). No entanto, de acordo com um grupo de trabalho criado pela Sociedade Americana de Pesquisa Óssea e Mineral, há poucas informações disponíveis sobre os efeitos colaterais dos N-BPs orais (Kos et al. 2010).
Duas revisões sistemáticas recentes da literatura sugerem que a ingestão de BPs orais não influenciou as taxas de sobrevivência de implantes a curto prazo (1–4 anos), mesmo quando ocorreram complicações (Madrid & Sanz 2009; Ata-Ali et al. 2014). No entanto, ainda faltam estudos prospectivos relatando taxas de sobrevivência e sucesso de implantes. Como diretrizes universalmente aceitas ainda não foram divulgadas, o manejo clínico da ONJ relacionada a bisfosfonatos continua controverso (Rupel et al. 2014). Desde 2003, foram publicados relatos sobre necrose dos ossos da mandíbula possivelmente associada à administração de bisfosfonatos (Hasegawa et al. 2012). Houve discussões sobre os riscos associados à realização de procedimentos cirúrgicos orais, particularmente enxertos ósseos e colocação de implantes, em pacientes que estão tomando BPs orais (Sarzi Amadè et al. 2008; Memon et al. 2012; Kwon et al. 2014). Os mesmos autores concluíram que a prevenção da ONJ relacionada a BP não é completamente possível, mas procedimentos preventivos não invasivos poderiam ajudar a diminuir sua incidência (Sarzi Amadè et al. 2008; Memon et al. 2012; Kwon et al. 2014). A Associação Americana de Cirurgiões Orais e Maxilofaciais recomenda que os pacientes suspendam os BPs 3 meses antes e 3 meses após a cirurgia oral, se possível, especialmente se um paciente estiver usando BPs por mais de 3 anos (Ruggiero et al. 2009; Allen & Ruggiero 2014). Para pacientes com histórico de tratamento com bisfosfonatos orais superior a 3 anos e aqueles em tratamento concomitante com prednisona, testes adicionais e opções de tratamento alternativas devem ser consideradas (Grant et al. 2008).
O objetivo deste estudo observacional prospectivo multicêntrico foi apresentar os dados de 3 anos sobre a sobrevivência e taxas de sucesso de implantes e próteses, bem como a perda óssea peri-implantar após a colocação de uma prótese dentária fixa suportada por implante, entregue a pacientes que tomam bisfosfonatos orais (alendronato 70 mg em comprimido uma vez por semana ou 5–10 mg uma vez ao dia) por pelo menos 3 anos antes da colocação do implante. Este estudo seguiu as diretrizes do STROBE (Fortalecimento da Reportagem de Estudos Observacionais em Epidemiologia).
Material e métodos
Desenho do estudo
Este estudo observacional prospectivo multicêntrico foi projetado para avaliar o resultado clínico e radiológico da prótese dentária fixa suportada por implante, entregue a pacientes que tomam alendronato 70 mg em comprimido uma vez por semana ou 5–10 mg uma vez ao dia, por pelo menos 3 anos antes da colocação do implante. Quarenta pacientes foram selecionados e tratados em dois centros privados (20 em Roma, 20 em Sassari, Itália), entre janeiro de 2008 e dezembro de 2011. Dois clínicos experientes realizaram todos os procedimentos de implantes e próteses. A investigação foi conduzida de acordo com os princípios contidos na Declaração de Helsinque de 1964 para pesquisa biomédica envolvendo sujeitos humanos, conforme emendada em 2008. Os pacientes foram informados sobre os procedimentos clínicos, materiais a serem utilizados, benefícios, riscos potenciais e complicações, bem como as avaliações de acompanhamento necessárias para o ensaio clínico, e deram seu consentimento por escrito para participar deste estudo.
Qualquer paciente saudável <90 anos, acima de 18 anos no momento da colocação do implante, que necessitasse de uma prótese suportada por implante foi convidado a participar da investigação em uma ordem consecutiva. Os pacientes foram incluídos no estudo após atender aos critérios de inclusão e não atender a nenhum dos critérios de exclusão.
Os critérios de exclusão foram os seguintes:
- Contraindicações médicas gerais (classe III ou IV da American Society of Anesthesiologist, ASA) e/ou psiquiátricas;
- Gravidez ou amamentação;
- Abuso de álcool ou drogas;
- Fumante pesado (>10 cigarros/dia);
- Terapia de radiação na região da cabeça ou pescoço nos últimos 5 anos;
- Atividade parafuncional alta e moderada;
- Ausência de dentes/prótese na mandíbula oposta;
- Periodontite não tratada;
- Implantes pós-extrativos;
- Sangramento bucal total e índice de placa bucal total maior ou igual a 25%;
- <10 mm de altura e 5 mm de largura de osso para permitir implantes;
- Indisponibilidade para acompanhamentos regulares.
Todos os pacientes foram tratados de acordo com um protocolo diagnóstico e terapêutico em duas etapas (Fig. 1). As etapas diagnósticas são as seguintes:
- Anamnese;
- Exame clínico e fotografias;
- Exame radiográfico incluindo raios-X periapicais e panorâmicos, tomografia computadorizada (TC) ou tomografia computadorizada de feixe cônico (CBCT);
- Exame periodontal (sondagem e medição dos índices de saúde bucal);
- Documentação fotográfica;
- Informações ao paciente (medicamentos a serem tomados e possíveis consequências).
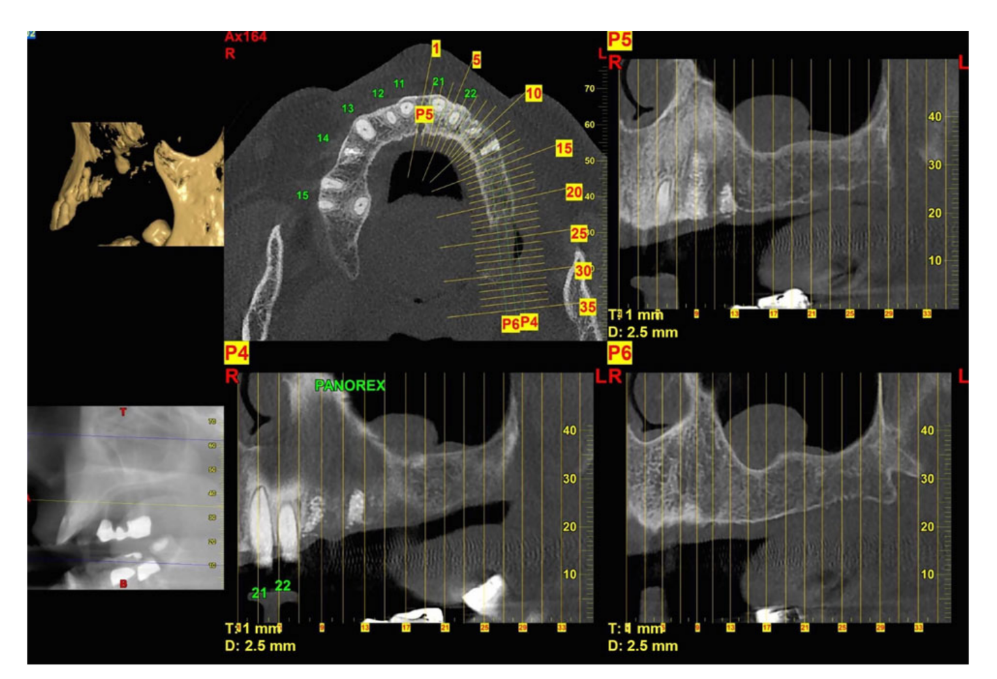
Procedimentos clínicos
Protocolo terapêutico (Tabela 1):
- Higiene profissional;
- Eliminação de todos os focos de infecção (raízes residuais, cáries, terapia periodontal):
- tratamento não restaurador-cirúrgico de todos os dentes comprometidos ou com prognóstico ruim;
- tratamento restaurador de dentes afetados por cárie;
- tratamento periodontal e terapia de suporte;
- avaliação da adequação das próteses removíveis e fixas. Em particular, foi avaliada a vedação das estruturas protéticas e a estabilidade da prótese removível, que deve ser atraumática.
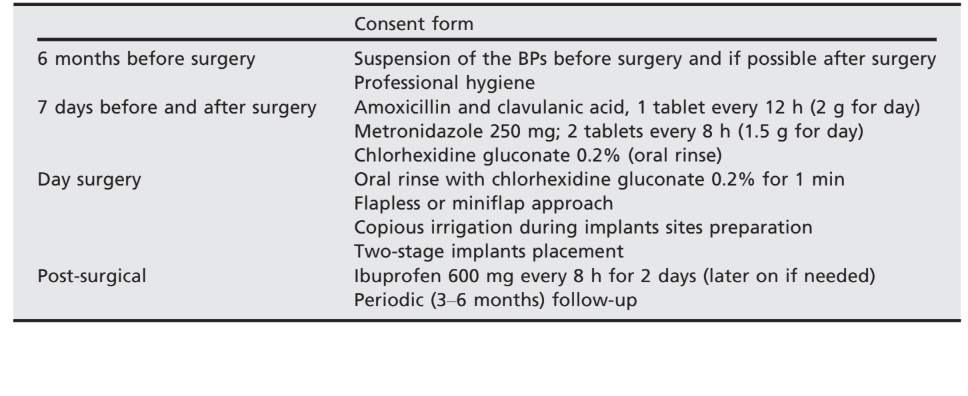
No final da fase de prevenção, os pacientes foram motivados a seguir um protocolo rigoroso de higiene bucal doméstica e a comparecer às consultas profissionais.
Dois cirurgiões experientes (MT & SMM) realizaram todas as intervenções. Quando planejada, a extração dentária atraumática foi realizada pelo menos 8 semanas antes da colocação do implante. Coroas de dentes multirradiculares foram seccionadas. As raízes foram então removidas individualmente e, se necessário, com a ajuda de um periotomo. Os alvéolos de extração residuais foram cuidadosamente desbravados de tecido de granulação e fibras residuais do ligamento periodontal com curetas.
O protocolo pré-cirúrgico exigia a suspensão dos BPs 6 meses antes da cirurgia e até a cicatrização completa, 4–6 meses após a instalação do implante. Antibióticos foram administrados profilaticamente 7 dias antes da cirurgia e continuaram por 7 dias (Sarzi Amadè et al. 2008):
- Amoxicilina e ácido clavulânico, um comprimido a cada 12 h (2 g por dia);
- Metronidazol 250 mg; dois comprimidos a cada 8 h (1,5 g por dia).
Antes do início da cirurgia, os pacientes enxaguaram com enxaguante bucal de clorexidina 0,2% por 1 min. A anestesia local foi induzida usando uma solução de articaína a 4% com epinefrina 1 : 100.000 (Ubistein; 3M Italy SpA, Milão, Itália). Os implantes foram colocados nos locais anatômicos planejados usando uma abordagem sem retalho ou uma abordagem de miniretalho, (Fig. 2). A densidade óssea foi avaliada durante a fase de perfuração pela experiência e sensação do clínico, e foi baseada na classificação de Lekholm e Zarb (Brånemark et al. 1985). Cada broca foi utilizada sob irrigação abundante de acordo com o protocolo recomendado pelo fabricante. A plataforma do implante foi posicionada ao nível da crista alveolar ou ligeiramente abaixo na área estética.
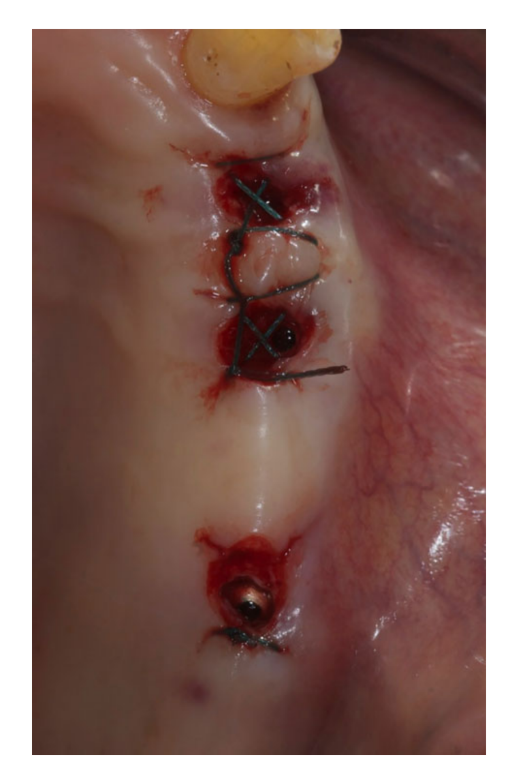
Após a colocação do implante, todos os pacientes receberam recomendações orais e escritas sobre medicação, manutenção da higiene bucal e dieta. O tratamento analgésico pós-cirúrgico foi realizado com ibuprofeno 100 mg, administrado a cada 8 h por 2 dias após a cirurgia, e posteriormente, se necessário. Os pacientes foram instruídos a enxaguar com enxaguante bucal de clorexidina 0,2% duas vezes ao dia, sem escovar a área do implante até a remoção dos pontos (10–14 dias depois).
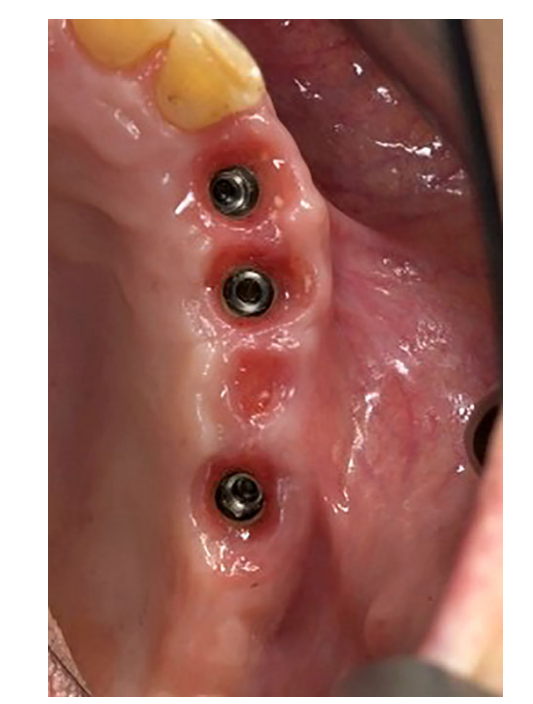
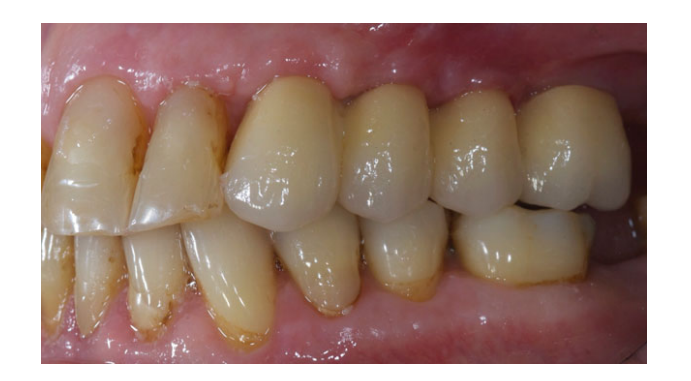
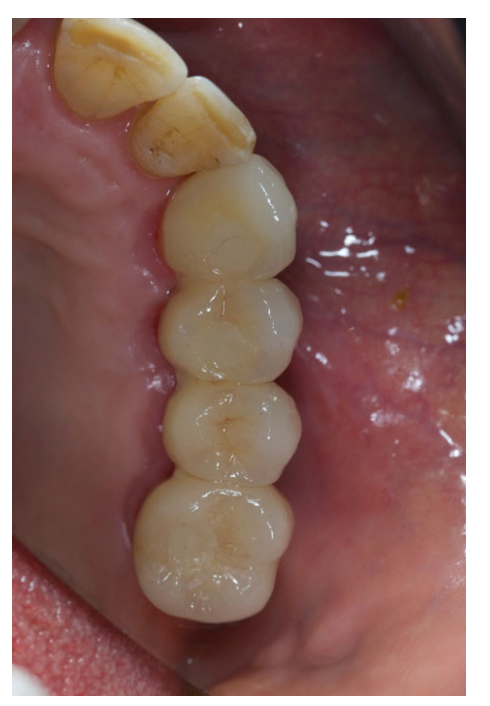
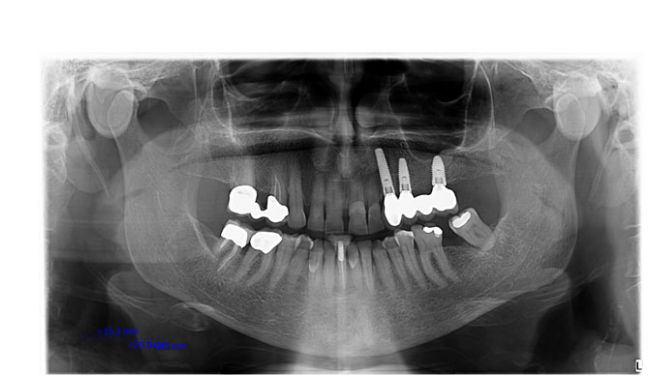
Todos os implantes foram colocados submersos. Os implantes foram expostos 3 meses após a colocação do implante (Figs 3 e 4). Impressões com bandeja aberta foram feitas usando um material de poliether (ImpregumTM, 3M ESPE, Seefeld, Alemanha) com uma bandeja aberta personalizada (Diatray Top, Dental Kontor, Stockelsdorf, Alemanha). No momento da entrega da prótese (Figs 5 e 6), a oclusão foi ajustada e as restaurações foram ou parafusadas ou cimentadas usando cimento de óxido de zinco sem eugenol (Temp Bond NE, Kerr Corporation, Orange, CA, EUA) 12 semanas após a primeira cirurgia, de acordo com um protocolo de carga convencional (Gallucci et al. 2013). As visitas de acompanhamento foram agendadas de 1 a 6 meses e, em seguida, anualmente até 3 anos de função (Fig. 7). Em cada visita de acompanhamento, o ajuste oclusal da prótese dentária foi realizado, se necessário. Os pacientes passaram por uma limpeza profissional por um higienista dental a cada 4–6 meses. Radiografias periapicais foram obtidas anualmente após a entrega da prótese definitiva com o mesmo suporte Rinn personalizado (Rinn, Elgin, IL, EUA).
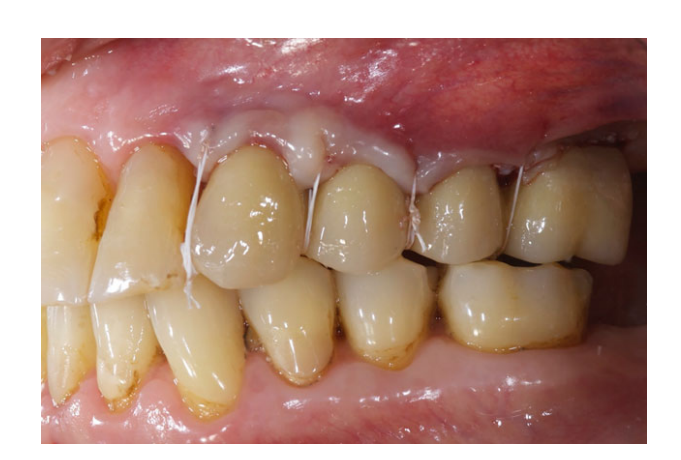
Medidas de resultado
As principais medidas de resultado foram as taxas de sucesso e sobrevivência do implante. Em cada exame de acompanhamento, os implantes foram examinados quanto à integração tecidual de acordo com os parâmetros rigorosos definidos por Buser et al. (1990). Especificamente, a integração foi considerada bem-sucedida se os seguintes parâmetros fossem atendidos: (1) ausência de infecção peri-implantar recorrente com supuração; (2) ausência de queixas subjetivas persistentes, como dor, sensação de corpo estranho e/ou disestesia; (3) ausência de radiolucidez contínua ao redor do implante e (4) ausência de qualquer mobilidade detectável do implante. Esses critérios se mostraram eficazes na definição do sucesso de um sistema de implante e na avaliação de resultados a longo prazo em ensaios clínicos. O sucesso da prótese foi avaliado seguindo uma modificação dos critérios de avaliação, sugerida pela Associação Dental da Califórnia (CDA (Associação CD 1976)).
Os desfechos secundários foram os seguintes: quaisquer complicações cirúrgicas e protéticas ocorridas durante todo o acompanhamento, perda óssea marginal, profundidade de sondagem de bolsa (PPD) e sangramento à sondagem (BOP).
- Complicações: Quaisquer complicações técnicas (fratura da estrutura e/ou do material de revestimento, afrouxamento de parafusos, etc.) e/ou biológicas (dor, inchaço, supuração, etc.) foram consideradas.
- Perda óssea marginal: A distância entre a margem mais coronal do colar do implante e o ponto mais coronal de contato osso-implante foi considerada como nível ósseo marginal (MBL). O MBL ao redor dos implantes foi avaliado em radiografias digitais intraorais obtidas com a técnica de paralelismo usando um suporte de filme (Rinn XCP, Dentsply, Elgin, IL, EUA) na colocação do implante (linha de base) e após 12, 24 e 36 meses. As radiografias foram aceitas ou rejeitadas para avaliação com base na clareza das roscas do implante. Todas as radiografias legíveis foram exibidas em um programa de análise de imagem (DFW2.8 para Windows, Soredex, Tuusula, Finlândia) em uma tela LCD de 24 polegadas (iMac, Apple, Cupertino, CA, EUA) e avaliadas sob condições padronizadas (SO 12646:2004). O software foi calibrado para cada imagem usando a distância conhecida do diâmetro ou comprimento do implante. Medições do nível da crista óssea mesial e distal adjacente a cada implante foram feitas com precisão de 0,1 mm e médias a nível do paciente.
- PPD e BoP foram medidos por um operador cego com uma sonda periodontal (PCP-UNC 15; Hu-Friedy Manufacturing, Chicago, IL, EUA) em 6, 12, 24 e 36 meses. Três valores vestibulares e três linguais foram coletados para cada implante e a média foi feita a nível do paciente.
Dois dentistas independentes e totalmente cegos (LC e EX) de cada centro avaliaram a sobrevivência e a taxa de sucesso do implante e da prótese. As complicações foram avaliadas e tratadas pelos clínicos que estavam em tratamento (MT e SMM), que não estavam cegos. A perda óssea marginal (DMBL) foi avaliada por um radiologista independente. Um higienista independente realizou todas as medições periodontais.
Análise estatística
A análise estatística foi realizada para parâmetros numéricos, como nível ósseo marginal e parâmetros de tecido mole, utilizando o SPSS para Mac OS X versão 22.0 (SPSS, Chicago, IL, EUA). Uma análise descritiva foi realizada utilizando a média, desvio padrão (DP) e mediana com intervalo de confiança (IC) de 95%. As taxas de sobrevivência e sucesso cumulativas foram calculadas usando os implantes e próteses como a unidade estatística das análises. As diferenças nos níveis ósseos marginais médios entre os acompanhamentos, médias a nível de paciente, foram comparadas pelo teste de postos sinalizados de Wilcoxon para amostras pareadas. O nível de significância estatística foi definido em 0,05. Comparações entre centros foram realizadas por análise de variância de uma via (ANOVA).
Resultados
No final do estudo, oito pacientes (20%) com 18 implantes (15,5%) desistiram. Um paciente no centro de Roma faleceu devido a câncer hepático. Cinco pacientes (dois no centro de Roma e três no centro de Sassari) tiveram sérios problemas de saúde não relacionados à terapia de implante dentário, de modo que não puderam comparecer às consultas de acompanhamento agendadas. Dois pacientes se mudaram para o exterior. No entanto, com base em uma entrevista por telefone, todos esses pacientes tinham seus implantes em funcionamento sem complicações relacionadas ao paciente (dor, inchaço). O tamanho final da amostra resultou em um total de 98 implantes com superfície oxidada rugosa e design de implante de corpo cônico (NobelReplace, Nobel Biocare AB) que foram colocados em 32 pacientes edêntulos consecutivos (32 mulheres) com uma idade média de 64,6 anos (faixa de 46 a 80). Cada centro tratou o mesmo número de 16 pacientes. Cada paciente foi acompanhado por ≥3 anos de função (faixa de 36 a 72 meses; média de 47,6 meses). Não houve desequilíbrios aparentes na linha de base entre os dois grupos, além de um número maior de implantes mais longos utilizados pelo centro de Roma e a presença de mais casos tratados com cirurgia assistida por computador baseada em template no centro da Sardenha. Nenhuma desvio do protocolo original ocorreu. Todos os dados coletados foram incluídos na análise estatística.
- Um dos 98 implantes (1,02%) falhou durante o período de cicatrização, antes da entrega das próteses finais, resultando em uma taxa de sobrevivência cumulativa de implantes de 98,98% no acompanhamento de 3 anos. A única falha de implante ocorreu em um paciente do centro da Sardenha (implante de plataforma estreita de 10 mm de comprimento). O implante não foi substituído.
- Na avaliação de acompanhamento de 3 anos, nenhuma das próteses definitivas havia falhado, resultando em uma taxa de sobrevivência prostética cumulativa de 100%.
- Nenhuma complicação protética foi observada. Nenhuma complicação biológica maior foi registrada. Três pacientes apresentaram inflamação mucosa peri-implantar com sangramento à sondagem após 6 meses. A melhoria na higiene bucal reduziu a inflamação peri-implantar, sem intervenções cirúrgicas.
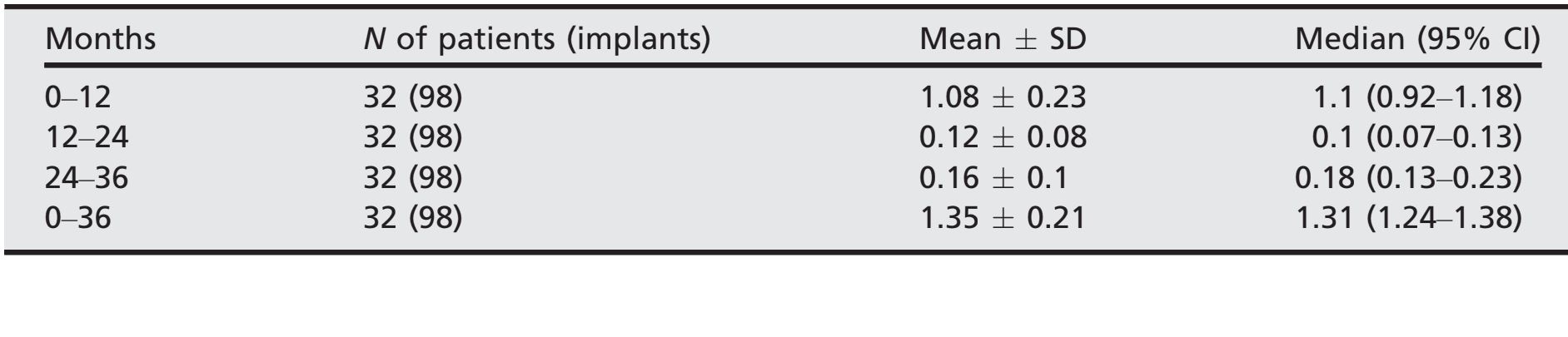
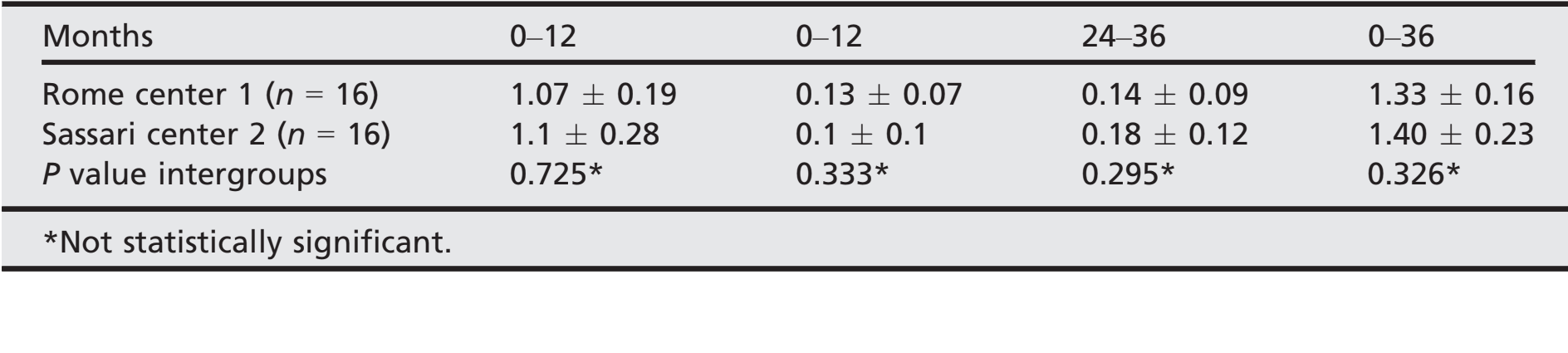
- Após uma perda óssea marginal média inicial de 1,08 ± 0,23 (mediana 1,1; IC 95% 0,92–1,18), todos os implantes perderam uma média de 0,12 ± 0,08 (mediana 0,1; IC 95% 0,07–0,13) entre o acompanhamento de 1 e 2 anos, e 0,16 ± 0,1 (mediana 0,18; IC 95% 0,13–0,23) entre o acompanhamento de 2 e 3 anos, sem diferença estatisticamente significativa (P = 0,059). No acompanhamento de 3 anos, a perda óssea marginal média foi de 1,35 ± 0,21 (mediana 1,31; IC 95% 1,24–1,38). Todos os dados estão relatados na Tabela 2. Em cada acompanhamento, as mudanças no nível ósseo foram semelhantes para ambos os centros (P ≥ 0,05). Todos os dados estão relatados na Tabela 3.
- Na avaliação de acompanhamento de 3 anos, os valores médios de PPD foram de 2,71 ± 0,38 mm (IC 95% = 2,54–2,86). Os valores médios de sangramento à sondagem foram de 1,29 ± 0,76 (IC 95% = 0,93–1,63).
Discussões
O presente estudo observacional prospectivo foi projetado para avaliar os resultados clínicos e radiográficos de 3 anos de uma prótese dentária fixa suportada por implante entregue a pacientes que tomam alendronato 70 mg em comprimido uma vez por semana ou 5–10 mg uma vez ao dia por pelo menos 3 anos antes da colocação do implante.
Na avaliação de acompanhamento de 3 anos, os resultados do presente estudo mostraram uma taxa de sobrevivência do implante e da prótese de 99% e 100%, respectivamente. As mudanças ósseas marginais, bem como os valores de BOP e PPD parecem estar estáveis após 3 anos, confirmando que a terapia com implantes em pacientes que tomam BPs orais é um tratamento viável de acordo com o protocolo terapêutico proposto. Esses resultados são consistentes com outros estudos que investigam o mesmo tópico. Em um estudo retrospectivo, Memon et al. (2012) concluíram que os bisfosfonatos não afetaram o sucesso inicial do implante ou as mudanças no osso crestal. Jeffcoat (2006) e Russo Dello et al. (2007), em dois estudos prospectivos, relataram que os BPs orais não pareciam aumentar a incidência de ONJ. Grant et al. (2008), em um estudo retrospectivo com 115 pacientes (468 implantes), relataram que a terapia com bisfosfonato oral não parecia afetar significativamente o sucesso do implante.
As principais limitações deste estudo são o número limitado de participantes, acompanhados por um curto período. No entanto, mesmo que oito pacientes tenham desistido, 98 implantes foram colocados em 32 pacientes tratados com o mesmo protocolo, e acompanhados por pelo menos 3 anos, permitindo que os resultados do presente estudo sejam generalizados para uma população maior com características semelhantes.
Estudos em animais mostraram que a administração de BPs interfere na remodelação óssea normal após a extração do dente, comprometendo a cicatrização a longo prazo ao redor dos implantes (Kim et al. 2013). Uma das complicações mais sérias, embora infrequente, é a osteonecrose dos maxilares relacionada a bisfosfonatos (BRONJ) (Kwon et al. 2014). A frequência de BRONJ pode variar dependendo da via de administração e da potência dos medicamentos utilizados. A Associação Americana de Cirurgiões Orais e Maxilofaciais relatou que a prevalência de BRONJ era de cerca de 0,8% a 12% quando os BPs são administrados por via intravenosa (Ruggiero et al. 2009; Allen & Ruggiero 2014). A prevalência é supostamente menor quando os BPs são administrados por via oral. No entanto, foi sugerido que atenção especial deve ser dada quando os pacientes se submetem ao tratamento com BPs por mais de 3 anos, pois a prevalência de BRONJ aumenta ao longo do período de tratamento com BPs (Sarzi Amade` et al. 2008). Após resultados preliminares pouco entusiasmados baseados em estudos retrospectivos não controlados, algumas revisões sistemáticas sugeriram resultados mais entusiasmados. Madrid & Sanz (2009) concluíram que um paciente recebendo bisfosfonatos orais por um período de <5 anos é “seguro” para se submeter a procedimentos dentários, especificamente implantes dentários (Madrid & Sanz 2009). Além disso, há um consenso geral sobre a não contraindicação da colocação de implantes em pacientes não oncológicos sob BPs orais, prescritos principalmente para osteoporose (Madrid & Sanz 2009). Mais recentemente, Kumar & Honne (2012) avaliando a sobrevivência de implantes dentários em usuários de bisfosfonatos vs. não usuários, concluíram que a terapia de BPs a curto prazo não aumenta nem diminui a taxa de sobrevivência de implantes dentários em comparação com não usuários.
Embora a técnica submersa não seja um pré-requisito para a osseointegração (Tallarico et al. 2011), no presente estudo todos os implantes foram colocados submersos, sem quaisquer complicações cirúrgicas. Isso pode representar um dos fatores-chave juntamente com um tratamento antibiótico significativo e a interrupção temporária da administração de alendronato, prevenindo a contaminação bacteriana do local do implante.
No presente estudo, embora o número limitado de pacientes, a cirurgia de implante não resultou em osteonecrose da mandíbula relacionada ao bisfosfonato após 3 anos da colocação do implante. No entanto, existem evidências suficientes para sugerir que todos os pacientes submetidos à colocação de implantes devem ser questionados sobre a terapia com bisfosfonato, incluindo o medicamento tomado, a dosagem e a duração do tratamento antes da cirurgia. Os riscos potenciais de BRONJ precisam ser explicados aos pacientes antes da instalação do implante. Para pacientes com histórico de tratamento oral com bisfosfonato superior a 3 anos e aqueles em tratamento concomitante com prednisona, testes adicionais e opções de tratamento alternativas devem ser considerados e a prevenção ainda é o meio mais eficaz para evitar possíveis complicações. Além disso, a localização anatômica do implante e a duração da terapia medicamentosa no momento da colocação não foram fatores significativos na taxa de sucesso ou nas alterações ósseas.
Conclusão
Dentro das limitações deste estudo, de acordo com o protocolo terapêutico proposto e realizando uma cirurgia submersa minimamente invasiva, a terapia com bisfosfonatos orais não pareceu afetar significativamente a sobrevivência e o sucesso do implante no acompanhamento de médio prazo. Essas conclusões devem ser confirmadas por novos estudos prospectivos envolvendo tamanhos de amostra maiores e durações de acompanhamento mais longas.
Marco Tallarico, Luigi Canullo
Referências
- Abtahi, J., Agholme, F., Sandberg, O. & Aspenberg, P. (2013) Efeito da entrega local vs. sistêmica de bisfosfonatos na fixação de implantes dentários em um modelo de osteonecrose da mandíbula. Journal of Dental Research 92: 279–283.
- Allen, M.R. & Ruggiero, S.L. (2014) Uma revisão de agentes farmacêuticos e saúde óssea oral: como a osteonecrose da mandíbula afetou o campo. International Journal of Oral and Maxillofacial Implants 29: e45–e57.
- Ata-Ali, J., Ata-Ali, F., Penarrocha-Oltra, D. & Galindo-Moreno, P. (2014) Qual é o impacto da terapia com bisfosfonatos sobre a sobrevivência de implantes dentários? Uma revisão sistemática e meta-análise. Clinical Oral Implants Research doi: 10.1111/clr.12526. [Epub ahead of print].
- Bernabei, R., Martone, A.M., Ortolani, E., Landi, F. & Marzetti, E. (2014) Triagem, diagnóstico e tratamento da osteoporose: uma breve revisão. Clinical Cases in Mineral and Bone Metabolism 11: 201–207.
- Brånemark, P.I., Zarb, G.A. & Albrektsson, T. (1985) Prótese Integrada ao Tecido: Osseointegração na Odontologia Clínica. Chicago: Quintessence ed.
- Buser, D., Weber, H.P. & Lang, N.P. (1990) Integração tecidual de implantes não submersos. Resultados de 1 ano de um estudo prospectivo com 100 implantes de cilindro oco e parafuso oco ITI. Clinical Oral Implants Research 1: 33–40.
- California Dental Association, Task Force on Quality Evaluation. (1976) Avaliação de Qualidade para Cuidados Dentários: Diretrizes para a Avaliação da Qualidade Clínica e Desempenho Profissional e os Padrões para o Programa de Design para Garantir a Qualidade do Atendimento. Los Angeles: California Dental Association ed. Chicago.
- Fleisch, H., Russell, R. & Straumann, F. (1966) Efeito do pirofosfato sobre a hidroxiapatita e suas implicações na homeostase do cálcio. Nature 212: 901–903.
- Grant, B.T., Amenedo, C., Freeman, K. & Kraut, R.A. (2008) Resultados da colocação de implantes dentários em pacientes que tomam bisfosfonatos orais: uma revisão de 115 casos. Journal of Oral and Maxillofacial Surgery 66: 223–230.
- Hasegawa, Y., Kawabe, M., Kimura, H., Kurita, K., Fukuta, J. & Urade, M. (2012) Influência das dentaduras no local de ocorrência inicial sobre o prognóstico da osteonecrose da mandíbula relacionada a bisfosfonatos: um estudo retrospectivo. Oral Surgery, Oral Medicine, Oral Pathology and Oral Radiology 114: 318–824.
- Jeffcoat, M.K. (2006) Segurança dos bisfosfonatos orais: estudos controlados sobre o osso alveolar. International Journal of Oral and Maxillofacial Implants 21: 349–353.
- Jones, D.H., Nakashima, T., Sanchez, O.H., Kozieradzki, I., Komarova, S.V., Sarosi, I., Morony, S., Rubin, E., Sarao, R., Hojilla, C.V., Komnenovic, V., Kong, Y.Y., Schreiber, M., Dixon, S.J., Sims, S.M., Khokha, R., Wada, T. & Penninger, J.M. (2006) Regulação da migração de células cancerosas e metástase óssea por RANKL. Nature 440: 692–696.
- Kanis, J.A., McCloskey, E.V., Johansson, H., Oden, A., Melton, L.J. & Khaltaev, N. (2008) Um padrão de referência para a descrição da osteoporose. Bone 42: 467–475.
- Khosla, S. (2009) Aumento das opções para o tratamento da osteoporose. New England Journal of Medicine 361: 818–820.
- Kim, I., Ki, H., Lee, W., Kim, H. & Park, J.B. (2013) O efeito dos bisfosfonatos administrados sistemicamente na cicatrização óssea após a extração dentária e na osseointegração de implantes dentários na maxila de coelhos. International Journal of Oral and Maxillofacial Implants 28: 1194–1200.
- Kos, M., Brusco, D., Kuebler, J. & Engelke, W. (2010b) Comparação clínica de pacientes com osteonecrose das mandíbulas, com e sem histórico de administração de bisfosfonatos. International Journal of Oral and Maxillofacial Surgery 39: 1097–1102.
- Kos, M., Kuebler, J.F., Luczak, K. & Engelke, W. (2010a) Osteonecrose das mandíbulas relacionada a bisfosfonatos: uma revisão de 34 casos e avaliação de risco. Journal of Cranio-Maxillofacial Surgery 38: 255–259.
- Kumar, M.N. & Honne, T. (2012) Sobrevivência de implantes dentários em usuários de bisfosfonatos versus não usuários: uma revisão sistemática. The European Journal of Prosthodontics and Restorative Dentistry 20: 159–162.
- Kwon, T.G., Lee, C.O., Park, J.W., Choi, S.Y., Rijal, G. & Shin, H.I. (2014) Osteonecrose associada a implantes dentários em pacientes em tratamento com bisfosfonatos. Clinical Oral Implants Research 25: 632–640.
- Madrid, C. & Sanz, M. (2009) Que impacto os bisfosfonatos administrados sistemicamente têm na terapia de implantes orais? Uma revisão sistemática. Clinical Oral Implants Research 20: 87–95.
- Memon, S., Weltman, R.L. & Katancik, J.A. (2012) Bisfosfonatos orais: sucesso inicial de implantes dentários endosseosos e mudanças no osso crestal. Um estudo retrospectivo. International Journal of Oral and Maxillofacial Implants 27: 1216–1222.
- Reszka, A.A. & Rodan, G.A. (2004) Mecanismo de ação dos bisfosfonatos contendo nitrogênio. Mini Reviews in Medicinal Chemistry 4: 711–719.
- Ruggiero, S.L., Dodson, T.B., Assael, L.A., Landesberg, R., Marx, R.E. & Mehrotra, B. (2009) Documento de posição da American Association of Oral and Maxillofacial Surgeons sobre osteonecrose da mandíbula relacionada a bisfosfonatos – atualização de 2009. Australian Endodontic Journal 35: 119–130.
- Rupel, K., Ottaviani, G., Gobbo, M., Contardo, L., Tirelli, G., Vescovi, P., Di Lenarda, R. & Biasotto, M. (2014) Uma revisão sistemática das abordagens terapêuticas na osteonecrose da mandíbula relacionada a bisfosfonatos (BRONJ). Oral Oncology 50: 1049-1057. Russo Dello, N.M., Jeffcoat, M.K., Marx, R.E. & Fugazzotto, P. (2007) Osteonecrose nas mandíbulas de pacientes que estão usando bisfosfonatos orais para tratar osteoporose. International Journal of Oral and Maxillofacial Implants 22: 146–153.
- Sarzi Amadè, D., Tallarico, M., Loreti, M.C., Montecchi, P.P. & Niccoli, A. (2008) Diretrizes clínicas para prevenção da osteonecrose das mandíbulas em pacientes em tratamento com bisfosfonatos: revisão da literatura e relato de três casos. Minerva Stomatologica 57: 429–446.
- Tallarico, M., Vaccarella, A. & Marzi, G.C. (2011) Resultados clínicos e radiológicos da colocação de implantes em 1 ou 2 estágios: resultados de 1 ano de um ensaio clínico randomizado. European Journal of Oral Implantology 4: 13–20.
- Tsetsenekou, E., Papadopoulos, T., Kalyvas, D., Papaioannou, N., Tangl, S. & Watzek, G. (2012) A influência do alendronato na osseointegração de implantes dentários tratados com nanoterapia em coelhos da Nova Zelândia. Clinical Oral Implants Research 23: 659–666.