O Uso do Tratamento de Superfície com Plasma a Vácuo para Melhorar a Hidrofobicidade e Molhabilidade de Substitutos de Enxerto Ósseo e Membranas Resorvíveis: Um Estudo In Vitro
Tradução automática
O artigo original está escrito em EN language (link para lê-lo) .
Resumo
Contexto/Objetivos: Desejamos avaliar in vitro se o tratamento de superfície com plasma a vácuo de substitutos de enxerto ósseo e membranas reabsorvíveis poderia melhorar a hidrofobicidade e a molhabilidade dos materiais testados.
Métodos: No total, 28 amostras esterilizadas foram consideradas para esta pesquisa e divididas em três grupos. Seis amostras foram utilizadas para a análise SEM-EDS. As outras 22 amostras foram atribuídas aleatoriamente aos grupos de teste (tratadas com plasma, n = 11) e controle (sem tratamento, n = 11). O tratamento de superfície com plasma a vácuo foi realizado no grupo de teste antes da análise SEM-EDS usando o ACTILINK renascente com um suporte de material (Plasmapp Co., Ltd., Daejeon, República da Coreia). Tintas Plasmatreat (Plasmatreat, Steinhagen, Alemanha) foram utilizadas para avaliar as diferenças na hidrofobicidade entre os grupos de teste e controle. As medidas de resultado foram o tempo de absorção, grau de molhabilidade e grau de descontaminação após diferentes ciclos de tempo.
Resultados: Após o tratamento de superfície com plasma a vácuo, o tempo de absorção das tintas diminuiu estatisticamente em todos os subgrupos (p < 0,05), enquanto o grau de molhabilidade aumentou. As análises de SEM-EDS mostraram uma taxa de redução aumentada de impurezas de carbono após até três ciclos de tratamento de superfície com plasma a vácuo. Além disso, a análise de SEM-EDS não revelou áreas de dano causadas pelos múltiplos tratamentos.
Conclusões: Dentro das limitações deste estudo in vitro, o tratamento de superfície com plasma a vácuo aumentou a hidrofobicidade e a molhabilidade dos biomateriais testados. O enxerto ósseo particulado e os blocos ósseos devem ser tratados utilizando programas de tempo mais longos. Mais ensaios clínicos randomizados bem conduzidos com cálculos de tamanho de amostra são necessários para confirmar esses resultados preliminares.
Introdução
A implantologia oral é reconhecida como uma metodologia clínica segura e previsível capaz de garantir resultados a longo prazo no campo da reabilitação oral. A osseointegração de implantes dentários tem sua origem no início da década de 1950, quando o Prof. Per-Ingvar Brånemark, um cirurgião ortopédico sueco, realizou originalmente experimentos ortopédicos em pernas de coelhos. Atualmente, um implante é considerado osseointegrado quando não há progressão
movimento relativo entre o implante e o osso com o qual deve ter contato direto. No passado, um dos aspectos mais importantes para alcançar a osseointegração era a estabilidade primária durante a colocação do implante. Desde suas origens até hoje, a literatura tem se concentrado em princípios puramente orientados biologicamente. Em relação a este último, numerosos métodos de tratamento de superfície foram investigados e implementados para melhorar as características biológicas da superfície dos implantes, incluindo modificações na rugosidade da superfície do implante e melhorias na hidrofobicidade dentro do processo de osseointegração. De acordo com estudos recentes, ambos os tratamentos parecem melhorar o mecanismo de osseointegração, com formação óssea mais forte e rápida, permitindo uma osseointegração mais rápida e resultados de longo prazo bem-sucedidos.
Vários estudos avaliaram o tratamento de superfície de implantes dentários e pilares. A ativação da superfície de um implante de titânio através do tratamento a plasma poderia representar uma estratégia positiva para remover contaminantes de pilares dentários e minimizar a reabsorção óssea peri-implantar, bem como aumentar as porcentagens de novo osso em estreito contato com a superfície do implante. Este fenômeno foi demonstrado ser mediado in vitro pelo aumento da adsorção de proteínas e adesão de osteoblastos na superfície de titânio. No entanto, ao melhor conhecimento dos autores e no momento da redação, nenhuma pesquisa avaliou tratamentos que sejam capazes de aumentar a energia superficial de substitutos ósseos e membranas. Em um estudo animal, Ho Jik Yang et al. avaliaram o efeito do tratamento de superfície a plasma a vácuo em uma matriz dérmica acelular humana, destacando o efeito potencial do tratamento na melhoria dos resultados de cirurgia reconstrutiva. O tratamento de superfície a plasma a vácuo também demonstrou uma melhoria na adesão celular, modificando a molhabilidade da superfície da placa de titânio, com uma redução no ângulo de contato entre fluidos biológicos e a superfície do implante que favorece a difusão de células osteoblásticas e não deixa resíduos após o tratamento. Algumas mudanças nas características físico-químicas foram relatadas, como a energia livre da superfície, conteúdo de hidrocarbonetos e grupos hidroxila funcionais, que poderiam potencialmente influenciar a resposta inflamatória no tecido peri-implantar. Em um ensaio clínico controlado randomizado, o tratamento a plasma de argônio demonstrou uma redução na remodelação óssea peri-implantar, com resultados estatisticamente mais fortes em até 5 anos de acompanhamento.
O objetivo principal deste estudo in vitro foi avaliar se o tratamento de superfície com plasma a vácuo de substitutos de enxerto ósseo e membranas reabsorvíveis, comumente utilizados para preservação de alvéolos e procedimentos de GBR, poderia melhorar a energia de superfície (hidrofobicidade) e a molhabilidade dos materiais testados. A hipótese nula era que o tratamento de superfície com plasma a vácuo não tinha efeito sobre o tempo de absorção ou a molhabilidade. Um objetivo secundário foi avaliar, utilizando análises SEM-EDS, o grau de descontaminação após diferentes ciclos de tempo. Este estudo foi relatado de acordo com as diretrizes CRIS (Checklist para Relato de Estudos In-vitro).
Materiais e Métodos
2.1 Amostras
No total, 28 amostras esterilizadas foram consideradas nesta pesquisa in vitro randomizada (teste e controle). Nenhum cálculo do tamanho da amostra foi realizado devido à ausência de outros estudos na literatura científica que comparassem biomateriais com e sem tratamento de superfície com plasma a vácuo. O número máximo de amostras foi utilizado de acordo com a disponibilidade do departamento. As amostras incluíram diferentes biomateriais comumente utilizados durante a preservação de alvéolos e/ou procedimentos de GBR e são relatadas da seguinte forma:
- Quatorze blocos RE-BONE de 10 × 10 × 10 (8) e 10 × 10 × 20 (6) mm (UBGEN SRL, Vigonza, Itália);
- Quatro membranas de pericárdio HEART (Bioteck SPA, Arcugnano, Itália);
- Dois grânulos esponjosos, 0,5 g~1 cc, 0,25–1 mm, OSTEOXENON (Bioteck SPA, Itália);
- Quatro grânulos esponjosos, 0,5 g, 0,25–1 mm (não colágeno), BIO-GEN (Bioteck SPA, Itália);
- Quatro XCs colágeno Xenomatrixes (Bioteck SPA).
No total, 6 de 28 amostras (blocos RE-BONE [UBGEN SRL, Vigonza, Itália]) foram utilizadas para a análise SEM-EDS. As outras 22 amostras foram divididas aleatoriamente em dois grupos iguais de 11 amostras (teste, tratado com plasma, e controle, sem tratamento) e testadas para avaliar os tempos de absorção e os graus de molhabilidade. Todas as medições foram realizadas no Departamento de Medicina, Cirurgia e Farmácia, da Universidade de Sassari, Itália. A análise SEM-EDS de três dos blocos RE-BONE tratados com plasma (UBGEN SRL) foi realizada no Centro de P&D Plasmapp (Plasmapp Co, República da Coreia).
O ACTILINK renasceu com um suporte de material (Plasmapp Co., Ltd., Daejeon, República da Coreia) que foi utilizado para tratar as amostras. As tintas Plasmatreat (Plasmatreat, Steinhagen, Alemanha) com diferentes tensões superficiais foram utilizadas. A energia superficial de diferentes biomateriais estéreis com (teste) e sem (controle) tratamento de superfície a plasma a vácuo foi avaliada medindo-se o ângulo de contato (para avaliar a molhabilidade) e o tempo de absorção (para avaliar a hidrofobicidade) das tintas utilizadas.
2.2 Tratamento de Superfície a Plasma a Vácuo
No grupo de teste, o tratamento de superfície a plasma a vácuo foi realizado usando a máquina ACTILINK renascida (Figura 1) com um suporte personalizado (um suporte de vórtice), projetado para fácil utilização. De acordo com o protocolo dos fabricantes, o tempo de ciclo do tratamento de superfície a plasma a vácuo, denominado modo VORTEX PLASMA, foi de 30 s. Todos os biomateriais no grupo de teste passaram pelo mesmo tempo de ciclo de tratamento de superfície a plasma a vácuo. Em contrapartida, nenhum dos biomateriais no grupo controle recebeu qualquer tipo de tratamento. No grupo de teste, após abrir a caixa estéril, o biomaterial testado foi retirado com uma pinça estéril e inserido no suporte de vórtice estéril, e finalmente, foi colocado na máquina ACTILINK para o tratamento de superfície a plasma a vácuo. Assim que o tratamento terminou, tanto os biomateriais tratados quanto os não tratados foram inseridos usando uma pinça estéril no suporte esterilizado, e cinco gotas das tintas Plasmatreat, com duas diferentes tensões superficiais (56 e 72 mN/m), foram colocadas em cada amostra. Imediatamente após, o respectivo tempo de absorção e grau de molhabilidade foram registrados, fotografados e criticamente comparados para avaliar a hidrofobicidade e o ângulo de contato entre a tinta e a superfície dos biomateriais utilizados. Tensões superficiais de 56 e 72 mN/m foram utilizadas porque o valor de 56 mN/m estava mais próximo do sangue humano.

2.3 Análise SEM
Para avaliar o efeito do tempo de tratamento a plasma a vácuo na descontaminação (reduzindo as impurezas de carbono) da superfície de um bloco ósseo, três blocos RE-BONE (UBGEN SRL) foram analisados usando o sistema SEM-EDS após até três ciclos de tratamento de superfície a plasma a vácuo. Seis blocos RE-BONE de 10 × 10 × 20 mm (UBGEN SRL) foram utilizados para o exame SEM-EDS. Dois blocos RE-BONE (UBGEN SRL) foram tratados sob três ciclos diferentes cada ([A] 30 s, [B] 60 s e [C] 90 s) antes do tratamento de superfície a plasma a vácuo. A máquina ACTILINK renascida foi utilizada no modo VORTEX PLASMA. Após cada ciclo de tratamento, os blocos ósseos foram analisados sob um microscópio eletrônico de varredura (SEM, Thermo Fisher Scientific, Phenom XL, Waltham, MA, EUA) conectado a um espectroscópio de raios X por dispersão de energia (EDS) para permitir uma análise direcionada das superfícies das amostras.
2.4 Medidas de Resultado
O tempo de absorção e o grau de molhabilidade foram avaliados a partir de vídeos gravados durante os procedimentos (Blackmagic Design Pocket Cinema Camera 4K, Blackmagic, Fremont, CA, EUA). Os grupos de teste e controle foram testados em comparação ao mesmo tempo. Dois pesquisadores realizaram todos os testes (M.T. e M.T).
- O tempo de absorção foi definido como o intervalo, em segundos, desde o momento em que a última gota tocou a superfície do biomaterial até o momento em que todas as gotas de tinta foram absorvidas pelo biomaterial. O vídeo gravado foi avaliado usando um aplicativo de edição de vídeo (iMovie para MacOS), e o tempo de absorção foi medido usando a linha do tempo expandida. Todas as medições foram repetidas três vezes por dois operadores diferentes (M.T. e M.T.). O valor médio e o desvio padrão (DP) foram calculados.
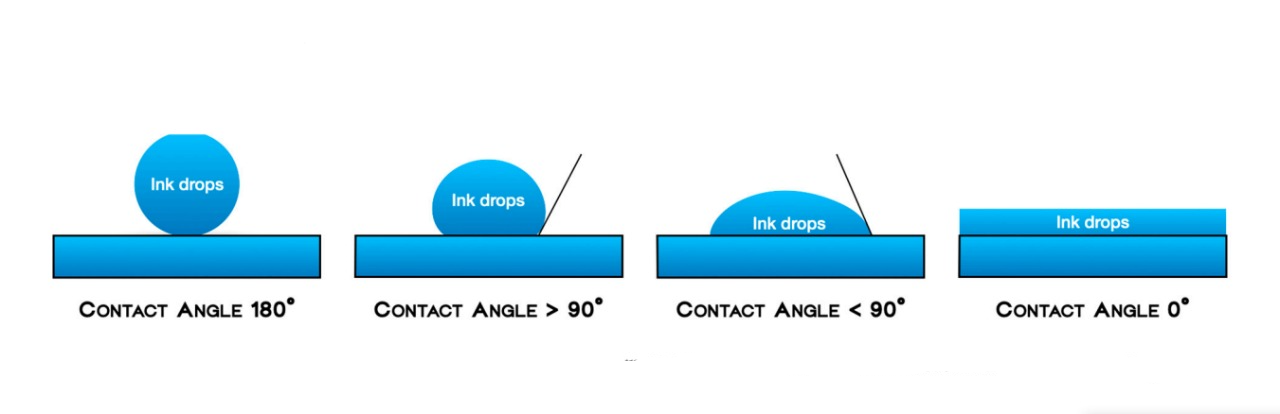
- A molhabilidade (geralmente referida como hidrofobicidade) foi definida como a dispersão das gotas de tinta sobre as superfícies dos biomateriais, medida pela planicidade de uma gota na superfície sólida. Os quatro graus de molhabilidade foram definidos da seguinte forma:
Nota nula: As gotas de tinta permaneceram na mesma posição em que foram deixadas, com um ângulo de contato de 180°; Nota baixa: Quando a mancha de tinta se alargou ligeiramente na superfície, com um ângulo de contato > 90°; Nota média: Quando a expansão moderada da mancha de tinta na superfície era apreciável e o ângulo de contato era <90°; Nota alta: Quando a mancha de tinta foi definitivamente absorvida, com um ângulo de contato de 0° (Figura 2).
- Análise SEM. A microscopia eletrônica de varredura foi empregada para visualizar imagens de alta resolução das superfícies das amostras. Usando o SEM, a topografia da superfície nas imagens foi analisada. Em particular, as imagens do SEM foram usadas para avaliar a taxa de redução de impurezas de carbono com três tempos de ciclo diferentes. O detector de espectroscopia de raios X por dispersão de energia (EDS) foi utilizado para medir a energia dos fótons emitidos no espectro eletromagnético de raios X e para obter informações químicas (a porcentagem atômica).
2.5 Análise Estatística
A análise de dados foi realizada de acordo com um plano de análise pré-estabelecido. Um bioestatístico com experiência em odontologia analisou os dados usando o software Ky Plot 2.0, Informer Technologies, Inc. NY, EUA, sem conhecer os códigos dos grupos. Os valores médios e desvios padrão foram calculados para cada medição. Um calculador de teste Kolmogorov–Smirnov de duas amostras foi utilizado para comparar o tempo de absorção entre os grupos. Comparações estatísticas foram realizadas no nível de significância de 0,05.
Resultados
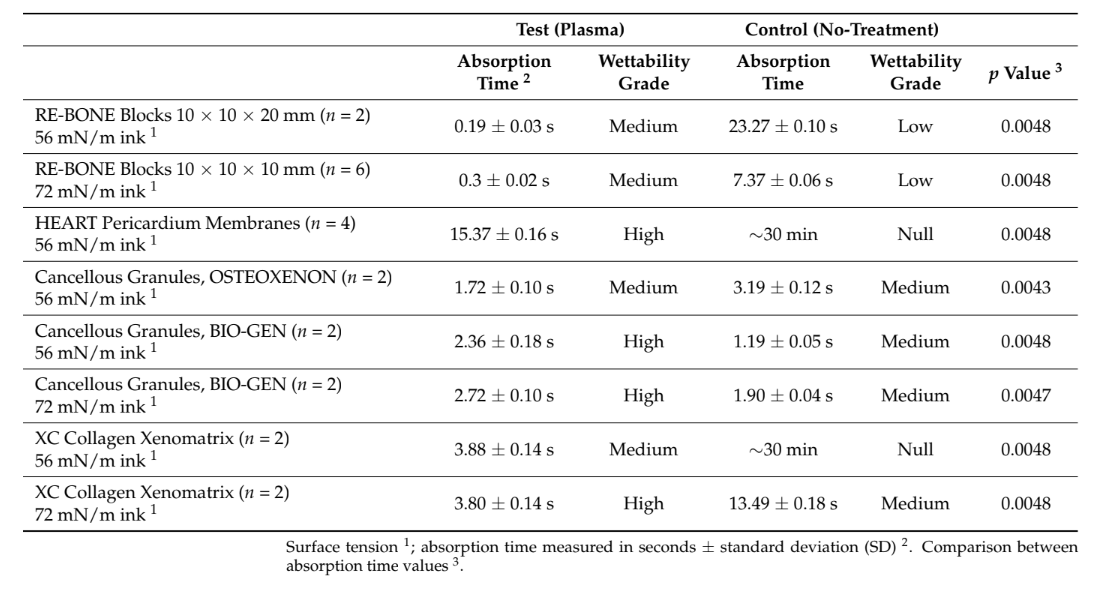
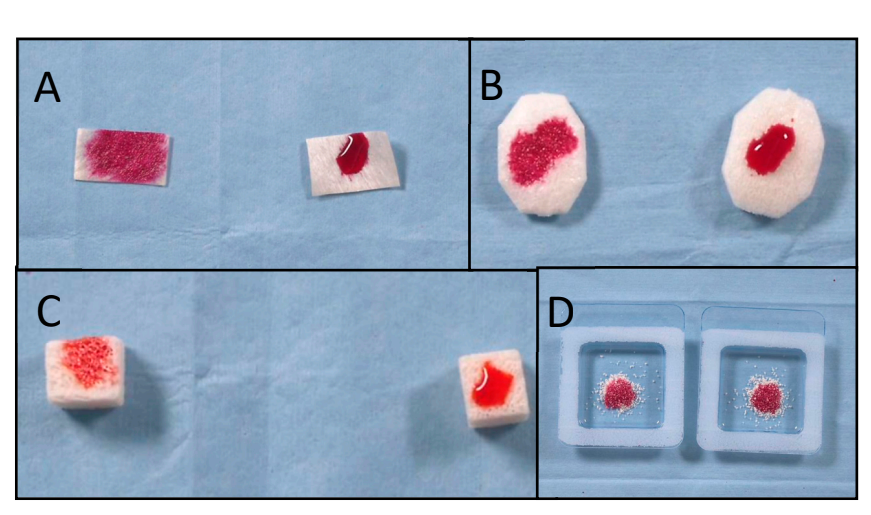
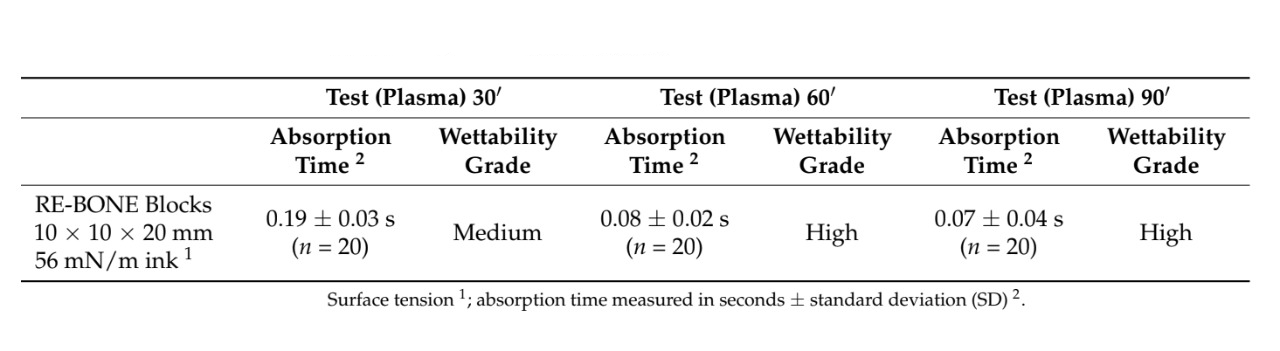
No total, 28 amostras foram utilizadas. O tempo de absorção e a molhabilidade de 22 amostras após a aplicação de várias tintas com diferentes tensões superficiais foram avaliados em ambos os grupos. O tratamento de superfície com plasma a vácuo reduziu estatisticamente o tempo de absorção em todas as amostras tratadas (p valor < 0,05, Tabela 1). Além disso, para todas as amostras, exceto para os grânulos de OSTEOXENON com tinta de 56 mN/m, a molhabilidade no grupo de teste foi de grau superior em comparação com o grupo controle. A maior diferença na molhabilidade foi encontrada para a membrana de pericárdio, com um grau alto no grupo de teste em comparação com um grau nulo no grupo controle. Os melhores resultados foram encontrados para o tratamento de superfície com plasma a vácuo dos blocos ósseos, membranas de colágeno, membranas de pericárdio e enxertos ósseos de colágeno, respectivamente. Todos os dados estão relatados na Tabela 1. Imagens explicativas estão relatadas na Figura 3.
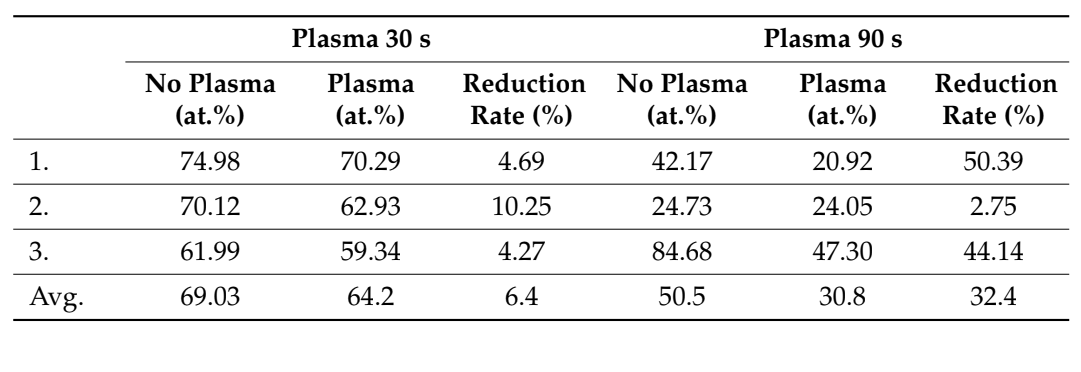
Seis blocos de osso (três após tratamentos de superfície com plasma a vácuo e três sem nenhum tratamento) foram avaliados na análise SEM-EDS após um, dois e três ciclos de tempo, respectivamente. A taxa de redução de impurezas de carbono tendia a aumentar após três ciclos de tempo em comparação com um e dois ciclos de tempo. Além disso, a análise SEM-EDS não mostrou danos aos biomateriais após múltiplos (até três vezes, 90 s, Figura 4) tratamentos de superfície com plasma a vácuo, enquanto o topo da superfície mostrou melhor molhabilidade após três ciclos de tempo (Figura 5). Todos esses dados estão relatados nas Tabelas 2 e 3.


Discussão
Este estudo teve como objetivo avaliar se o efeito do tratamento de superfície com plasma a vácuo em vários biomateriais utilizados para preservação de alvéolos e procedimentos de GBR poderia melhorar sua hidrofobicidade e molhabilidade. A hidrofobicidade foi medida através do tempo de absorção da tinta e do grau de molhabilidade. O tempo de absorção da tinta das amostras tratadas com plasma foi significativamente mais curto do que o das amostras não tratadas. Portanto, a hipótese nula de que não havia diferença foi parcialmente rejeitada. Esses testes iniciais in vitro indicaram que o tratamento de superfície com plasma a vácuo teve um efeito positivo nos blocos ósseos, membranas de pericárdio, matrizes de colágeno e enxertos ósseos de colágeno em termos de tempo de absorção e grau de molhabilidade. Por outro lado, o tratamento de superfície com plasma a vácuo não conseguiu reduzir o tempo de absorção para enxertos ósseos não colagenosos. Isso indica que o tratamento de superfície com plasma a vácuo converteu as superfícies dos biomateriais secos de hidrofóbicas para superfícies altamente hidrofílicas. No entanto, as características iniciais da superfície são importantes na definição dos resultados esperados.
O aumento do tempo total de tratamento, até três ciclos de tempo, melhorou os resultados. Uma possível explicação é que as impurezas de carbono tendem a diminuir após três ciclos de tempo. In vivo, o tratamento de superfície com plasma a vácuo de uma matriz dérmica acelular humana mostrou uma infiltração de fibroblastos aprimorada, indicando uma biocompatibilidade melhorada. Na pesquisa atual, o tratamento de superfície com plasma a vácuo exibiu alguns efeitos positivos em termos de descontaminação dos biomateriais tratados e em termos de ativação das superfícies, reduzindo as impurezas e aumentando sua hidrofobicidade.
Vários estudos na literatura confirmaram a eficácia dos tratamentos com plasma em termos de adesão celular e atividade de fibroblastos. No entanto, os principais tópicos desses estudos foram pilares dentários e superfícies de implantes.
A molhabilidade da superfície é um dos parâmetros mais importantes que afetam a resposta biológica a um material implantado, afetando a adsorção de proteínas, adesão/ativação de plaquetas, coagulação sanguínea e adesão de células e bactérias. Na pesquisa atual, tintas foram usadas para medir o tempo de absorção e o grau de molhabilidade dos biomateriais testados. A tensão superficial do sangue desempenha um papel importante no corpo humano. De acordo com Hrncír e Rosina, a tensão superficial do sangue, avaliada em um grupo de 71 sujeitos saudáveis usando o método de gota a uma temperatura de 22 graus Celsius, foi de 55,89 × 10(−3) N × m(−1), com um DP = 3,57 × 10(−3) N × m(−1). Considerando que mudanças no comportamento da tensão superficial de fluidos biológicos humanos são características em algumas doenças, para a pesquisa atual, foram utilizadas tintas com tensões superficiais de 56 mN/m e 72 mN/m.
Analisando os dados coletados na presente pesquisa, constatou-se que no grupo controle, a tinta com maior tensão superficial (72 mN/m) foi absorvida mais rapidamente do que a tinta com menor tensão superficial (56 mN/m) tanto pelos blocos de osso quanto pelas Xenomatrixes de colágeno, mas não pelos enxertos ósseos não colagenosos. Por outro lado, no grupo de teste, a diferença não foi relevante. Esses resultados podem significar que, após o tratamento de superfície com plasma a vácuo, as variações na tensão superficial poderiam ser menos relevantes para o processo de cicatrização.
Após até três ciclos de tempo, a imagem SEM da topografia da superfície não revelou alterações sob os tratamentos de superfície com plasma a vácuo, e nenhum dano físico foi observado. O aumento da hidrofobicidade, a redução no grau de impureza e a preservação da estrutura original, sem qualquer dano físico aos blocos de osso tratados com plasma, devem ser considerados como evidências da biocompatibilidade melhorada e potencial biointegração dos materiais testados.
O tratamento com plasma a vácuo é amplamente utilizado na medicina para melhorar a biocompatibilidade e biointegração em cirurgias reconstrutivas. Descobertas de uma pesquisa in vitro semelhante destacam o potencial do tratamento com plasma para melhorar o desempenho de hADMs em ambientes clínicos, oferecendo uma avenida promissora para melhorar os resultados de cirurgias reconstrutivas. Além disso, o tratamento com plasma a vácuo também é utilizado em outros campos, como para aumentar as propriedades elétricas de filmes de organossilicato ou a molhabilidade de polímeros de polieteretercetona (PEEK).
A principal limitação da pesquisa atual é o pequeno número de amostras e, claro, sua natureza in vitro. Outra limitação é que o ângulo de contato de molhabilidade deveria ter sido fornecido em vez do nível de grau de molhabilidade. Mesmo que os resultados da pesquisa atual sejam encorajadores para o tratamento de superfície com plasma a vácuo, os dados in vitro não nos permitem tirar conclusões clínicas definitivas. No entanto, a análise dos dados da análise SEM-EDS revelou que a taxa de impureza de carbono nas superfícies dos blocos ósseos tendia a diminuir ao aumentar o número de ciclos de tempo; portanto, aumentar os ciclos de tempo até três poderia ser sugerido dependendo dos substitutos de enxerto ósseo utilizados. Além disso, o tempo de absorção e o grau de molhabilidade também melhoraram após dois e três ciclos de tempo. Em relação a este último, membranas de pericárdio e enxertos ósseos, particularmente enxertos ósseos não colágenos, poderiam ser tratados aumentando o número de ciclos para dois ou três para reduzir o grau de impurezas de carbono e aumentar sua hidrofobicidade. No entanto, mais ensaios clínicos randomizados controlados são necessários para confirmar esses resultados preliminares. Outra limitação desta pesquisa é que, como não havia muitos estudos semelhantes na literatura científica, não foi fácil definir um critério para interpretar os resultados, especialmente em relação ao grau de molhabilidade dos substitutos de enxerto ósseo testados e membranas reabsorvíveis. Dados de estudos in vitro e in vivo semelhantes confirmaram o efeito positivo do tratamento com plasma em implantes e pilares ao usar plasma de argônio. Em relação a este último, os dados desta pesquisa in vitro devem ser considerados um relatório preliminar para encorajar mais avaliações clínicas.
Conclusões
O tratamento de superfície com plasma a vácuo aumentou estatisticamente a hidrofobicidade da maioria dos biomateriais testados, reduzindo o tempo de absorção e aumentando o grau de molhabilidade. Além disso, a taxa de impurezas de carbono poderia ser reduzida aumentando o tempo do ciclo. No entanto, mais estudos controlados randomizados com cálculos de tamanho de amostra são necessários para confirmar esses resultados preliminares.
Marco Tallarico, Silvio Mario Meloni, Michele Troia, Carlotta Cacciò, Aurea Immacolata Lumbau, Ieva Gendviliene, Francesco Mattia Ceruso e Milena Pisano
Referências
- Busenlechner, D.; Fürhauser, R.; Haas, R.; Watzek, G.; Mailath, G.; Pommer, B. Sucesso de implante a longo prazo na Academia de Implantologia Oral: acompanhamento de 8 anos e análise de fatores de risco. J. Periodontal Implant. Sci. 2014, 44, 102–108. [CrossRef] [PubMed]
- Kim, T.-I. Uma homenagem ao Dr. Per-Ingvar Brånemark. J. Periodontal Implant. Sci. 2014, 44, 265. [CrossRef] [PubMed]
- Mavrogenis, A.F.; Dimitriou, R.; Parvizi, J.; Babis, G.C. Biologia da Osseointegração do Implante. J. Musculoskelet. Neuronal Interact. 2009, 9, 61–71. [PubMed]
- Peñarrocha, D.M.; Cavani, U.; Cuadrado, L. Atlas de Carga Imediata de Implantes Dentários; Springer International Publishing: Berlim/Heidelberg, Alemanha, 2019; ISBN 9783030055462, 3030055469.
- Wong, M.; Eulenberger, J.; Schenk, R.; Hunziker, E. Efeito da topologia da superfície na osseointegração de materiais de implante em osso trabecular. J. Biomed. Mater. Res. 1995, 29, 1567–1575. [CrossRef]
- Wennerberg, A.; Albrektsson, T. Sobre superfícies de implante: Uma revisão do conhecimento e opiniões atuais. Int. J. Oral Maxillofac. Implant. 2010, 25, 63–74. [PubMed]
- Wennerberg, A.; Albrektsson, T. Efeitos da topografia da superfície de titânio na integração óssea: Uma revisão sistemática. Clin. Oral Implant. Res. 2009, 20, 172–184. [CrossRef]
- Beutner, R.; Michael, J.; Schwenzer, B.; Scharnweber, D. Nano-funcionalização biológica de superfícies de biomateriais à base de titânio: Uma caixa de ferramentas flexível. J. R. Soc. Interface 2010, 7, S93–S105. [CrossRef]
- Sun, X.D.; Liu, T.T.; Wang, Q.Q.; Zhang, J.; Cao, M.S. Modificação de Superfície e Funcionalidades para Implantes Dentários de Titânio. ACS Biomater. Sci. Eng. 2023, 9, 4442–4461. [CrossRef] [PubMed]
- Canullo, L.; Tallarico, M.; Peñarrocha, M.; Corrente, G.; Fiorellini, J.; Peñarrocha, D. Tratamento de Limpeza com Plasma de Argônio em Pilares de Implante em Pacientes Periodontalmente Saudáveis: Resultados de Seis Anos Pós-Carregamento de um Estudo Controlado Randomizado. Int. J. Periodontics Restor. Dent. 2017, 37, 683–690. [CrossRef]
- Canullo, L.; Tallarico, M.; Botticelli, D.; Alccayhuaman, K.A.A.; Neto, E.C.M.; Xavier, S.P. Mudanças em Tecidos Duros e Moles ao Redor de Implantes Ativados Usando Plasma de Argônio: Um Estudo Histomorfométrico em Cães. Clin. Oral Implant. Res. 2018, 29, 389–395. [CrossRef]
- Yang, H.J.; Lee, B.; Shin, C.; You, B.; Oh, H.S.; Lee, J.; Lee, J.; Oh, S.K.; Oh, S.H. Melhoria na Biocompatibilidade e Biointegração da Matriz Dérmica Acelular Humana através do Tratamento de Superfície com Plasma a Vácuo. Bioengineering 2024, 11, 359. [CrossRef] [PubMed]
- Kawai, H.; Shibata, Y.; Miyazaki, T. Pré-tratamento com Plasma de Descarga Brilhante Aumenta a Diferenciação e Sobrevivência de Osteoclastos em Placas de Titânio. Biomaterials 2004, 25, 1805–1811. [CrossRef]
- Shibata, Y.; Hosaka, M.; Kawai, H.; Miyazaki, T. Tratamento de Plasma de Descarga Brilhante de Placas de Titânio Aumenta a Adesão de Células Semelhantes a Osteoblastos às Placas através do Mecanismo Mediado por Integrinas. Int. J. Oral Maxillofac. Implant. 2002, 17, 771–777. [PubMed]
- Canullo, L.; Genova, T.; Mandracci, P.; Mussano, F.; Abundo, R.; Fiorellini, J.P. Mudanças Morfométricas Induzidas pelo Tratamento com Plasma Frio de Argônio em Osteoblastos Crescidos em Diferentes Superfícies de Implantes Dentários. Int. J. Periodontics Restor. Dent. 2017, 37, 541–548. [CrossRef] [PubMed]
- Noro, A.; Kaneko, M.; Murata, I.; Yoshinari, M. Influência da Topografia da Superfície e da Fisicoquímica da Superfície na Molhabilidade da Zircônia (Zircônia Tetragonal Policristalina). J. Biomed. Mater. Res. Biomater. 2013, 101, 355–363. [CrossRef]
- Canullo, L.; Tallarico, M.; Peñarrocha-Oltra, D.; Monje, A.; Wang, H.; Peñarrocha-Diago, M. Limpeza de Pilares de Implante com Plasma de Argônio: Acompanhamento de 5 Anos de um Estudo Controlado Randomizado. J. Periodontol. 2016, 87, 434–442. [CrossRef]
- Krithikadatta, J.; Gopikrishna, V.; Datta, M. Diretrizes CRIS (Checklist para Relatar Estudos In-vitro): Uma nota conceitual sobre a necessidade de diretrizes padronizadas para melhorar a qualidade e transparência na divulgação de estudos in-vitro em pesquisa dental experimental. J. Conserv. Dent. 2014, 17, 301–304. [CrossRef]
- Canullo, L.; Genova, T.; Chinigò, G.; Iacono, R.; Pesce, P.; Menini, M.; Mussano, F. Dispositivo de Tratamento com Plasma a Vácuo para Aumentar a Atividade de Fibroblastos em Superfícies de Titânio Usinadas e Rugosas. Dent. J. 2024, 12, 71. [CrossRef]
- Jeon, H.J.; Jung, A.; Kim, H.J.; Seo, J.S.; Kim, J.Y.; Yum, M.S.; Gweon, B.; Lim, Y. Aumento da Adesão e Proliferação de Osteoblastos na Superfície de Implante Tratada com Plasma a Vácuo. Appl. Sci. 2022, 12, 9884. [CrossRef]
- Pesce, P.; Menini, M.; Santori, G.; Giovanni, E.D.; Bagnasco, F.; Canullo, L. Ativação Foto e Plasma das Superfícies de Titânio de Implantes Dentários. Uma Revisão Sistemática com Meta-Análise de Estudos Pré-Clínicos. J. Clin. Med. 2020, 9, 2817. [CrossRef]
- Lee, H.; Jeon, H.J.; Jung, A.; Kim, J.; Kim, J.Y.; Lee, S.H.; Kim, H.; Yeom, M.S.; Choe, W.; Gweon, B.; et al. Melhoria da eficácia de osseointegração do implante de titânio através do tratamento de superfície com plasma. Biomed. Eng. Lett. 2022, 12, 421–432. [CrossRef] [PubMed]
- Fathi-Azarbayjani, A.; Jouyban, A. Tensão superficial na fisiopatologia humana e sua aplicação como uma ferramenta de diagnóstico médico. Bioimpacts 2015, 5, 29–44. [CrossRef] [PubMed]
- Hrncír, E.; Rosina, J. Tensão superficial do sangue. Physiol. Res. 1997, 46, 319–321. [PubMed]
- Baklanov, M.R.; Gismatulin, A.A.; Naumov, S.; Perevalov, T.V.; Gritsenko, V.A.; Vishnevskiy, A.S.; Rakhimova, T.V.; Vorotilov, K.A. Revisão Abrangente sobre o Impacto da Composição Química, Tratamento com Plasma e Irradiação Ultravioleta a Vácuo (VUV) nas Propriedades Elétricas de Filmes Organossilicatados. Polímeros 2024, 16, 2230. [CrossRef]
- Primc, G. Estratégias para Melhorar a Molhabilidade de Polímeros de Polieteretercetona (PEEK) por Tratamento com Plasma Não Equilíbrio. Polímeros 2022, 14, 5319. [CrossRef]
