Ácido hialurônico na extração dentária: uma revisão sistemática e meta-análise de ensaios pré-clínicos e clínicos
Tradução automática
O artigo original está escrito em EN language (link para lê-lo) .
Resumo
Objetivos Avaliar se em animais ou pacientes com ≥ 1 dente extraído, a aplicação de ácido hialurônico (HyA) resulta em cicatrização superior e/ou melhor manejo de complicações em comparação com qualquer outro tratamento ou sem tratamento.
Materiais e métodos Três bancos de dados foram pesquisados até abril de 2022. Os critérios de elegibilidade mais relevantes foram (1) aplicação local de HyA como adjunto à extração dentária ou como tratamento de osteíte alveolar, e (2) relato de dados clínicos, radiográficos, histológicos ou relatados pelo paciente. A formação de novo osso e/ou qualidade foram considerados principais parâmetros de resultado em estudos pré-clínicos, enquanto dor, inchaço e trismo foram definidos como principais parâmetros de resultado em estudos clínicos.
Resultados Cinco estudos pré-clínicos e 22 estudos clínicos (1062 pacientes na avaliação final) foram incluídos. Em ensaios pré-clínicos, HyA foi aplicado no alvéolo da extração. Embora um efeito positivo de HyA tenha sido observado em todos os estudos individuais sobre a formação óssea, esse efeito não foi confirmado pela meta-análise. Em estudos clínicos, HyA foi aplicado no alvéolo da extração ou utilizado como spray ou enxaguante bucal. A aplicação de HyA após a extração não cirúrgica de dentes normalmente erupcionados pode ter um efeito positivo na cicatrização dos tecidos moles. Com base em meta-análises, a aplicação de HyA após a remoção cirúrgica de terceiros molares inferiores (LM3) resultou em redução significativa na percepção da dor 7 dias após a cirurgia em comparação com a ausência de manipulação adicional da ferida ou a aplicação de um placebo/carreador. A dor pós-operatória precoce, o trismo e a extensão do inchaço não foram afetados.
ConclusõesA aplicação de HyA pode ter um efeito positivo na redução da dor após a remoção do LM3, mas não após a extração de dentes normalmente erupcionados.
Relevância clínicaA aplicação de HyA pode ter um efeito positivo na redução da dor após a remoção cirúrgica do LM3, mas não parece ter impacto em outras complicações ou após a extração de dentes normalmente erupcionados. Além disso, parece não reduzir a modelagem do rebordo alveolar pós-extração, embora estudos pré-clínicos mostrem formação óssea aumentada.
Introdução
Embora o processo de cicatrização após a extração dentária seja comumente sem complicações, qualquer dor subsequente pode comprometer o bem-estar dos pacientes, enquanto complicações também podem ocorrer. Por exemplo, a extração cirúrgica de terceiros molares semi-/totalmente impactados está regularmente associada a dor significativa, inchaço e trismo, que são agravados no caso do desenvolvimento de osteíte alveolar (OA)—também chamada de alvéolo seco. A OA é considerada uma das complicações mais frequentes da extração dentária, ocorrendo em 20 a 35% dos casos de extração cirúrgica de terceiros molares inferiores (LM3), e em 1,4 a 5% da extração (não cirúrgica) de dentes normalmente erupcionados. Além de tais complicações precoces, que afetam negativamente a qualidade de vida dos pacientes, a cicatrização comprometida do alvéolo de extração também pode levar a defeitos significativos de tecido duro, seja no local da extração ou nos dentes vizinhos. Por exemplo, foi relatado que defeitos periodontais profundos, por exemplo, profundidades de sondagem de bolsa ≥ 7 mm, na face distal do segundo molar ocorrem em quase um em cada quatro pacientes após a extração de LM3 impactados.
Para reduzir a morbidade dos pacientes e melhorar a cicatrização dos tecidos moles e duros das cavidades de extração, bem como para o tratamento de complicações precoces (por exemplo, AO), vários materiais e/ou técnicas cirúrgicas foram testados (por exemplo, aplicação de esponjas de colágeno, géis, derivados do sangue, vários materiais de enxerto). Uma atenção crescente tem sido dada recentemente ao ácido hialurônico (HyA), devido às suas propriedades anti-inflamatórias e antibacterianas e seus efeitos positivos na cicatrização dos tecidos moles e duros. Especificamente, estudos pré-clínicos demonstraram um efeito positivo, histologicamente, na cicatrização de defeitos ósseos e periodontais após a aplicação de HyA. Com base nos resultados das meta-análises de uma revisão sistemática de ensaios clínicos sobre a extração cirúrgica de terceiros molares, foi relatada uma redução significativa da dor no terceiro e sétimo dia pós-operatório, mas não no trismo, em grupos que receberam produtos à base de HyA. Nesse contexto, uma avaliação abrangente das evidências pré-clínicas e clínicas disponíveis sobre o efeito da aplicação de HyA em conexão com a extração dentária em geral, incluindo a prevalência, extensão e/ou manejo de complicações, está faltando. Portanto, a presente revisão sistemática abordou a seguinte questão PICOS (população (P), intervenção (I), comparação (C), resultados (O) e desenho do estudo (S)): “Em animais/pacientes com ≥ 1 dente extraído, a aplicação de HyA sozinha ou combinada com outros produtos/transportadores resulta em cicatrização superior dos tecidos moles/duros, redução da morbidade, redução da taxa de complicações e/ou melhora no manejo de complicações em comparação com qualquer outro tratamento ou nenhum tratamento?”.
Material e métodos
Protocolo do estudo e registro do estudo
O presente trabalho seguiu as diretrizes disponíveis para a realização de revisões sistemáticas de estudos pré-clínicos e clínicos (Itens Preferenciais para Revisões Sistemáticas e Meta-análise (PRISMA); Apêndice 1). Ambos os protocolos foram registrados no registro internacional prospectivo de revisões sistemáticas (PROSPERO), ou seja, um para o pré-clínico (CRD42021266190) e um para os ensaios clínicos (CRD42021266183).
Fontes de informação, busca na literatura e critérios de elegibilidade
A busca na literatura foi realizada em 3 bases de dados (ou seja, Ovid (MEDLINE e CENTRAL), EMBASE e Pubmed) em 14 de outubro de 2021, e atualizada em 7 de abril de 2022. Detalhes sobre a busca, incluindo as palavras-chave, estão apresentados no Apêndice 2. Após a remoção dos duplicados, títulos e resumos foram avaliados quanto à elegibilidade por 2 revisores (DD, TL) e os valores kappa para os textos completos avaliados e as publicações finalmente incluídas foram calculados. Qualquer ambiguidade foi resolvida em discussão com um terceiro autor (KB). Independentemente do tipo de estudo, foram incluídos estudos se (a) escritos em inglês ou alemão, (b) o texto completo estava disponível e (c) dados clínicos, radiográficos ou histológicos foram fornecidos. Critérios adicionais de inclusão para os estudos pré-clínicos foram (a) experimentos controlados randomizados e não randomizados, e (b) aplicação local de um produto à base de HyA sozinho ou em combinação com outro produto em ≥ 1 dos grupos após a extração de ≥ 1 dente. Critérios adicionais de inclusão para os estudos clínicos foram (a) ensaio controlado randomizado (RCT), ensaio controlado (CT) ou séries de casos com um mínimo de 10 pacientes, e (b) aplicação local de um produto à base de HyA sozinho ou em combinação com outro produto em ≥ 1 dos grupos, seja após a extração de ≥ 1 dente ou como tratamento de AO de ≥ 1 dente.
Coleta e extração de dados
Dois autores (DD, KB) extraíram os dados de forma independente duas vezes e qualquer desacordo foi resolvido em discussão com um terceiro autor (AS). Dos estudos pré-clínicos, as seguintes informações foram extraídas: (a) primeiro autor, (b) ano de publicação, (c) desenho do estudo, (d) modelo de tratamento, (e) local de tratamento, (f) espécie, (g) forma de aplicação de HyA, (h) grupos de tratamento, (i) período de acompanhamento, (j) parâmetros de resultado disponíveis e (k) detalhes de financiamento. Da mesma forma, as seguintes informações foram extraídas dos ensaios clínicos: (a) primeiro autor, (b) ano de publicação, (c) desenho do estudo, (d) características dos pacientes (ou seja, gênero, idade, estado de saúde e status de tabagismo), (e) critérios de inclusão específicos do local, (f) número de locais na linha de base e no último acompanhamento, (g) grupos de tratamento, (h) detalhes do produto, (i) forma de aplicação, (j) período de acompanhamento, (k) medicação pós-operatória, (l) parâmetros de resultado disponíveis, (m) ambiente clínico (ou seja, prática privada ou ambiente universitário) e (n) detalhes de financiamento. Finalmente, todas as informações disponíveis sobre os produtos à base de HyA foram resumidas, ou seja, (a) nome comercial, (b) fabricante, (c) concentração, (d) forma química e (e) forma de aplicação.
Avaliação do risco de viés
Para os ensaios pré-clínicos, a ferramenta de risco de viés (RoB) do SYRCLE foi utilizada. Conforme sugerido, os seguintes critérios foram avaliados como tendo “baixo”, “alto” ou “incerto” RoB: (1) geração de sequência, (2) características basais, (3) ocultação de alocação, (4) alojamento aleatório, (5) cegamento de cuidadores ou pesquisadores, (6) avaliação aleatória de resultados, (7) cegamento do avaliador de resultados, (8) dados de resultados incompletos, (9) relato seletivo de resultados e (10) outras fontes de viés. Para cada estudo, o número e a porcentagem de itens pontuados positivamente foram calculados (ou seja, “pontuação de qualidade”).
Para o RCT, a ferramenta RoB 2.0 da Colaboração Cochrane foi utilizada. O RoB foi considerado como tendo “baixo”, “alto” ou “algumas” preocupações para cada um dos seguintes critérios: (1) processo de randomização, (2) desvios das intervenções pretendidas, (3) dados de resultados ausentes, (4) medição do resultado, (5) seleção do resultado relatado e (6) risco geral de viés. Para os ensaios não randomizados, a ferramenta ROBINS-I foi utilizada. O risco de viés foi considerado como “baixo”, “moderado”, “sério”, “crítico” ou “sem informação” para os seguintes critérios: (1) confusão, (2) seleção de participantes, (3) classificação de intervenções, (4) desvios das intervenções pretendidas, (5) dados de resultados ausentes, (6) medição do resultado, (7) seleção do resultado relatado e (8) risco geral de viés.
A avaliação foi realizada por 2 revisores (DD, KB) e, em caso de qualquer ambiguidade, um consenso foi alcançado por meio de discussão com um terceiro autor (AS). Um autor repetiu a avaliação (DD).
Síntese dos resultados e análise estatística
Para os estudos pré-clínicos, a formação de novo osso e o volume ósseo por volume de tecido (BV/TV) foram considerados os principais parâmetros de resultado, enquanto para os estudos clínicos, dor, trismo e inchaço foram definidos como os principais parâmetros de resultado. Os dados foram extraídos do texto, tabelas e figuras, calculados e/ou os autores das publicações originais foram contatados.
Caso pelo menos 2 estudos randomizados com desenho de estudo comparável (ou seja, indicação de tratamento, regime de HyA, período de acompanhamento, avaliação de resultados) fossem identificados, uma meta-análise pareada foi realizada. As meta-análises foram limitadas a ECRs, incluindo assim estudos de maior qualidade metodológica. Os grupos que aplicavam HyA foram comparados a um grupo de controle negativo (ou seja, sem etapa de tratamento adicional) ou a um grupo de controle que aplicava outro tratamento, incluindo um placebo ou o material transportador do grupo de teste (“placebo/transportador”). Meta-análises pareadas foram realizadas para cada comparação separada, bem como de forma geral. A máxima verossimilhança restrita para calcular a heterogeneidade (τ2) foi utilizada e o ajuste do erro padrão de Knapp–Hartung foi aplicado para levar em conta o pequeno número de estudos. A diferença média entre o grupo controle e o grupo teste, o erro padrão da diferença média e o intervalo de confiança (IC) de 95% foram calculados. Em estudos utilizando o desenho de boca dividida, os dados foram tratados como dependentes ao calcular o erro padrão da diferença média, definindo r = 0,5. O teste qui-quadrado foi utilizado para avaliar a heterogeneidade, e um valor de p < 0,1 foi considerado indicativo de heterogeneidade significativa. Além disso, o teste I2 para homogeneidade foi realizado para quantificar a extensão da heterogeneidade e, em caso de pelo menos 3 estudos comparáveis, o intervalo de previsão de 95% foi adicionalmente calculado. A análise estatística foi realizada com STATA/IC 17.0 para Mac.
Qualidade da evidência (GRADE)
A certeza da evidência meta-analítica de ensaios pré-clínicos e clínicos incluídos neste documento foi resumida pela Avaliação, Desenvolvimento e Avaliação de Recomendações (GRADE). Para os ensaios pré-clínicos e clínicos, o software GRADEpro GDT (Ferramenta de Desenvolvimento de Diretrizes, Universidade McMaster e Evidence Prime, 2022) foi utilizado para classificar a qualidade da evidência dos resultados.
Resultados
Seleção e características do estudo
A busca na literatura é apresentada no Apêndice 3; 147 referências potenciais foram identificadas e, após a remoção dos duplicados, 90 estudos foram selecionados para triagem de título e resumo. Um total de 57 estudos foi removido por vários motivos, restando 33 estudos para análise do texto completo. Após a exclusão de mais 6 estudos em que o tipo de produto não atendia aos critérios de inclusão ou design de estudo incorreto, 5 estudos pré-clínicos e 22 estudos clínicos foram incluídos na presente revisão sistemática. Ambos os revisores concordaram perfeitamente sobre os estudos escolhidos para triagem do texto completo (kappa de Cohen = 1; 100% de concordância), enquanto uma concordância substancial foi alcançada para a inscrição final dos estudos (kappa de Cohen = 0,61; 84,9% de concordância).
Em todos os ensaios pré-clínicos, HyA foi aplicado na cavidade do dente após a extração de dentes que irromperam regularmente. Os ensaios clínicos foram divididos em 3 grupos de acordo com a indicação de tratamento: (1) remoção cirúrgica de LM3 (RCT (n = 10), CT (n = 1)), (2) extração de dentes que irromperam regularmente (RCT (n = 7), estudo de boca dividida não randomizado (n = 1), série de casos prospectiva (n = 1)), e (3) tratamento de AO (RCT (n = 1), série de casos prospectiva (n = 1)).
População do estudo
Quanto aos estudos pré-clínicos, 2 estudos incluíram 5–11 ratos Holtzman ou 5–6 ratos Wistar nos vários grupos, respectivamente, enquanto 3 estudos utilizaram cães beagle (20 cães no total). Nos estudos com ratos, HyA foi aplicado na cavidade de extração em animais saudáveis ou diabéticos, enquanto nos estudos com cães, HyA foi aplicado em cavidades de extração infectadas (Tabela 1).
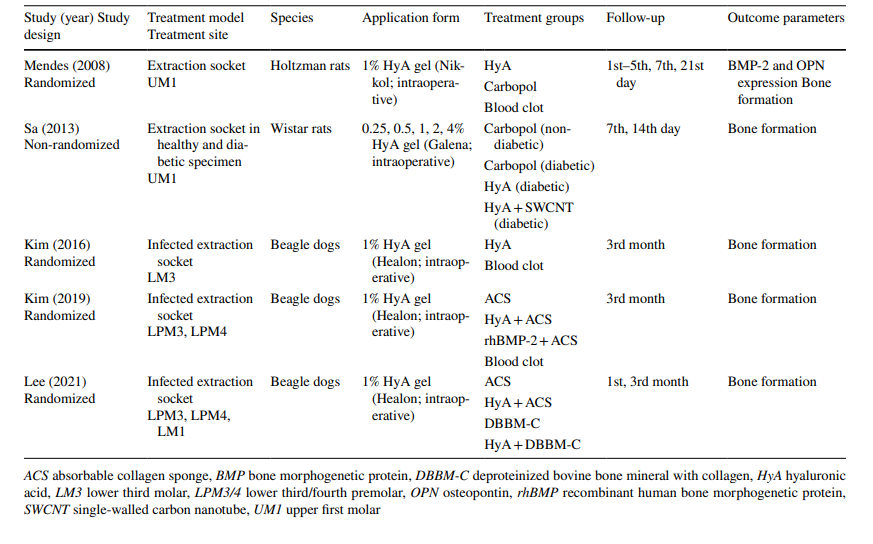
Os estudos clínicos sobre a remoção cirúrgica do LM3, extração de dentes que erupcionaram regularmente e tratamento de AO incluíram na avaliação final 603, 349 e 110 pacientes, respectivamente, contribuindo com 306, 226 e 90 locais tratados com HyA, e 370, 257 e 20 locais controle/não tratados com HyA, respectivamente (Tabela 2). Na maioria dos estudos, os pacientes eram sistemicamente saudáveis, enquanto um estudo cada um se referia a pacientes com doença hepática crônica ou diabéticos; 4 estudos não relataram sobre o estado de saúde dos pacientes. O estado de tabagismo foi relatado em 12 estudos; 8 estudos incluíram apenas não fumantes, 2 estudos incluíram pacientes fumando ≤ 10 cigarros/dia, e 2 estudos incluíram ambos, ou seja, não fumantes e fumantes. Dez estudos não forneceram nenhuma informação sobre o estado de tabagismo.
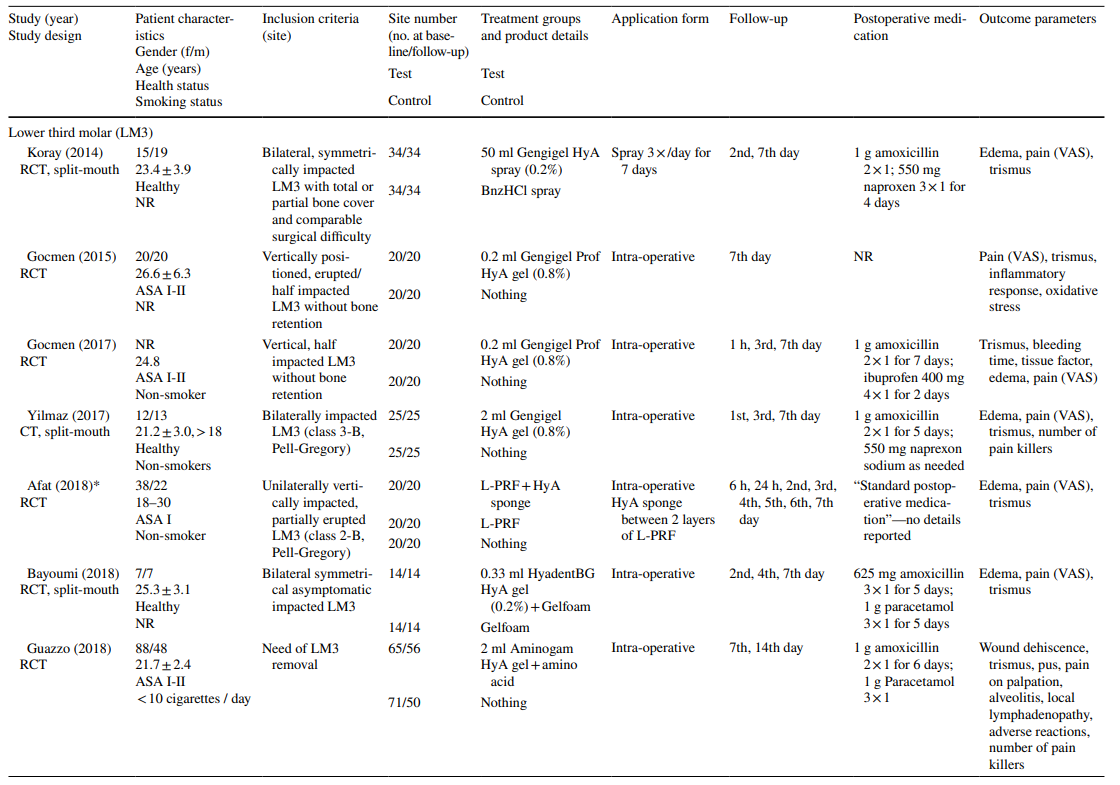
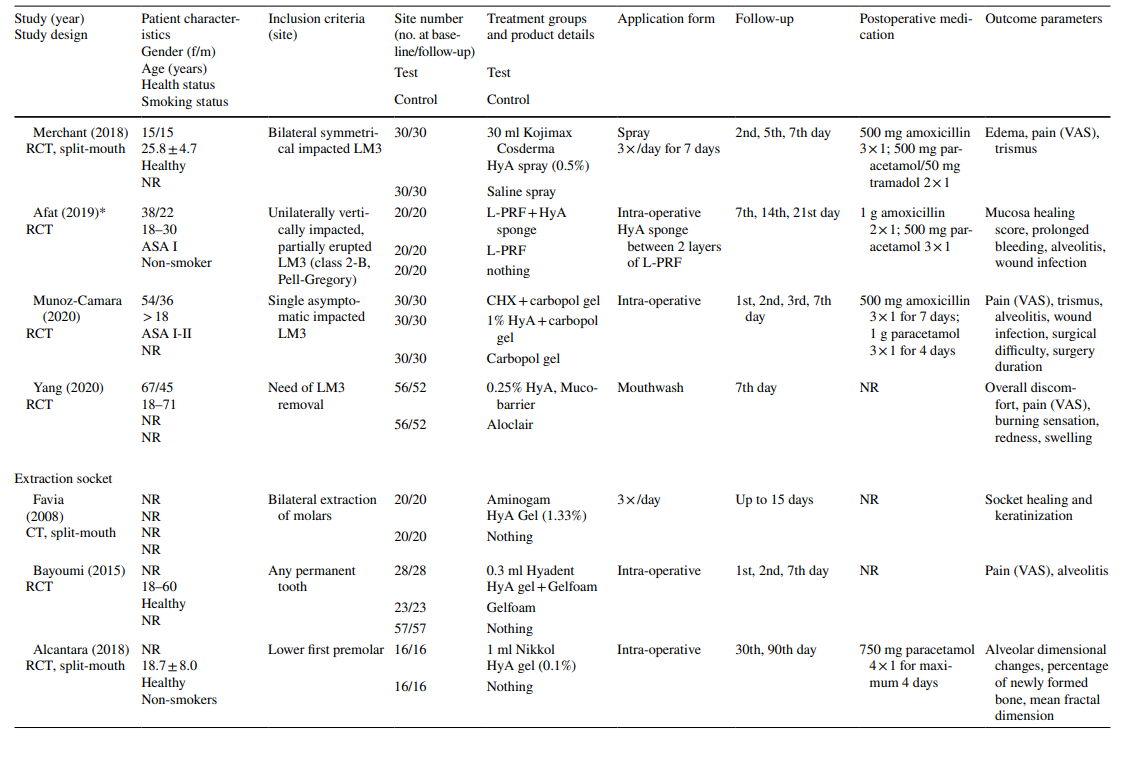
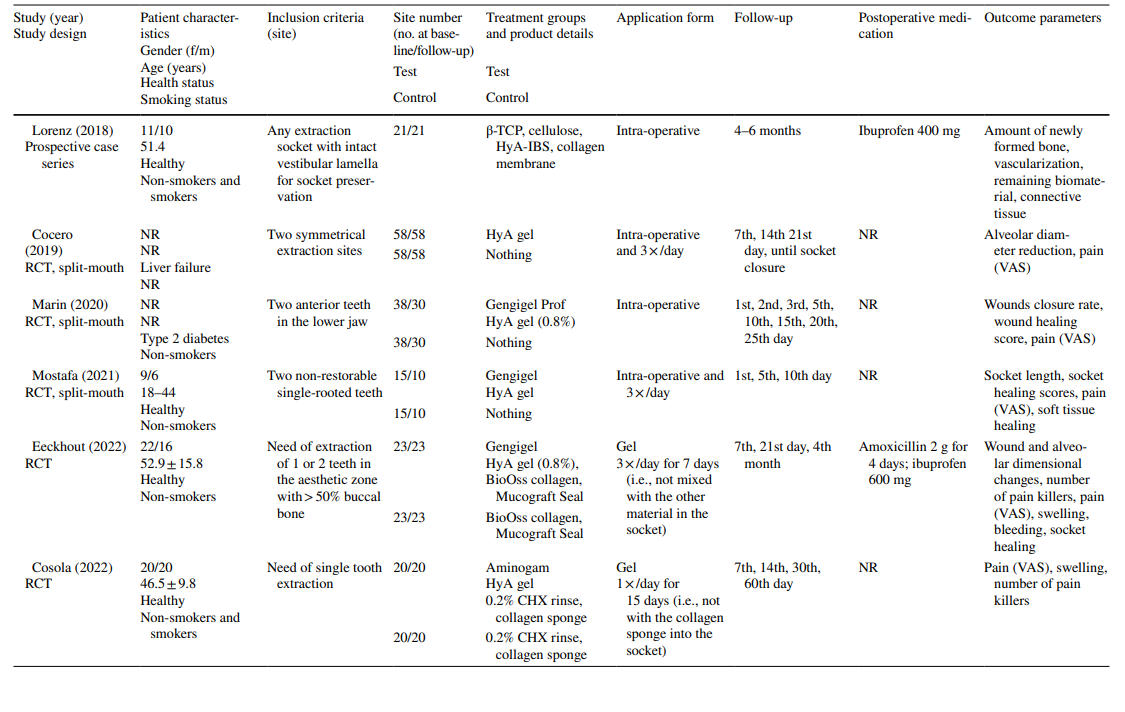
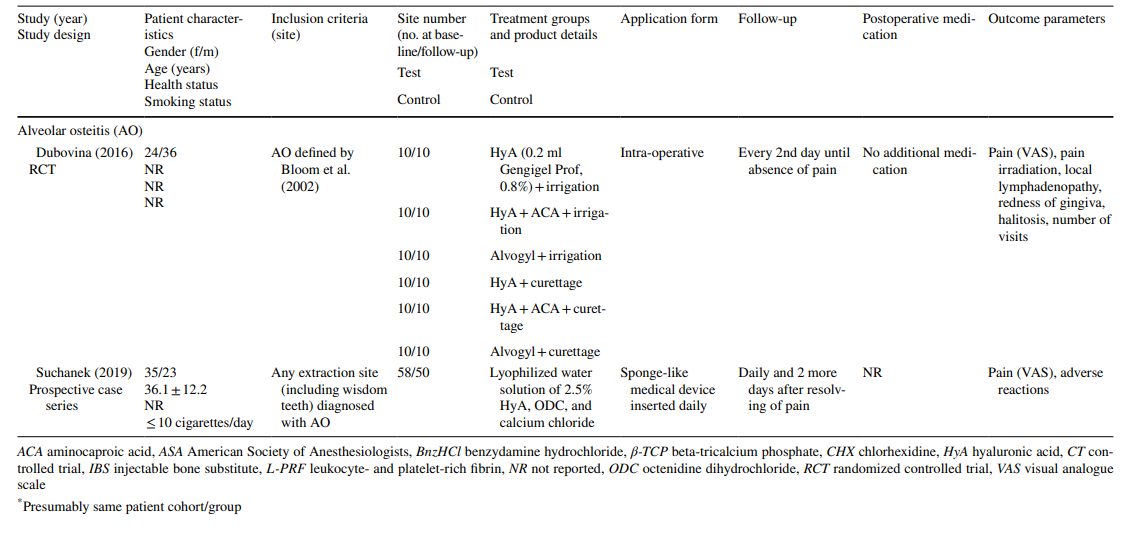
Nos estudos sobre a extração de LM3, os dentes eram assintomáticos, predominantemente impactados verticalmente ou meio impactados, permitindo o fechamento primário da ferida após a remoção cirúrgica. Metade dos estudos sobre a extração de dentes erupcionados regularmente incluía apenas dentes de raiz única (seja dentes anteriores ou pré-molares), enquanto a outra metade incluía molares ou qualquer tipo de dente. Ambos os estudos no grupo de tratamento de AO incluíram todos os tipos de dentes que atendiam aos critérios de AO de acordo com Blum et al. (2002).
Intervenção do estudo
Em todos os ensaios pré-clínicos, o HyA foi aplicado como um gel no alvéolo de extração logo após a remoção do dente, seja sozinho (n = 3) ou em combinação com uma esponja de colágeno absorvível (n = 2) (Tabela 1).
Na maioria dos estudos clínicos (n = 19) (Tabela 2), o HyA foi aplicado como um gel intraoperatoriamente no alvéolo de extração ou postoperatoriamente no local da extração, seja sozinho (n = 13) ou com algum transportador (ou seja, esponja de colágeno absorvível (n = 3), fibrina rica em leucócitos e plaquetas (n = 2) ou substitutos ósseos (n = 1)). Nos 3 estudos clínicos restantes, o HyA foi utilizado como spray 3 vezes ao dia durante 1 semana (n = 2) ou como enxaguante bucal (n = 1).
Informações sobre HyA
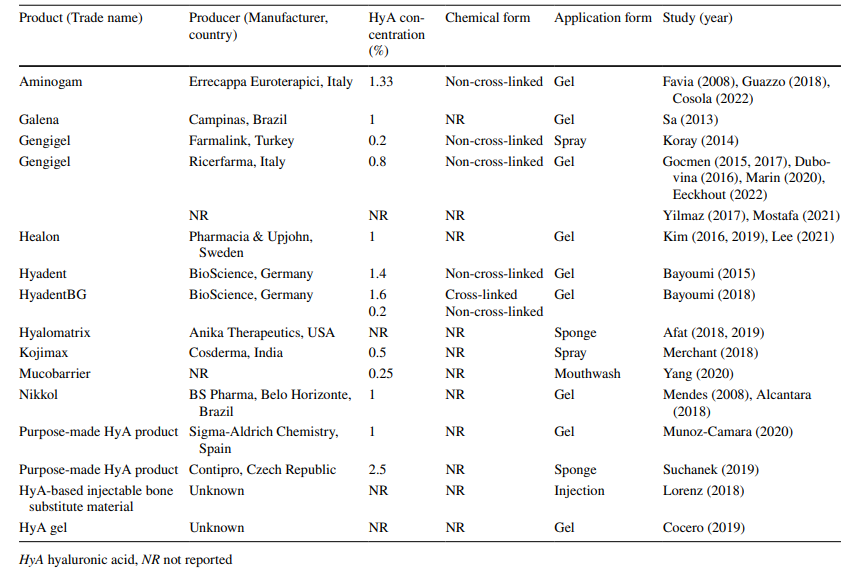
Nos 5 estudos pré-clínicos e 22 estudos clínicos incluídos, foram utilizados 11 produtos HyA comerciais, 2 feitos em casa e 2 de origem desconhecida (Tabela 3). Em todos os estudos pré-clínicos (n = 5), o HyA foi aplicado como um gel, enquanto nos estudos clínicos o HyA foi aplicado como gel (n = 15), spray (n = 2), enxaguante bucal (n = 1) ou combinado com uma esponja (n = 3) ou material de substituição óssea (n = 1) durante o processo de fabricação. A concentração de HyA variou de 0,2% em um spray, 0,25% em um enxaguante bucal, até 2,5% em uma esponja de HyA feita em casa, enquanto em 5 estudos a concentração de HyA não foi relatada. A forma química, ou seja, não reticulada ou reticulada, não foi relatada na maioria dos estudos (n = 16), enquanto 10 estudos utilizaram HyA não reticulada, e um estudo combinou HyA não reticulada e reticulada.
Configuração clínica e detalhes de financiamento
Todos os ensaios pré-clínicos foram financiados por subsídios de pesquisa independentes, únicos ou múltiplos.
Em um estudo clínico, foi relatado um desenho de estudo multicêntrico que incluiu 8 centros médicos, enquanto todos os outros estudos clínicos foram realizados em um único departamento em um ambiente universitário. Onze estudos clínicos não relataram fontes de financiamento, enquanto em 9 estudos clínicos o financiamento foi fornecido pelo departamento; no entanto, em 3 desses 9 estudos, o gel de HyA foi fornecido pelo fabricante. Em um único estudo, o financiamento foi fornecido por 3 diferentes fundações de pesquisa.
Variáveis de resultado relatadas e acompanhamento
Nos estudos pré-clínicos, a formação óssea foi avaliada por diferentes métodos entre 14 dias e 3 meses pós-operatórios. Um estudo investigou, além disso, o nível da proteína morfogenética óssea-2 e osteopontina (Tabela 1). Além disso, 4 estudos não registraram efeitos colaterais após a aplicação de HyA, enquanto um estudo não relatou ausências/presença de efeitos colaterais.
Nos estudos clínicos, os parâmetros de resultado avaliados variaram dependendo da indicação do tratamento (Tabela 2). Nos estudos sobre a remoção cirúrgica do LM3, a presença de dor medida pela escala analógica visual (EAV), inchaço e trismo foram os parâmetros de resultado mais frequentemente avaliados. Outros parâmetros avaliados com menos frequência foram a presença/ausência de sangramento prolongado, presença/ausência de deiscência de tecido mole, velocidade de cicatrização da mucosa, taxa de infecção de AO/ferida e marcadores laboratoriais de inflamação, estresse oxidativo e cicatrização de feridas. Entre os estudos sobre a extração de dentes erupcionados regularmente, 3 publicações utilizaram diferentes pontuações de cicatrização de alvéolo/tecido mole, 3 publicações avaliaram a quantidade de osso recém-formado e/ou mudanças dimensionais alveolares, 3 publicações avaliaram a dor, e um estudo avaliou a taxa de AO. Ambos os estudos sobre o tratamento de AO focaram na avaliação da dor e reações adversas. A maioria dos estudos clínicos não registrou efeitos colaterais após a aplicação local de HyA, enquanto 6 estudos não mencionaram a ausência/presença de efeitos colaterais. Um único estudo aplicando gel de HyA a 0,8% após a remoção do LM3 relatou um tempo de sangramento significativamente prolongado após o fechamento da ferida em comparação com o grupo controle; no entanto, como a hemostasia ocorreu dentro de um intervalo fisiológico, isso não foi considerado um evento adverso.
Resumo dos resultados dos estudos individuais
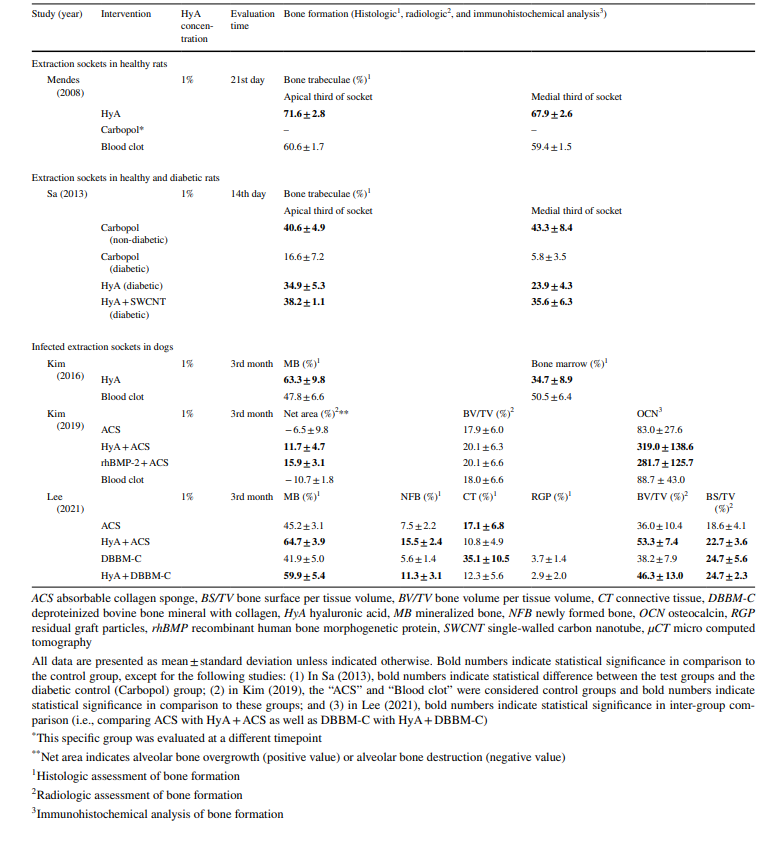
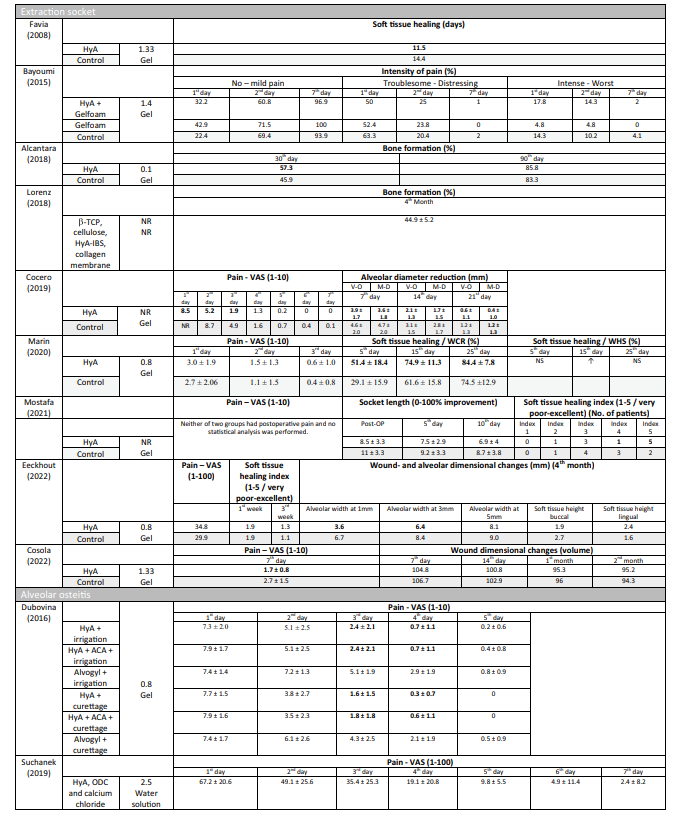
Em todos os estudos pré-clínicos (Tabela 4), com base em análise histológica, radiológica ou imuno-histoquímica, os grupos de teste com HyA mostraram resultados significativamente melhores em comparação ao grupo controle em pelo menos um dos parâmetros relacionados à formação óssea; isso foi independente da condição do alvéolo (saudável ou infectado) e do tipo de tratamento controle.
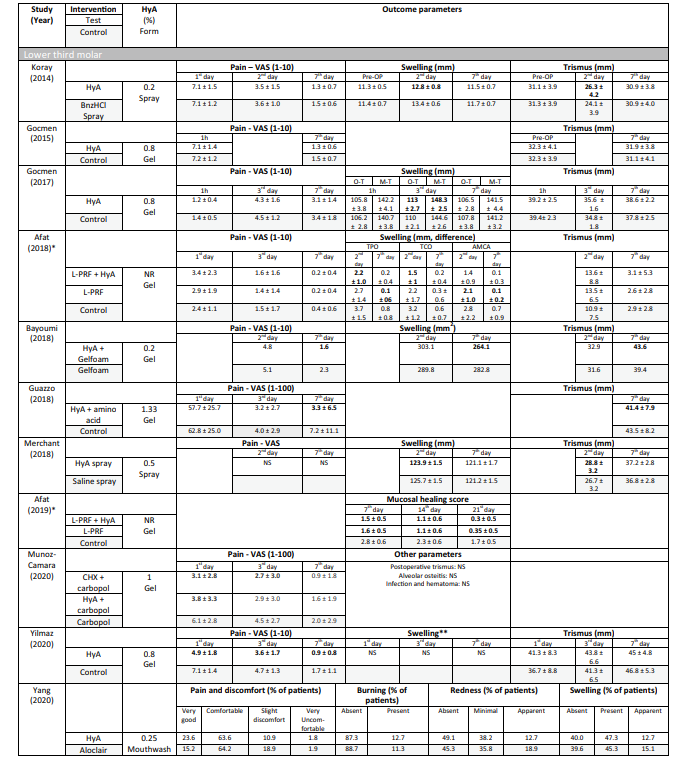
Em 4 de 10 estudos clínicos sobre a remoção cirúrgica do LM3 (Tabela 5) que relataram sobre dor, foram relatadas vantagens significativas para o grupo de teste usando HyA, em comparação com o grupo controle, em pelo menos um ponto de tempo pós-operatório. Da mesma forma, em 4 de 7 estudos e em 3 de 9 estudos que relataram sobre inchaço e trismo, respectivamente, foram relatadas vantagens significativas a favor da aplicação de HyA em comparação com o grupo controle. Em 3 de 4 estudos que relataram sobre a cicatrização de tecidos moles após a extração de dentes que erupcionaram regularmente, foi registrada uma cicatrização de tecidos moles significativamente melhor após a aplicação de HyA em comparação com o grupo controle. Além disso, um estudo relatou formação óssea melhorada após 30 dias, um estudo relatou uma redução diminuída do diâmetro alveolar após até 21 dias, enquanto 2 estudos relataram nenhuma diferença entre os grupos ou desvantagens significativas para o grupo de teste usando HyA em termos de mudanças dimensionais alveolares. Finalmente, a percepção da dor foi relatada em 6 estudos, mas apenas 2 estudos relataram diferenças significativas entre os grupos a favor da aplicação de HyA. Um estudo avaliando o tratamento de AO relatou dor pós-operatória significativamente menor após a aplicação de HyA em comparação com a aplicação de alvogyl; o segundo estudo não tinha grupo controle.

Síntese dos resultados
Estudos pré-clínicos—volume ósseo por volume de tecido em ensaios pré-clínicos
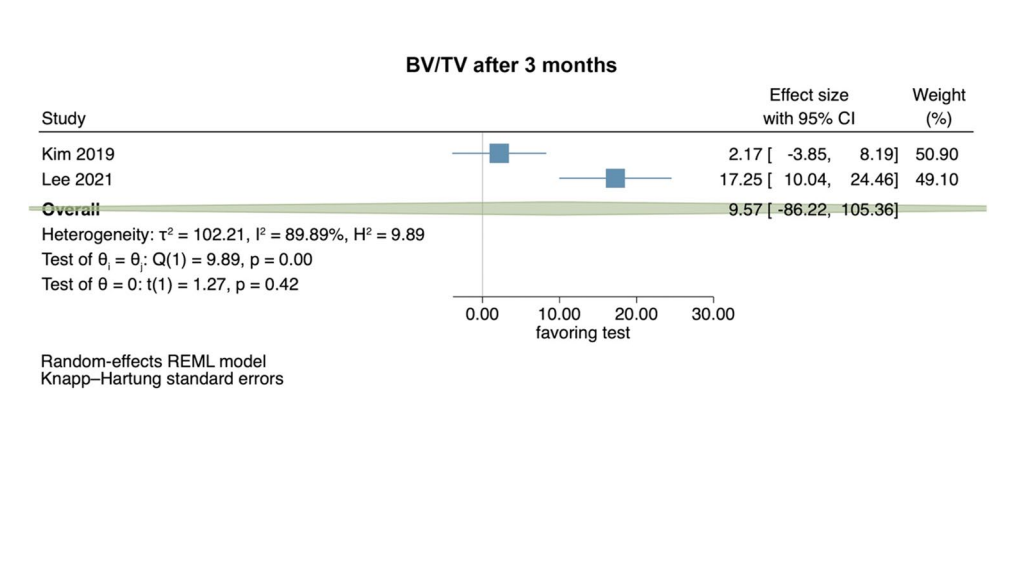
Dois estudos pré-clínicos forneceram dados para resumir o BV/TV avaliado radiograficamente 3 meses após a operação (Fig. 1). Os estudos compararam a aplicação de HyA em combinação com uma esponja de colágeno absorvível versus a esponja de colágeno absorvível. No geral, nenhuma diferença significativa entre os grupos foi identificada (tamanho do efeito: 9.57; 95% CI: − 86.22 a 105.36; p = 0.42), mas a heterogeneidade estatística entre os estudos foi significativa (I2 = 89.89%; p < 0.01).
Estudos clínicos—avaliação da dor 2–3 e 7 dias após a remoção cirúrgica do LM3
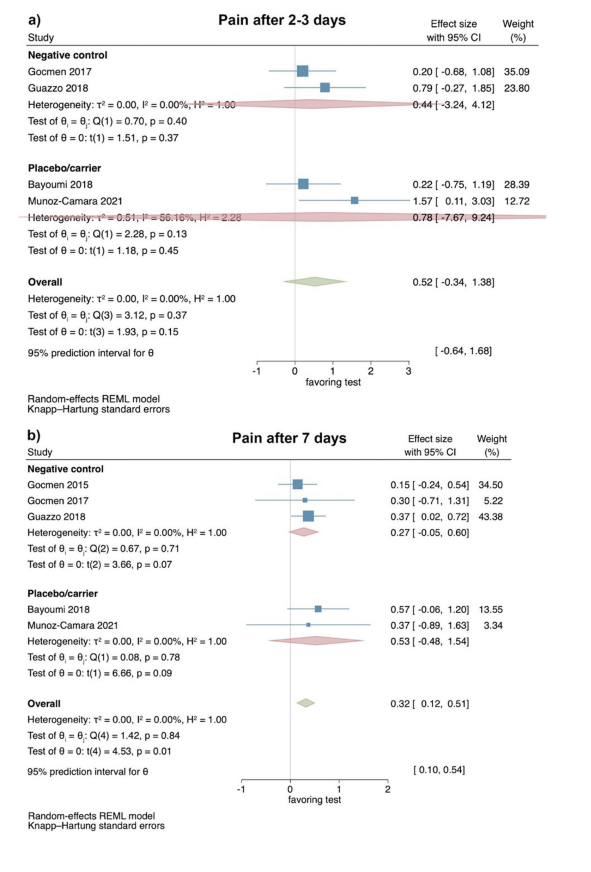
Com base nos resultados de 4 ECRs, a percepção da dor não mostrou diferenças estatisticamente significativas entre os grupos teste e controle 2–3 dias após a cirurgia (tamanho do efeito: 0.52; IC 95%: − 0.34–1.38; p = 0.15), sem heterogeneidade estatística entre os estudos (I2 = 0.00%; p = 0.37). Análises separadas com 2 estudos cada um comparando HyA com um grupo de controle negativo (tamanho do efeito: 0.44; IC 95%: − 3.24–4.12; p = 0.37) e HyA com um grupo placebo/carreador (tamanho do efeito: 0.78; IC 95%: − 7.67–9.24; p = 0.45) também não apresentaram significância estatística (Fig. 2a).
Com base nos resultados de 5 ECRs, a percepção da dor 7 dias após a cirurgia foi significativamente menor nos grupos teste que aplicaram HyA (tamanho do efeito: 0.32; IC 95%: 0.12–0.51; p = 0.01), sem heterogeneidade estatística entre os estudos (I2 = 0.00%; p = 0.84). No entanto, as análises separadas não apresentaram significância estatística para a comparação HyA com um grupo de controle negativo (3 estudos; tamanho do efeito: 0.27; IC 95%: − 0.05–0.60; p = 0.07) e para a comparação HyA com um grupo placebo/carreador (2 estudos; tamanho do efeito: 0.53; IC 95%: − 0.48–1.54; p = 0.09; Fig. 2b).
Estudos clínicos—avaliação do inchaço 2–3 e 7 dias após a remoção cirúrgica do LM3
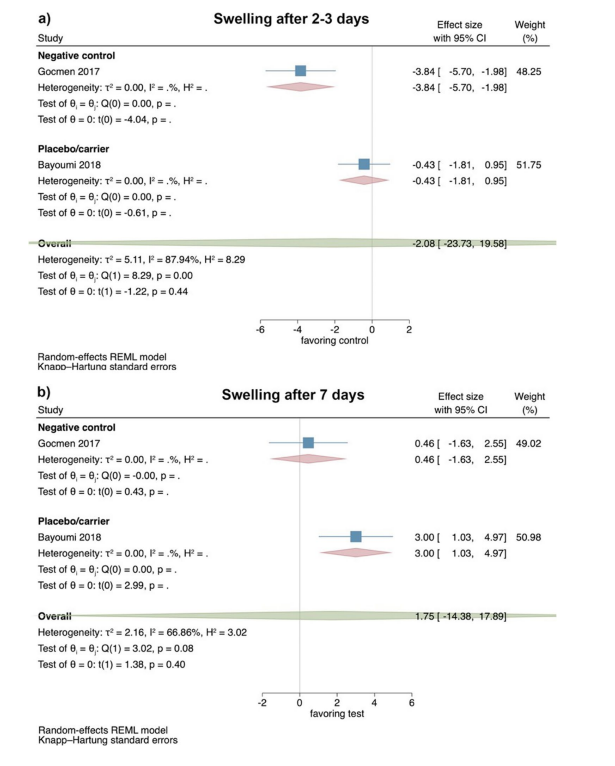
Com base nos resultados de 2 ECR, a extensão do inchaço 2–3 dias no pós-operatório não mostrou diferença significativa entre os grupos teste e controle (tamanho do efeito: − 2.08; 95% CI: − 23.73–19.58; p = 0.44); no entanto, a heterogeneidade estatística entre os estudos foi significativa (I2 = 87.94%; p < 0.01; Fig. 3a).
Da mesma forma, a extensão do inchaço 7 dias após a cirurgia também não mostrou diferença significativa entre os grupos de teste e controle (tamanho do efeito: 1,75; IC 95%: − 14,38–17,89; p = 0,40), e a heterogeneidade estatística entre os estudos foi novamente significativa (I2 = 66,86%; p = 0,08; Fig. 3b). Não foi possível realizar uma análise separada para a comparação de HyA com qualquer controle negativo ou grupo placebo/carreador devido ao número limitado de estudos.
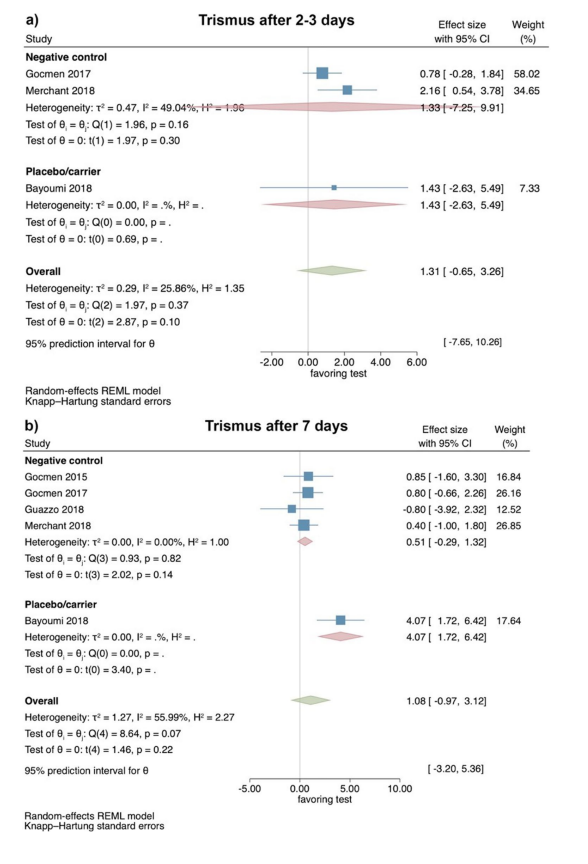
Estudos clínicos—avaliação do trismo 2–3 e 7 dias após a remoção cirúrgica do LM3
Com base nos resultados de 3 ECRs, o trismo não apresentou diferenças significativas entre os grupos de teste e controle 2–3 dias pós-operatórios (tamanho do efeito: 1.31; IC 95%: − 0.65–3.26; p = 0.10), sem heterogeneidade estatística entre os estudos (I2 = 25.86%; p = 0.37). As análises separadas também não mostraram significância estatística para a comparação de HyA com um grupo controle negativo (2 estudos; tamanho do efeito: 1.33; IC 95%: − 7.25–9.91; p = 0.30), enquanto apenas um único estudo estava disponível para a comparação de HyA com um grupo placebo/carreador (Fig. 4a).
Com base nos resultados de 5 ECRs, o trismo não apresentou diferença significativa entre os grupos de teste e controle 7 dias pós-operatórios (tamanho do efeito: 1.08; IC 95%: − 0.97–3.12; p = 0.22); no entanto, a heterogeneidade estatística entre os estudos foi significativa (I2 = 55.99%; p = 0.07). As análises separadas também não mostraram diferença significativa entre HyA e um grupo controle negativo (4 estudos; tamanho do efeito: 0.51; IC 95%: − 0.29–1.32; p = 0.14), enquanto apenas um único estudo estava disponível para a comparação de HyA com um grupo placebo/carreador (Fig. 4b).
Avaliação do risco de viés
Entre os estudos pré-clínicos, a pontuação de qualidade variou entre 20 e 40% (Apêndice 4); apenas o relato das características basais e outras fontes de viés foram julgados em todos os estudos como baixo risco de viés.
Os RCT incluídos foram considerados como tendo algumas preocupações (n = 13) ou baixo risco de viés (n = 5) (Apêndice 5). Nenhum dos RCT desviou da intervenção pretendida, 5 RCTs foram considerados como tendo algumas preocupações no processo de randomização, e aproximadamente metade dos estudos foi considerada como tendo algumas preocupações em sua reportagem sobre dados de desfecho ausentes, medição do desfecho e seleção dos resultados reportados. A maioria dos estudos não randomizados foi considerada como tendo baixo risco de viés (n = 3), enquanto um estudo foi considerado como tendo algumas preocupações (Apêndice 6).
Qualidade da evidência (GRADE)
Para os resultados da meta-análise incluindo 2 ensaios pré-clínicos, a certeza da evidência para o parâmetro de desfecho BV/TV após 3 meses foi classificada como baixa (Apêndice 8a).
A certeza da evidência obtida a partir de meta-análises incluindo ensaios clínicos foi considerada como moderada para percepção de dor e trismo e como baixa para a avaliação de inchaço (Apêndice 8b).
Discussão
O HyA demonstrou possuir propriedades anti-inflamatórias, antiedematosas, osteoindutivas e proangiogênicas; assim, parece que o HyA melhora a cicatrização de feridas.
A presente revisão sistemática teve como objetivo fornecer uma avaliação abrangente de todas as evidências disponíveis (ou seja, pré-clínicas e clínicas) sobre o efeito da aplicação de HyA em conexão com a extração dental. No geral, parece que a aplicação de HyA em conexão com a remoção cirúrgica do LM3 pode ter um efeito positivo na redução da dor durante a primeira semana pós-operatória. Especificamente, a meta-análise de 5 estudos clínicos mostrou que a aplicação local (intra-cirúrgica) do gel de HyA estava associada a uma percepção de dor estatisticamente significativamente reduzida 7 dias após a cirurgia em comparação com o grupo controle, que não teve manipulação adicional da ferida ou a aplicação de um placebo/carreador. A aplicação de HyA não parece ter impacto em outras complicações que frequentemente aparecem após a remoção do LM3 (ou seja, inchaço e trismo) ou em conexão com a extração não cirúrgica de dentes normalmente erupcionados.
Este efeito positivo da aplicação intra-cirúrgica de HyA na percepção da dor dentro da primeira semana pós-operatória da remoção do LM3 complementa os resultados de uma revisão sistemática anterior, que também avaliou o possível benefício da HyA na mesma indicação. Especificamente, com base em uma seleção de estudos diferente, a aplicação de HyA reduziu significativamente a dor tanto no 3º quanto no 7º dia pós-operatório. Aparentemente, o efeito positivo da HyA nos primeiros dias pós-operatórios observado naquela revisão não foi visto na presente meta-análise, devido ao aumento das informações fornecidas por 2 estudos adicionais incluídos aqui e devido à exclusão de um estudo não randomizado, que favoreceu fortemente o grupo de teste da HyA. Um efeito positivo da HyA em termos de redução da percepção da dor pode ser parcialmente explicado pelo seu efeito modulador na resposta inflamatória no local cirúrgico. Foi demonstrado anteriormente que a HyA pode regular negativamente a produção e expressão de prostaglandina E2, bradicinina e substância P, que estão todas envolvidas na transmissão e sensação da dor. No entanto, qualquer potencial efeito positivo da HyA na resposta inflamatória local não se traduz necessariamente em menos inchaço e/ou trismo na clínica, uma vez que tanto as análises incluídas aqui quanto as da revisão mencionada acima não indicaram diferenças entre os grupos de teste e controle em relação a esses aspectos. No entanto, esses resultados devem ser interpretados com cautela devido ao pequeno número de estudos originais e à falta de padronização nos métodos de avaliação do inchaço facial, bem como na intervenção em si. Por exemplo, os estudos incluídos raramente forneceram informações sobre o nível de dificuldade cirúrgica e/ou o design do retalho aplicado, aspectos que podem afetar os parâmetros de resultado. Além disso, a falta de qualquer efeito positivo significativo da HyA na percepção da dor na extração não cirúrgica de dentes erupcionados regularmente, observada na maioria dos estudos (4 em 5) incluídos nesta revisão, não deve ser interpretada como falta de ação da HyA em si. Isso pode ser devido a diferenças no modo de cicatrização, ou seja, “fechado” após a remoção cirúrgica do LM3 versus “aberto” após a extração de dentes erupcionados regularmente, onde a falta de fechamento primário e de qualquer transportador pode ter resultado em uma rápida eliminação da HyA. Se a aplicação de HyA em um transportador poderia melhorar sua ação, é difícil de avaliar, uma vez que isso foi utilizado apenas em um único estudo que não conseguiu mostrar diferenças. No entanto, também deve-se ter em mente que, na maioria dos casos, a extração dentária não complicada está associada a baixos níveis de dor, e assim, qualquer possível efeito positivo da HyA pode ser difícil de capturar. De fato, no único estudo comparativo sobre o manejo de AO incluído nesta revisão, foi relatada uma redução significativa da dor pós-operatória nos grupos que receberam HyA (sem fechamento primário e sem uso de um transportador).
Alguns dos estudos sobre a cicatrização após a extração de dentes que erupcionaram regularmente, incluídos nesta revisão, também avaliaram o possível impacto da aplicação de HyA na cicatrização de tecidos moles e duros. Em 3 dos 4 estudos que avaliaram a cicatrização de tecidos moles, um efeito positivo do HyA foi relatado com base no tempo até e/ou na porcentagem de fechamento do alvéolo, bem como com base nas pontuações para julgar a cicatrização de tecidos moles. Em contraste, em 3 estudos comparativos, o uso intra ou pós-operatório de gel de HyA não teve nenhum efeito positivo em termos de mudanças dimensionais alveolares em comparação com a não aplicação de HyA, após um período de acompanhamento de 3 a 4 meses. De fato, em um dos estudos, onde após a preservação da crista com enxerto de alvéolo com mineral ósseo bovino desproteinizado enriquecido com colágeno e selagem do alvéolo por meio de uma matriz de colágeno em terapia cirúrgica, o gel de HyA foi aplicado na matriz de colágeno três vezes ao dia durante 1 semana, foi observada uma perda óssea horizontal significativamente maior na face coronal dos alvéolos de extração. Essas descobertas sobre a falta de um efeito positivo do HyA no osso podem parecer de alguma forma em contraste com os achados relatados nos estudos pré-clínicos incluídos aqui. Nos 2 estudos que relataram sobre a cicatrização de alvéolos de extração não infectados em ratos saudáveis ou diabéticos, a aplicação de HyA melhorou significativamente a cicatrização óssea em comparação com o grupo controle. Da mesma forma, em 3 dos 3 estudos com cães que relataram sobre a cicatrização de alvéolos de extração infectados, a aplicação de HyA, sozinha ou com uma esponja de colágeno ou mineral ósseo bovino desproteinizado com colágeno como transportador, melhorou a cicatrização óssea. É importante mencionar, no entanto, que esse efeito positivo do HyA na cicatrização óssea não foi demonstrado na única meta-análise possível aqui em relação ao BV/TV, provavelmente devido ao fato de que ambos os estudos usaram um tempo de cicatrização tardio para este modelo animal particular; ou seja, a cicatrização óssea dentro de um alvéolo de extração no cão está bastante avançada após 3 meses, mesmo sem qualquer tratamento. Vale ressaltar que o BV/TV no grupo HyA foi semelhante ao de outro grupo de teste, tratado com proteína morfogenética óssea humana recombinante-2 (rhBMP-2), um conhecido agente muito potente de aumento ósseo. Além disso, tais efeitos positivos do HyA na cicatrização óssea também foram demonstrados em outros estudos pré-clínicos, utilizando modelos de defeito de tamanho crítico. Em perspectiva, nenhum estudo sobre a remoção cirúrgica do LM3 avaliou o resultado da cicatrização na face distal do segundo molar inferior, um local que muitas vezes está associado a um defeito periodontal profundo após a extração do LM3 impactado.
Esta revisão também tentou identificar se a aplicação de HyA pode reduzir a taxa de AO após a extração dentária; no entanto, houve um relato limitado sobre essa complicação nos estudos. Nesse contexto, a aplicação de HyA é geralmente considerada segura e sem efeitos colaterais; no entanto, deve-se mencionar que a HyA pode levar a eventos adversos significativos caso seja aplicada (injetada) nos tecidos. Neste caso, apenas um único estudo relatou um tempo de sangramento prolongado após o fechamento da ferida em comparação com o grupo controle; no entanto, a hemostasia foi considerada dentro de um intervalo fisiológico e, portanto, não foi considerada um evento adverso. Todos os outros estudos incluídos nesta revisão não mencionaram quaisquer efeitos colaterais ou complicações após a aplicação de HyA. Além do fato de que a HyA é segura para aplicação em conexão com extrações dentárias cirúrgicas LM3 ou não cirúrgicas, não podem ser feitas conclusões sobre a formulação de HyA mais eficiente (por exemplo, baixa vs. alta concentração, não reticulada vs. reticulada, gel vs. spray) ou modo de aplicação (por exemplo, com vs. sem um transportador, frequência), e assim, nenhuma recomendação clara pode ser fornecida.
No total, apenas um número limitado de ensaios pré-clínicos e clínicos bem projetados e randomizados pôde ser identificado aqui e combinado em uma meta-análise. Além disso, como mencionado acima, há uma falta de consenso e informações sobre os detalhes dos produtos de HyA, mas também sobre os detalhes cirúrgicos (por exemplo, nível de dificuldade cirúrgica ou design do retalho). Essas limitações resultaram em uma certeza geral de evidência baixa a moderada. Em estudos futuros, uma melhor e mais padronizada apresentação dos detalhes dos produtos de HyA, dosagens e aplicações, e tempos de acompanhamento mais longos devem ser implementados para permitir uma avaliação mais completa do potencial do uso de HyA em conexão com a extração dentária. Além disso, futuras revisões sistemáticas atualizadas, incluindo um número maior de estudos, também devem considerar nas meta-análises uma comparação entre estudos com braços paralelos e estudos em design de boca dividida. Isso seria especificamente de interesse para parâmetros como percepção da dor, algo não viável aqui devido ao número muito limitado de estudos de boca dividida.
Conclusão
Os resultados da presente revisão sistemática e meta-análises mostraram que a aplicação intra-cirúrgica de HyA em conexão com a remoção cirúrgica do LM3 resultou em uma redução significativa na percepção da dor 7 dias após a cirurgia, enquanto a dor pós-operatória precoce, trismo e a extensão do inchaço não foram afetados. Além disso, parece que a aplicação de HyA pode ter um efeito positivo na cicatrização de tecidos moles após a extração não cirúrgica de dentes normalmente erupcionados, mas parece não reduzir a modelagem da crista alveolar pós-extração, embora evidências de estudos pré-clínicos indiquem que a HyA pode melhorar a formação óssea.
Autores: Danijel Domic, Kristina Bertl, Tobias Lang, Nikolaos Pandis, Christian Ulm, Andreas Stavropoulos
Referências:
- Upadhyaya C, Humagain H (2010) Prevalência de alveolite seca após extração de dentes permanentes no Hospital Universitário de Kathmandu (KUTH), Dhulikhel, Kavre, Nepal: um estudo. Kathmandu Univ Med J (KUMJ) 8(29):18–24
- Akinbami BO, Godspower T (2014) Alveolite seca: incidência, características clínicas e fatores predisponentes. Int J Dent 2014:796102
- Duarte-Rodrigues L et al (2018) Remoção do terceiro molar e seu impacto na qualidade de vida: revisão sistemática e meta-análise. Qual Life Res 27(10):2477–2489
- Halabi D et al (2018) Clorexidina para prevenção de osteíte alveolar: um ensaio clínico randomizado. J Appl Oral Sci 26:e20170245
- Kan KW et al (2002) Defeitos periodontais residuais distais ao segundo molar mandibular 6–36 meses após a extração do terceiro molar impactado. J Clin Periodontol 29(11):1004–1011
- Peng KY et al (2001) Estado periodontal do segundo molar mandibular após a extração do terceiro molar. J Periodontol 72(12):1647–1651
- MacBeth N et al (2017) Mudanças em tecidos duros e moles após a preservação da crista alveolar: uma revisão sistemática. Clin Oral Implants Res 28(8):982–1004
- Taberner-Vallverdú M et al (2015) Eficácia de diferentes métodos utilizados para o manejo da alveolite seca: uma revisão sistemática. Med Oral Patol Oral Cir Bucal 20(5):e633–e639
- Taberner-Vallverdú M, Sánchez-Garcés M, Gay-Escoda C (2017) Eficácia de diferentes métodos utilizados para a prevenção da alveolite seca e análise de fatores de risco: uma revisão sistemática. Med Oral Patol Oral Cir Bucal 22(6):e750–e758
- Han W et al (2022) A atividade anti-inflamatória de oligossacarídeos de ácido hialurônico de tamanhos específicos. Carbohydr Polym 276:118699
- Harris LG, Richards RG (2004) Adesão de Staphylococcus aureus a diferentes superfícies de titânio tratadas. J Mater Sci Mater Med 15(4):311–314
- Romanò CL et al (2017) Ácido hialurônico e seus compostos como uma barreira antimicrobiana/antiaderente local. J Bone Jt Infect 2(1):63–72
- Matheus HR et al (2021) Associação de ácido hialurônico com um enxerto bovino desproteinizado melhora a reparação óssea e aumenta a formação óssea em defeitos ósseos de tamanho crítico. J Periodontol 92(11):1646–1658
- Yun J, Lee J, Ha CW et al (2021) O efeito de um andaime de ácido polilático impresso em 3D com e sem ácido hialurônico na regeneração óssea. J Periodontol 1–11. https://doi.org/10.1002/JPER.21-0428
- Shirakata Y et al (2021) Cicatrização de feridas periodontais/regeneração de defeitos intraboneais de duas paredes após cirurgia reconstrutiva com gel de ácido hialurônico reticulado com ou sem uma matriz de colágeno: um estudo pré-clínico em cães. Quintessence Int 0(0):308–316
- Shirakata Y et al (2021) Cicatrização de recessões gengivais bucais após tratamento com retalho avançado coronariamente isolado ou combinado com um gel de ácido hialurônico reticulado. Um estudo experimental em cães. J Clin Periodontol 48(4):570–580
- Maria de Souza G et al (2020) A eficácia do ácido hialurônico no controle da dor, edema e trismo após a extração de terceiros molares: revisão sistemática e meta-análise. J Oral Maxillofac Surg 14:14
- de Vries R et al (2015) Um formato de protocolo para a preparação, registro e publicação de revisões sistemáticas de estudos de intervenção em animais. Evid-Based Preclin Med 2:e00007
- Page MJ et al (2021) A declaração PRISMA 2020: uma diretriz atualizada para relatar revisões sistemáticas. Syst Rev 10(1):89
- Hooijmans CR et al (2014) Ferramenta de risco de viés SYRCLE para estudos em animais. BMC Med Res Methodol 14:43
- Sterne JAC et al (2019) RoB 2: uma ferramenta revisada para avaliar o risco de viés em ensaios randomizados. BMJ 366:l4898
- Sterne JA et al (2016) ROBINS-I: uma ferramenta para avaliar o risco de viés em estudos não randomizados de intervenções. BMJ 355:i4919
- Higgins JPT, Thompson SG, Spiegelhalter DJ (2009) Uma reavaliação da meta-análise de efeitos aleatórios. J R Stat Soc A Stat Soc 172(1):137–159
- Wei D et al (2016) O uso da abordagem GRADE em revisões sistemáticas de estudos em animais. J Evid Based Med 9(2):98–104
- Chen H et al (2015) Como usar gradepro gdt para avaliar a qualidade da evidência em revisões sistemáticas de estudos de intervenção: Uma introdução. Chin J Evid Based Med 15:600–606
- Mendes RM et al (2010) Efeitos de nanotubos de carbono de parede única e sua funcionalização com hialuronato de sódio na reparação óssea. Life Sci 87(7–8):215–222
- Kapitan M et al (2021) Observação inicial de fatores que interferem no tratamento da osteíte alveolar usando ácido hialurônico com octenidina - uma série de relatos de casos. Biomolecules 11(8):04
- Martins-Junior PA et al (2016) Avaliação de nanotubos de carbono funcionalizados com hialuronato de sódio nos processos inflamatórios para aplicações em medicina regenerativa oral. Clin Oral Invest 20(7):1607–1616
- Catanzano O et al (2018) Esponjas compostas de alginato-hialuronano para a entrega de ácido tranexâmico em feridas alveolares pós-extração. J Pharm Sci 107(2):654–661
- Mendes RM et al (2008) O hialuronato de sódio acelera o processo de cicatrização em alvéolos dentários de ratos. Arch Oral Biol 53(12):1155–1162
- Sa MA et al (2013) Nanotubos de carbono funcionalizados com hialuronato de sódio restauram a reparação óssea em alvéolos de ratos diabéticos. Oral Dis 19(5):484–493
- Kim JJ et al (2016) O ácido hialurônico melhora a formação óssea em alvéolos de extração com patologia crônica: um estudo piloto em cães. J Periodontol 87(7):790–795
- Kim JJ et al (2019) Biomodificação de alvéolos de extração comprometidos usando ácido hialurônico e rhBMP-2: um estudo experimental em cães. J Periodontol 90(4):416–424
- Lee JB et al (2021) Efeitos do ácido hialurônico e mineral ósseo bovino desproteinizado com 10% de colágeno para preservação da crista em alvéolos de extração comprometidos. J Periodontol 23:23
- Koray M et al (2014) Eficácia do spray de ácido hialurônico sobre inchaço, dor e trismo após a extração cirúrgica de terceiros molares mandibulares impactados. Int J Oral Maxillofac Surg 43(11):1399–1403
- Gocmen G et al (2015) A eficiência antioxidante e anti-inflamatória do ácido hialurônico após a extração do terceiro molar. J Craniomaxillofac Surg 43(7):1033–1037
- Gocmen G et al (2017) Efeitos do ácido hialurônico sobre sangramento após a extração do terceiro molar. J Appl Oral Sci 25(2):211–216
- Afat İM, Akdoğan ET, Gönül O (2018) Efeitos do fibrina rica em leucócitos e plaquetas sozinha e combinada com ácido hialurônico sobre dor, edema e trismo após a extração cirúrgica de terceiros molares mandibulares impactados. J Oral Maxillofac Surg 76(5):926–932
- Bayoum A, Nadershah M, Albandar A, Alsulaimani B, Sankour I et al (2018) O efeito do ácido hialurônico reticulado na extração cirúrgica de terceiros molares mandibulares impactados. Int J Dent Oral Health 4(2). https://doi.org/10.16966/2378-7090.254
- Guazzo R et al (2018) Efeito na cicatrização de feridas de um gel tópico contendo aminoácidos e hialuronato de sódio aplicado ao alvéolo após a extração do terceiro molar mandibular: um ensaio clínico controlado randomizado duplo-cego. Quintessence Int 49(10):831–840
- Merchant R et al (2018) Avaliação comparativa da eficácia clínica do spray de ácido hialurônico versus spray de solução salina normal sobre inchaço, dor e trismo após a extração cirúrgica do terceiro molar mandibular impactado - um estudo controlado randomizado de boca dividida. Int J Sci Res 7:152
- Afat IM, Akdoğan ET, Gönül O (2019) Efeitos do fibrina rica em leucócitos e plaquetas sozinha e combinada com ácido hialurônico sobre a cicatrização inicial de tecidos moles após a extração cirúrgica de terceiros molares mandibulares impactados: um estudo clínico prospectivo. J Craniomaxillofac Surg 47(2):280–286
- Munoz-Camara D, Pardo-Zamora G, Camacho-Alonso F (2020) Efeitos pós-operatórios da aplicação intra-alveolar de géis bioadesivos de clorexidina a 0,2% ou ácido hialurônico a 1% após a extração do terceiro molar mandibular: um ensaio clínico controlado randomizado duplo-cego. Clin Oral Investig 24:24
- Yilmaz N et al (2017) A eficácia do ácido hialurônico em alvéolos pós-extração de terceiros molares impactados: um estudo piloto. Niger J Clin Pract 20(12):1626–1631
- Yang H et al (2020) Estudo de não inferioridade da eficácia de dois produtos de ácido hialurônico em alvéolos pós-extração de terceiros molares impactados. Maxillofac Plast Reconstr Surg 42(1):40
- Favia G et al (2008) Cicatrização acelerada de feridas de tecidos moles orais e efeito angiogênico induzido por um pool de aminoácidos combinado com hialuronato de sódio (AMINOGAM®). J Biol Regul Homeost Agents 22(2):109–116
- Bayoumi AM, Jan A, Amoudi WA, Shakir M (2015) Os Efeitos do Uso de Ácido Hialurônico nos Alvéolos de Extração. Int J Dent Oral Health 2(1). https://doi.org/10.16966/2378-7090.157
- Alcântara CEP et al (2018) O ácido hialurônico acelera a reparação óssea em alvéolos dentários humanos: um ensaio clínico randomizado triplo-cego. Braz Oral Res 32:e84
- Lorenz J et al (2018) Material substituto ósseo injetável à base de beta-TCP e hialuronano alcança completa regeneração óssea enquanto passa por degradação quase completa. Int J Oral Maxillofac Implants 33(3):636–644
- Marin S et al (2020) Resultado do tratamento com ácido hialurônico na cicatrização de feridas pós-extração em pacientes com diabetes tipo 2 mal controlado: um estudo controlado randomizado de boca dividida. Med Oral Patol Oral Cir Bucal 25(2):e154–e160
- Mostafa D et al (2021) Efeito do gel de ácido hialurônico na cicatrização de alvéolos de extração dentária simples: um estudo piloto. Open Access Maced J Med Sci 9(D):190–195
- Eeckhout C et al (2022) Um ensaio clínico controlado randomizado avaliando o gel de ácido hialurônico como agente de cicatrização em preservação da crista alveolar. J Clin Periodontol 49(3):280–291
- Cosola S, Oldoini G, Boccuzzi M, Giammarinaro E, Genovesi A, Covani U, Marconcini S (2022) Fórmula enriquecida com aminoácidos para o cuidado pós-operatório de alvéolos de extração avaliados por escaneamento intraoral 3D. Int J Environ Res Public Health 19(6):3302. https://doi.org/10.3390/ijerph19063302
- Cocero N et al (2019) Eficácia do hialuronato de sódio e aminoácidos sintéticos em alvéolos pós-extração em pacientes com insuficiência hepática: estudo de boca dividida. J Biol Regul Homeost Agents 33(6):1913–1919
- Dubovina D et al (2016) O uso de ácido hialurônico e ácido aminocaproico no tratamento da osteíte alveolar. Vojnosanit Pregl 73(11):1010–1015
- Suchánek J, Ivančaková RK, Mottl R, Browne KZ, Pilneyová KC, Pilbauerová N, Schmidt J, Suchánková Kleplová T (2019) Dispositivo médico à base de ácido hialurônico para tratamento da osteíte alveolar - estudo clínico. Int J Environ Res Public Health 16:3698. https://doi.org/10.3390/ijerph16193698
- Blum IR (2002) Visões contemporâneas sobre alveolite seca (osteíte alveolar): uma avaliação clínica da padronização, etiopatogenia e manejo: uma revisão crítica. Int J Oral Maxillofac Surg 31(3):309–317
- Lee J-B, Chu S, Amara HB et al (2021) Os efeitos do ácido hialurônico e mineral ósseo bovino desproteinizado com 10% de colágeno para preservação da crista em alvéolos de extração comprometidos. J Periodontol 1–12. https://doi.org/10.1002/JPER. 20-0832
- Sá MA et al (2013) Nanotubos de carbono funcionalizados com hialuronato de sódio restauram a reparação óssea em alvéolos de ratos diabéticos. Oral Dis 19(5):484–493
- Marin S et al (2020) Resultado do tratamento com ácido hialurônico na cicatrização de feridas pós-extração em pacientes com diabetes tipo 2 mal controlado: um estudo controlado randomizado de boca dividida. Medicina Oral, Patologia Oral y Cirugia Bucal 25(2):e154–e160