Implantes de Disco Articular Temporomandibular Bioengenheirados: Protocolo de Estudo para um Ensaio Piloto Pré-clínico Aleatório em Duas Fases com 18 Ovelhas Merino Negras (TEMPOJIMS)
Tradução automática
O artigo original está escrito em EN language (link para lê-lo) .
Resumo
Contexto: Ensaios pré-clínicos são essenciais para testar opções eficazes para substituir o disco da articulação temporomandibular (ATM). A ausência contemporânea de um tratamento ideal para pacientes com distúrbios severos da ATM pode estar relacionada a dificuldades quanto ao desenho de estudo apropriado para conduzir ensaios pré-clínicos na área da ATM. Essas dificuldades podem estar associadas ao uso de modelos animais heterogêneos, ao uso da ATM contralateral como controle, à ausência de ensaios pré-clínicos rigorosos e controlados randomizados com avaliadores de resultados cegos, e a dificuldades envolvendo equipes multidisciplinares.
Objetivo: Este estudo tem como objetivo desenvolver um novo desenho de estudo, reprodutível e eficaz para pesquisa pré-clínica no domínio da ATM, obtendo dados rigorosos relacionados a (1) identificar o impacto da discectomia bilateral em ovelhas Merino negras, (2) identificar o impacto da discopexia bilateral em ovelhas Merino negras, e (3) identificar o impacto de três diferentes discos de ATM bioengenheirados em ovelhas Merino negras.
Métodos: Um ensaio clínico prévio exploratório randomizado controlado em duas fases com resultados cegos é proposto. Na primeira fase, nove ovelhas são randomizadas em três diferentes procedimentos cirúrgicos bilaterais: discectomia bilateral, discopaxia bilateral e cirurgia simulada. Na segunda fase, nove ovelhas são randomizadas para testar bilateralmente três diferentes implantes de disco bioengenharia para ATM. O resultado primário é a graduação histológica da ATM. Os resultados secundários são mudanças de imagem, tempo absoluto de mastigação, tempo de ruminação por ciclo, cinética de ruminação, área de ruminação e peso das ovelhas.
Resultados: Estudos pré-clínicos anteriores neste campo utilizaram o lado contralateral não operado como controle, diferentes modelos animais variando de camundongos a um modelo canino, com desenhos de estudo não randomizados, não cegos e não controlados e medidas de resultados limitadas. O principal objetivo deste protocolo pré-clínico exploratório é estabelecer um novo padrão para futuros ensaios pré-clínicos em cirurgia oromaxilofacial, particularmente no campo da ATM, propondo um desenho rigoroso em ovelhas Merino negras. Os autores também pretendem testar a viabilidade de resultados piloto. Os autores esperam aumentar a qualidade de estudos futuros neste campo e progredir em opções de tratamento para pacientes submetidos a cirurgia de substituição do disco da ATM.
Conclusões: O estudo começou, mas é muito cedo para fornecer resultados ou conclusões.
Introdução
A articulação temporomandibular (ATM) é a articulação mais frequentemente utilizada no corpo humano. A ATM abre e fecha de 1500 a 2000 vezes por dia e é essencial para as funções diárias da boca, como mastigação, fala, deglutição, bocejo e ronco, envolvendo uma sinergia obrigatória especial de ambos os lados articulares. O disco da ATM é um componente essencial na ATM normal e tem as seguintes funções: (1) distribui a carga intra-articular, (2) estabiliza as articulações durante a translação e (3) diminui o desgaste da superfície articular. A maioria dos distúrbios da ATM (DTA) é tratada com sucesso com tratamentos reversíveis, conservadores e de baixa tecnologia, como educação e aconselhamento, exercícios terapêuticos, terapia com placa e farmacoterapia.
Quando o disco da ATM está deslocado, malformado ou danificado, pode induzir sérios processos patológicos internos e/ou osteoartrite. Atualmente, os pacientes que sofrem de DTM severa têm opções de tratamento validadas limitadas. A maioria das abordagens cirúrgicas, como a discectomia da ATM, não restaura as propriedades estruturais ou biológicas da articulação e do disco. Este procedimento pode não ser ideal porque a ATM fica sem uma estrutura funcional importante. Uma variedade de materiais interposicionais tem sido utilizada para substituir os discos removidos, incluindo materiais sintéticos fabricados a partir de silicone, Teflon, politetrafluoretileno e enxertos biológicos interposicionais retirados de diferentes locais anatômicos. Esses materiais interposicionais não levam em consideração a anatomia e as características bioquímicas e biomecânicas do disco nativo da ATM, e alguns deles têm sido associados a complicações sérias para os pacientes. No final da década de 1980, o Proplast/Teflon da ATM (implante interposicional sintético) foi considerado prejudicial em muitos pacientes. A degradação do material, provavelmente causada pelas altas forças biomecânicas da ATM, levou a partículas fragmentadas que resultaram em uma resposta imune de corpo estranho que causou problemas que variaram de reações inflamatórias cutâneas severas nas áreas pré-auriculares e das bochechas a doenças degenerativas articulares severas com perfuração na fossa craniana média. O resultado foi um espectro clínico dramático de falhas para esses implantes. Em dezembro de 1991, o Boletim da Administração de Alimentos e Medicamentos dos EUA recomendou a remoção imediata de todos os implantes Proplast/Teflon da ATM anteriores devido às falhas mecânicas, muitas resultando em degeneração óssea progressiva. Em um workshop de 1992, a Academia Americana de Cirurgia Oral e Maxilofacial instruiu a descontinuação do Proplast/Teflon.
A ausência de opções eficazes para substituir o disco da ATM pode estar relacionada a dificuldades na tradução de evidências animais para a prática clínica em humanos. Essas limitações provavelmente estão relacionadas a:
o uso de modelos animais heterogêneos com resultados conflitantes, possivelmente devido à anatomia variável e à carga intra-articular entre as espécies;
o uso da ATM contralateral como controle, que pode estar associado à sobrecarga contralateral;
os biomateriais utilizados para substituir o disco não levam em conta as características morfológicas e biomecânicas do disco nativo;
ausência de ensaios clínicos controlados randomizados com cegamento dos avaliadores de resultados; e
falta de equipes multidisciplinares envolvidas no projeto.
A pesquisa pré-clínica deve promover a tradução eficaz do conhecimento em prática. Os aspectos mencionados anteriormente podem limitar a tradução eficaz do conhecimento científico de qualidade na prática clínica e podem apresentar problemas potenciais para pacientes, clínicos e o progresso científico.
A ausência contemporânea de opções bem-sucedidas para substituir o disco da ATM ainda é um grande problema para a saúde pública. Pouca coisa mudou na última década em relação aos desenhos de estudo para investigação da ATM, e o tratamento para pacientes com DTM severa continua sendo controverso. O principal objetivo do Estudo de Material Interposicional da Articulação Temporomandibular (TEMPOJIMS) é desenvolver um novo desenho de estudo, reprodutível e eficaz para pesquisa pré-clínica no campo da ATM. O segundo objetivo é avançar na bioengenharia e medicina regenerativa avaliando os benefícios de um implante de bioengenharia da ATM para substituir o disco nativo danificado da ATM. Este estudo exploratório pré-clínico é dividido em duas fases. A Fase 1 deste estudo é um ensaio clínico pré-clínico randomizado cego, projetado para investigar se a ATM sofre lesão importante na discectomia bilateral, discopexia bilateral e cirurgia simulada. As intenções da Fase 2 são avaliar a segurança e eficácia de três diferentes implantes de bioengenharia da ATM usando o mesmo método rigoroso da fase 1.
Métodos
Desenho do Estudo
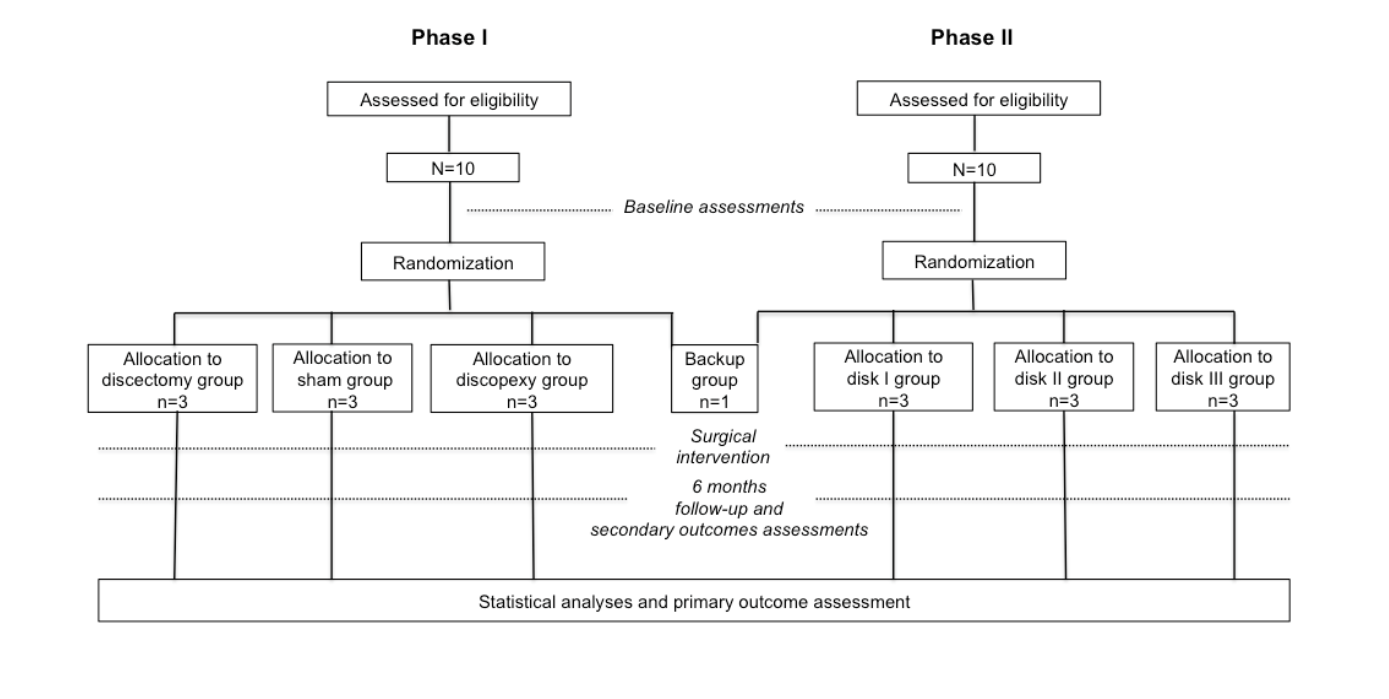
O TEMPOJIMS é um ensaio clínico pré-clínico randomizado exploratório de duas fases planejado para reunir informações preliminares para (1) avaliar um novo desenho de estudo para investigação da ATM; (2) avaliar o modelo animal de ovelha Merino negra para investigação da ATM; (3) avaliar o comportamento da ATM sob intervenção cirúrgica bilateral (discectomia e discopaxia) utilizando um desfecho primário histológico (pontuação microscópica de mudanças destrutivas na ATM usando um sistema de pontuação Mankin modificado), desfecho secundário de imagem (pontuação de imagem da ATM); (4) testar a aplicabilidade de desfechos secundários piloto predominantemente para a cinética de ruminantes; e (5) obter uma linha de base para interpretação dos resultados de implantes bioengenheirados de disco da ATM. A Fase II tem como objetivo testar a segurança e eficácia de três diferentes implantes de disco bioengenheirados para ATM bilateral (Figura 1). Os avaliadores e analistas de desfechos estão cegos para as avaliações cirúrgicas.
As principais instituições envolvidas neste estudo são (1) Faculdade de Medicina de Lisboa para o desenho do estudo, coordenação e análise estatística; (2) Centro Interdisciplinar de Investigação em Saúde Animal da Faculdade de Medicina Veterinária para preparação histológica e suporte veterinário de todos os animais; (3) Centro de Desenvolvimento Rápido e Sustentável de Produtos para implantes de disco bioengenheirados (discos I e II); (4) Bioengenharia, Cirurgia, Engenharia Química, Engenharia Mecânica e Ciência dos Materiais, Universidade de Pittsburgh, para implantes de disco bioengenheirados (disco III); (5) Departamento de Cirurgia Oral e Maxilofacial-Cabeça e Pescoço, Hospital Universitário Infanta Cristina, Badajoz, Espanha, para suporte cirúrgico; (6) Instituto de Pesquisa Óssea e Articular-Distrito de Saúde Local do Norte de Sydney-Escola de Medicina de Sydney do Norte, Universidade de Sydney, Austrália, para análise histológica; e (7) Departamento de Radiologia do Hospital Santa Maria, Lisboa, Portugal, para análise de imagem.
Modelo Animal
Uma variedade de linhagens/raças de ovelhas tem sido utilizada em investigações sobre a ATM. Para diminuir a variabilidade biológica, os autores recomendaram ovelhas Merino pretas como o modelo animal para conduzir o estudo. Conforme recomendado, os autores propuseram usar “ovelhas esqueléticamente maduras” com ≥2 anos de idade. Os critérios de inclusão são ovelhas Merino pretas certificadas, adultas (idade de 2 a 5 anos), fêmeas e em boas condições de saúde (um exame veterinário é realizado em todos os animais). Em relação às considerações éticas sobre os animais, o desenho do estudo foi aprovado pela Autoridade Nacional Portuguesa para a Saúde Animal, registrada com o número 026618. O desenho e a organização do estudo respeitam as diretrizes de Pesquisa Animal: Relato de Experimentos In Vivo (ARRIVE).
Avaliação Basal e de Acompanhamento
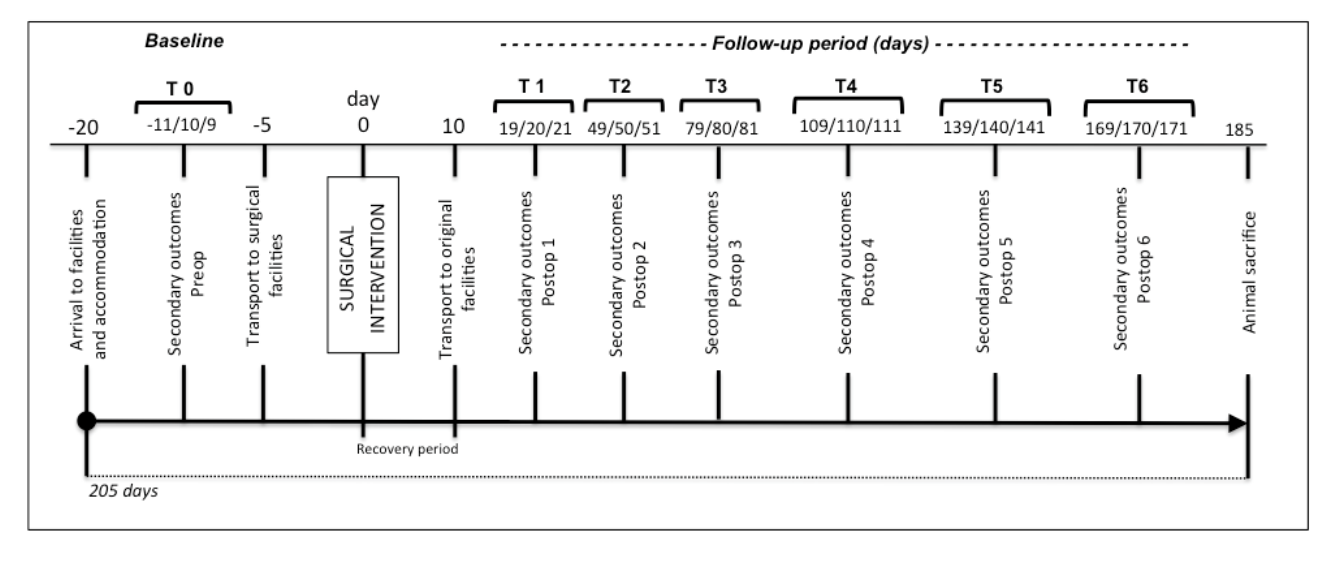
As avaliações basal e de acompanhamento são delineadas em pontos de tempo específicos (Figura 2). Resultados secundários piloto e peso são medidos nos dias 11, 10 e 9 antes da cirurgia (detalhes sobre os resultados secundários são relatados nas medidas de resultados). O transporte para as instalações cirúrgicas é realizado 5 dias antes da cirurgia para evitar estresse nos animais e permitir a familiarização com as instalações temporárias. A tomografia computadorizada (TC) da cabeça é realizada no dia da cirurgia, aproveitando a sedação pré-anestésica. Dez dias após a cirurgia, os animais são transportados para as principais instalações do TEMPOJIMS. Nos dias 19, 20 e 21 após a cirurgia, os resultados secundários de acompanhamento começam a ser registrados a cada 30 dias durante 6 meses (Figura 2). No final, os animais são sacrificados e uma nova TC é realizada para medir o resultado de imagem e iniciar a preparação histológica.
Randomização, Alocação e Cegamento
A randomização é realizada por um grupo estatístico não envolvido nas avaliações de desfecho, gerido pela Faculdade de Medicina de Lisboa. A alocação a cada grupo randomizado é realizada pré-operatoriamente por envelope lacrado e separadamente para a fase 1 e fase 2 do estudo. A equipe cirúrgica não está cega em relação à alocação do tratamento, dado o tipo de intervenção; no entanto, os membros da equipe cirúrgica não estão envolvidos nas avaliações de desfecho. Todos os avaliadores de desfecho estão cegos em relação à intervenção. Na fase 1, 10 ovelhas são alocadas ao grupo de intervenção: grupo de cirurgia simulada (n=3), grupo de discectomia (n=3), grupo de discopaxia (n=3) e grupo de reserva (n=1). A ovelha de reserva está planejada para ser utilizada se ocorrer morte devido à anestesia ou outra complicação não relacionada à intervenção cirúrgica. Na fase 2, 10 ovelhas são aleatoriamente atribuídas ao grupo disco I (n=3), grupo disco II (n=3), grupo disco III (n=3) e grupo de reserva (n=1) (Figura 1).
Fase de Intervenção
Protocolo de Anestesia
O jejum e a restrição de água são necessários 24 horas antes da cirurgia. A sedação é realizada com diazepam (0,5 mg/kg iv), seguida pela indução da anestesia com cetamina (5 mg/kg iv). A intubação oral é realizada e a anestesia é mantida com isoflurano (1,5% a 2%). Para garantir a analgesia do animal, meloxicam (0,5 mg/kg iv, bid) é administrado no dia da cirurgia e durante 4 dias no pós-operatório. Profilaxia antibiótica com amoxicilina e ácido clavulânico é utilizada por 5 dias.
Protocolo de Intervenção Cirúrgica para as Fases 1 e 2
Fase 1
Discectomia bilateral (n=3): sob anestesia geral, a equipe cirúrgica realiza uma incisão na pele pré-auricular e uma dissecação romba do tecido mole que cobre a articulação. A área da articulação é exposta e a cápsula articular é incisa. O disco e suas ligações são identificados. As ligações medial, anterior, posterior e lateral do disco são destacadas e a discectomia é realizada. A ferida é fechada em camadas.
Discopexia bilateral (n=3): sob anestesia geral, a equipe cirúrgica realiza uma incisão na pele pré-auricular e uma dissecação romba do tecido mole que cobre a articulação. A área da articulação é exposta e a cápsula articular é incisa. O disco e suas fixações são identificados. As fixações lateral e posterior do disco são destacadas e suturadas com poli- p-dioxanona (PDS) 3/0. A ferida é fechada em camadas.
Cirurgia simulada (n=3): sob anestesia geral, a equipe cirúrgica realizará uma incisão na pele pré-auricular e uma dissecação romba do tecido mole que cobre a articulação. A cápsula não é incisa. A ferida é fechada em camadas.
Fase 2
Disco I (n=3): sob anestesia geral, a equipe cirúrgica realiza uma incisão na pele pré-auricular e uma dissecação romba do tecido mole que cobre a articulação. A área da articulação é exposta e a cápsula articular é incisa. O disco e suas fixações são identificados. As fixações medial, anterior, posterior e lateral do disco são destacadas e a discectomia é realizada. O disco I é introduzido no espaço articular e suturado nas fixações laterais. A ferida é fechada em camadas. O disco I será um biomaterial alternativo e, por razões intelectuais, não pode ser revelado neste artigo.
Disco II (n=3): sob anestesia geral, a equipe cirúrgica realiza uma incisão na pele pré-auricular e uma dissecação romba do tecido mole que cobre a articulação. A área da articulação é exposta e a cápsula articular é incisa. O disco e suas ligações são identificados. As ligações medial, anterior, posterior e lateral do disco são destacadas e a discectomia é realizada. O disco II é introduzido no espaço articular e suturado nas ligações laterais. A ferida é fechada em camadas. O disco II será um suporte poroso de poli(glicerol sebacato) (PGS) reforçado com poli(caprolactona) (PCL).
Disco III (n=3): sob anestesia geral, a equipe cirúrgica realiza uma incisão na pele pré-auricular e uma dissecação romba do tecido mole que cobre a articulação. A área da articulação é exposta e a cápsula articular é incisa. O disco e suas ligações são identificados. As ligações medial, anterior, posterior e lateral do disco são destacadas e a discectomia é realizada. O disco III é introduzido no espaço articular e suturado na ligação lateral. A ferida é fechada em camadas. O disco III será um suporte poroso de PGS preparado por um método modificado de fusão de sal. Resumidamente, partículas de sal moídas (150 mg) com um tamanho variando de 25 a 32 µm serão colocadas em um molde impresso em 3-D. O molde será transferido para um incubador a 37°C e 90% de umidade relativa por 1 hora. Os moldes fundidos de partículas de sal secarão em um forno a vácuo a 90°C e 100 millitorr (mTorr) durante a noite, removendo cuidadosamente o bolo de sal do molde antes do processamento adicional. PGS recém-fabricado dissolvido em tetra-hidrofurano (THF; 20% em peso, 380 µL, sal:PGS=2:1) é adicionado ao bolo de sal, e o THF é permitido evaporar completamente em uma capela de exaustão por 30 minutos. O bolo de sal é transferido para um forno a vácuo e curado a 150°C e 100 mTorr por 24 horas. Os moldes de sal impregnados com PGS resultantes são imersos em água deionizada por 4 horas, e então substituídos por água por 4 horas, com troca de água a cada 4 horas durante as primeiras 12 horas. Após o banho de água de 12 horas, os suportes são transferidos para água deionizada por mais 24 horas com troca de água a cada 8 horas. Os suportes resultantes são congelados a –80°C e, em seguida, o processo de liofilização é aplicado.
Dez dias para recuperação é contemplado para cuidados com feridas e medicação pós-operatória (veja Figura 2).
Medidas de Resultado
O resultado primário é a pontuação microscópica das alterações destrutivas na ATM usando um sistema de pontuação Mankin modificado. Os resultados secundários são a pontuação de imagem das alterações destrutivas da ATM, tempo absoluto de mastigação, tempo de ruminação por ciclo, cinética de ruminação, área de ruminação e peso corporal das ovelhas. Os parâmetros de resultado primários e secundários estão descritos com mais detalhes em Figura 3.
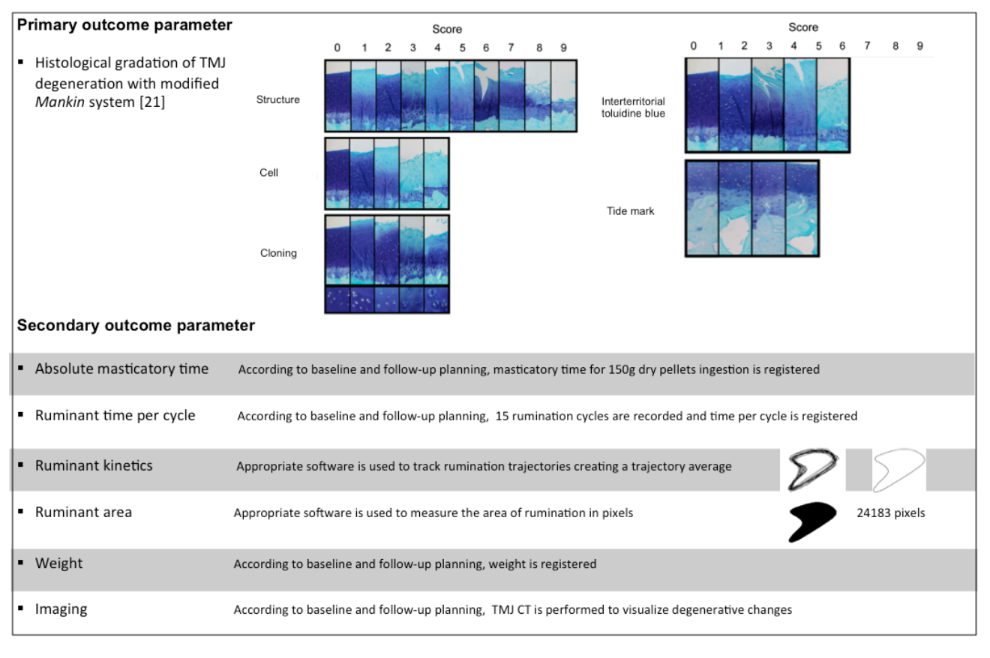
Resultado Primário
O objetivo é avaliar a graduação histológica das alterações destrutivas da ATM. O ponto de tempo é 6 meses após a intervenção cirúrgica.
Seis meses após a cirurgia, a ATM é removida utilizando uma serra oscilatória de osso de necropsia de acordo com as seguintes referências anatômicas: cranial (aspecto cranial do processo coronoide na região de união do processo zigomático), caudal (externo ao meato acústico), dorsal (referência estabelecida ao osso temporal escamoso) e ventral (referência fixada 2 cm abaixo do meato acústico na zona do ângulo estilohióideo). As articulações são fixadas em formalina tamponada a 10% por 24 horas e armazenadas em etanol a 70%. A descalcificação é obtida por imersão em ácido fórmico a 10% em formalina a 5% por até 20 dias, após o que as articulações são cortadas sagitalmente através de todo o côndilo. Após a descalcificação, as articulações da ATM são imersas em três misturas graduadas de metil salicilato/parafina e cortadas sagitalmente da parte lateral para a parte central da ATM. As seções histológicas são enviadas ao Instituto de Pesquisa Óssea e Articular de Sydney para pontuação histológica usando um sistema de pontuação Mankin modificado. Esta avaliação é realizada e classificada de forma independente por dois histologistas que estarão cegos para a intervenção. Um terceiro histologista atuará como árbitro em caso de disparidade.
Resultados Secundários
As características avaliadas são análise de imagem, tempo absoluto de mastigação, tempo de ruminação por ciclo, cinemática de ruminação, área de ruminação e peso das ovelhas (veja Apêndices Multimídia 1 e 2). O ponto de tempo é a cada mês após a intervenção cirúrgica por um total de 6 meses.
Para medir os resultados secundários, uma gaiola específica (veja Figura 4) foi construída com uma janela frontal e um alimentador.
Análise de imagem: a TC pré-operatória é realizada em todas as ovelhas. Após o sacrifício do animal, os blocos da ATM são escaneados por TC e a avaliação de imagem é realizada usando os critérios e pontuação descritos na Tabela 1.
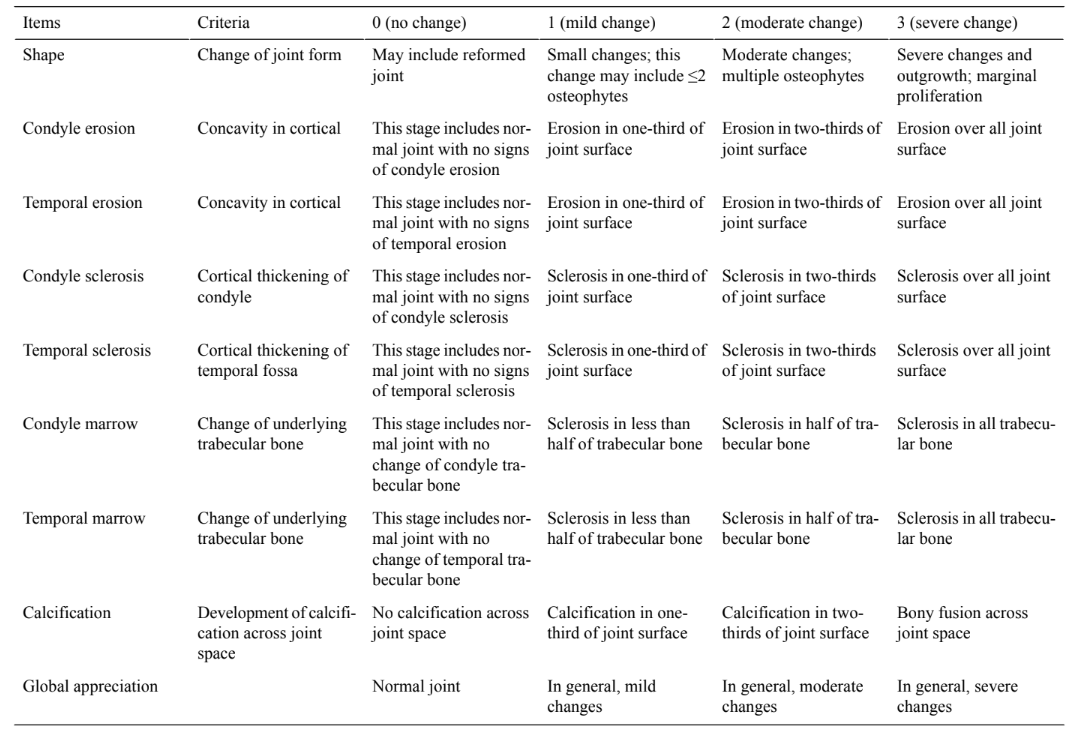

Esta avaliação é realizada e classificada de forma independente por dois radiologistas experientes que estarão cegos para a intervenção. Um terceiro radiologista atuará como árbitro em caso de disparidade.
Tempo absoluto de mastigação: respeitando o fluxograma (Figura 2), às 9:00 da manhã os animais são colocados em gaiolas individuais. Uma dose de 150 gramas de pellets secos (Rico Gado A3) é introduzida no comedouro e o tempo até que eles comam todos os pellets é medido com um cronômetro (veja Apêndice Multimídia 1).
Tempo de ruminação por ciclo: respeitando o cronograma (Figura 2), registramos 15 ciclos de ruminação aproximadamente 4 horas após a alimentação de 150 gramas. Usamos uma câmera de vídeo Canon 7D e imagens com 25 quadros por segundo. Em seguida, o número de quadros por ciclo é dividido por 25 para obter o tempo em segundos por ciclo (veja Apêndice Multimídia 2).
Cinetica de ruminantes: usamos o software Foundry Nuke (rastreamento 2D) para realizar o rastreamento ruminatório e obter a média do ciclo ruminatório. Com o software After Effects , convertamos o rastreamento 2-D em uma forma geométrica (veja Apêndice Multimídia 2).
Área ruminante: determinamos a média de 15 ciclos e criamos uma forma geométrica. Usando o software Image J, realizamos uma medida quantitativa em pixels da média da área ruminante.
Peso: de acordo com o cronograma, após comer 150 gramas de pellets secos, as ovelhas são pesadas (veja Apêndice Multimídia 1).
Todas as avaliações são realizadas por pesquisadores que estão cegos para a intervenção cirúrgica.
Análises Estatísticas
Todas as análises estatísticas serão realizadas usando o SPSS versão 22 (IBM Corp, Armonk, NY, EUA). Uma análise transversal será realizada para comparar as variáveis de resultado nos três níveis da variável independente antes e depois da atribuição do grupo de tratamento randomizado. Nas análises transversais, uma análise de variância unidirecional (ANOVA) será realizada, após testar todas as suposições. Para a análise longitudinal, uma ANOVA unidirecional com medidas repetidas será realizada considerando como efeitos dentro dos sujeitos as observações após a cirurgia (meses 1 a 6). O teste de diferença mínima significativa de Fisher será realizado como testes pós-hoc para verificar diferenças significativas para os diferentes tratamentos.
Relato de Eventos Adversos
Eventos adversos relacionados ao estudo serão considerados, incluindo (1) eventos de anestesia: morte idiopática, pneumotórax, outras complicações relacionadas à anestesia; (2) técnica cirúrgica: sangramento maciço, fratura condilar, outras complicações relacionadas à técnica cirúrgica; e (3) eventos pós-operatórios: infecção da ATM, deiscência de sutura, diminuição do apetite, paresia facial, diminuição da ruminação, diminuição de peso.
Discussão
Este estudo investiga os efeitos e efeitos adversos de (1) discectomia bilateral, (2) discopexia bilateral e (3) implantes de disco bioengenheirados. Embora este estudo pré-clínico sirva principalmente como um estudo piloto, esperamos obter uma melhor compreensão das mudanças morfológicas e histológicas na ATM e suas implicações na cinética mastigatória.
Até agora, os resultados sobre discectomia são conflitantes. Estudos pré-clínicos anteriores nesta área usaram o lado contralateral não operado como controle e diferentes modelos animais variando de camundongos a um modelo canino. Usar o lado contralateral como controle pode ser inadequado considerando a influência da sobrecarga contralateral. Teoricamente, esperamos reduzir esse viés usando uma abordagem bilateral. A variabilidade animal nos diferentes estudos é um alerta sobre a importância de usar o mesmo modelo animal em estudos futuros sobre investigações de implantes na ATM. Portanto, nosso grupo realizou um estudo anterior considerando ovelhas Merino negras como um modelo animal promissor para estudos sobre investigações de implantes de disco na ATM, próteses de ATM e modelo de osteoartrite da ATM. Para aumentar a qualidade do TEMPOJIMS, os autores usarão um grupo controle de cirurgia simulada.
Esperamos obter informações valiosas relacionadas ao grupo de discopexia da fase 1 sobre se a abordagem cirúrgica promove danos intra-articulares. Isso pode melhorar as conclusões futuras sobre a atribuição de possíveis danos à intervenção em si, em vez do implante de ATM. Esta questão é importante considerando que uma abordagem cirúrgica para colocar implantes de ATM na fase 2 será necessária. Novamente, usar uma intervenção bilateral poderia reduzir um possível viés.
A maioria dos estudos pré-clínicos se concentrou em avaliações morfológicas/histológicas grossas e não foi projetada para caracterizar o movimento articular fundamental alterado (cinética) ou as consequências funcionais. Neste estudo, incluímos resultados secundários piloto para avaliar mudanças na cinética de ruminantes. Esperamos correlacionar os resultados primários com os resultados secundários para entender se podem ser utilizados em futuros estudos de ATM. Pode ser interessante entender vários itens:
- Existem diferenças em relação ao tempo de mastigação nos grupos de disco em comparação com discectomia e discopexia?
- Há uma correlação entre os resultados histológicos, de imagem e cinéticos?
- A área e a geometria do ruminante mudam ao realizar diferentes intervenções?
- Há uma diferença em relação à cinética do ruminante nos grupos de disco em comparação com discectomia e discopexia?
- Os implantes de ATM aceleram a osteoartrite?
Em relação à fase 2, a escolha do biomaterial é crítica. O implante de ATM será exposto a um ambiente mecânico e estressante com um suprimento sanguíneo limitado que pode restringir a migração celular e a regeneração in situ. Testar três discos de bioengenharia diferentes in vivo e correlacionar in vitro com o comportamento in vivo pode melhorar seriamente as estratégias de bioengenharia para alcançar um implante de disco de ATM seguro e eficaz para humanos.
A principal força deste estudo é o modelo animal proposto; os resultados convencionais e piloto descritos; o desenho do estudo com um grupo de controle randomizado, cego e placebo; e o uso de procedimentos cirúrgicos bilaterais. As potenciais limitações do estudo incluem o tamanho relativamente pequeno da amostra. Se este estudo confirmar a viabilidade do protocolo proposto e a eficácia inicial dos implantes de disco da ATM planejados, um ensaio pré-clínico maior seria justificado para determinar ainda mais a eficácia desses discos e promover a tradução das evidências animais para a prática clínica em humanos.
Autores: David Faustino Ângelo, Florencio Gil Monje, Raúl González-García, Christopher B Little, Lisete Mónico, Mário Pinho, Fábio Abade Santos, Belmira Carrapiço, Sandra Cavaco Gonçalves, Pedro Morouço, Nuno Alves, Carla Moura, Yadong Wang, Eric Jeffries, Jin Gao, Rita Sousa, Lia Lucas Neto, Daniel Caldeira, Francisco Salvado
Referências
- Bae Y, Park Y. O efeito dos exercícios de relaxamento para os músculos mastigatórios na disfunção da articulação temporomandibular (ATM). J Phys Ther Sci 2013;25(5):583-586. [doi: 10.1589/jpts.25.583]
- Allen K, Athanasiou K. Engenharia de tecidos do disco da ATM: uma revisão. Tissue Eng 2006;12(5):1183-1196. [doi: 10.1089/ten.2006.12.1183]
- Tanaka E, Sasaki A, Tahmina K, Yamaguchi K, Mori Y, Tanne K. Propriedades mecânicas do disco articular humano e sua influência na carga da ATM estudadas com o método de elementos finitos. J Oral Rehabil 2001 Mar;28(3):273-279. [Medline: 11394374]
- Martins-Júnior RL, Palma Antônio JC, Marquardt EJ, Gondin TM, Kerber FD. Transtornos temporomandibulares: um relato de 124 pacientes. J Contemp Dent Pract 2010 Oct 14;11(5):71-78. [Medline: 20978727]
- Navrátil L, Navratil V, Hajkova S, Hlinakova P, Dostalova T, Vranová J. Tratamento abrangente de distúrbios da articulação temporomandibular. Cranio 2014 Jan;32(1):24-30. [doi: 10.1179/0886963413Z.0000000002] [Medline: 24660643]
- Mehra P, Wolford LM. O mini âncora Mitek para reposicionamento do disco da ATM: técnica cirúrgica e resultados. Int J Oral Maxillofac Surg 2001 Dec;30(6):497-503. [doi: 10.1054/ijom.2001.0163] [Medline: 11829231]
- Al-Baghdadi M, Durham J, Araujo-Soares V, Robalino S, Errington L, Steele J. Manejo do deslocamento do disco da ATM sem redução: uma revisão sistemática. J Dent Res 2014 Jul;93(7 Suppl):37S-51S [FREE Full text] [doi: 10.1177/0022034514528333] [Medline: 24659775]
- Estabrooks L, Fairbanks C, Collett R, Miller L. Uma avaliação retrospectiva de 301 implantes Proplast-Teflon da ATM. Oral Surg Oral Med Oral Pathol 1990 Sep;70(3):381-386. [Medline: 2216373]
- Henry CH, Wolford LM. Resultados do tratamento para reconstrução da articulação temporomandibular após falha do implante Proplast-Teflon. J Oral Maxillofac Surg 1993 Apr;51(4):352-358; discussão 359. [Medline: 8450350]
- Mercuri LG, Giobbie-Hurder A. Resultados a longo prazo após reconstrução total aloplástica da articulação temporomandibular após exposição a materiais falhos. J Oral Maxillofac Surg 2004 Sep;62(9):1088-1096. [Medline: 15346359]
- Morouço P, Ângelo D, Francisco L, Moura C, Alves N. Engenharia de tecidos para reparo e regeneração do disco da articulação temporomandibular: uma perspectiva metodológica. Adv Cell Mol Otolaryngol 2017 Jan 17;4(1):33709. [doi: 10.3402/acmo.v4.33709]
- Lypka M, Yamashita DR. Reação exuberante de células gigantes de corpo estranho a um implante de teflon/proplast da articulação temporomandibular: relato de um caso. J Oral Maxillofac Surg 2007 Sep;65(9):1680-1684. [doi: 10.1016/j.joms.2006.09.030] [Medline: 17719383]
- Spagnoli D, Kent JN. Avaliação multicêntrica do implante de disco Proplast-Teflon da articulação temporomandibular. Oral Surg Oral Med Oral Pathol 1992 Oct;74(4):411-421. [Medline: 1408011]
- Fricton JR, Look JO, Schiffman E, Swift J. Estudo a longo prazo da cirurgia da articulação temporomandibular com implantes aloplásticos comparado com cirurgia não implantada e reabilitação não cirúrgica para deslocamento doloroso do disco da articulação temporomandibular. J Oral Maxillofac Surg 2002 Dec;60(12):1400-1411; discussão 1411. [doi: 10.1053/joms.2002.36091] [Medline: 12465000]
- Kulber DA, Davos I, Aronowitz JA. Reação cutânea severa de corpo estranho após reconstrução da articulação temporomandibular com Proplast-Teflon. J Oral Maxillofac Surg 1995 Jun;53(6):719-722; discussão 722. [Medline: 7776062]
- Chuong R, Piper MA. Vazamento de líquido cefalorraquidiano associado à remoção de implante proplast da articulação temporomandibular. Oral Surg Oral Med Oral Pathol 1992 Oct;74(4):422-425. [Medline: 1408012]
- Berarducci JP, Thompson DA, Scheffer RB. Perfuração na fossa craniana média como sequela do uso de um implante Proplast-Teflon para reconstrução da articulação temporomandibular. J Oral Maxillofac Surg 1990 May;48(5):496-498. [Medline: 2329399]
- [Nenhum autor listado]. Recomendações para o manejo de pacientes com implantes da articulação temporomandibular. Workshop de Cirurgia de Implante da Articulação Temporomandibular. J Oral Maxillofac Surg 1993 Oct;51(10):1164-1172. [Medline: 8410459]
- Herring S. Anatomia da ATM e modelos animais. J Musculoskelet Neuronal Interact 2003 Dec;3(4):391-394; discussão 406 [FREE Full text] [Medline: 15758330]
- Angelo D, Morouço P, Alves N, Viana T, Santos F, González R. Escolhendo ovelhas (Ovis aries) como modelo animal para pesquisa da articulação temporomandibular: caracterização morfológica, histológica e biomecânica do disco articular. Morphologie 2016 Jul:223-233 [FREE Full text] [doi: 10.1016/j.morpho.2016.06.002] [Medline: 27450042]
- Leiggener CS, Erni S, Gallo LM. Abordagem inovadora para o estudo da cinemática da mandíbula em uma reconstrução aloplástica da ATM. Int J Oral Maxillofac Surg 2012 Sep;41(9):1041-1045. [doi: 10.1016/j.ijom.2012.06.014] [Medline: 22819692]
- Little CB, Smith MM, Cake MA, Read RA, Murphy MJ, Barry FP. A iniciativa de histopatologia OARSI - recomendações para avaliações histológicas da osteoartrite em ovelhas e cabras. Osteoarthritis Cartilage 2010 Oct;18 Suppl 3:S80-S92 [FREE Full text] [doi: 10.1016/j.joca.2010.04.016] [Medline: 20864026]
- Cake MA, Appleyard RC, Read RA, Smith MM, Murrell GA, Ghosh P. Ovariectomia altera as propriedades estruturais e biomecânicas da cartilagem articular femoro-tibial ovina e aumenta o iNOS da cartilagem. Osteoarthritis Cartilage 2005 Dec;13(12):1066-1075 [FREE Full text] [doi: 10.1016/j.joca.2005.07.001] [Medline: 16154775]
- Cohen W, Servais J, Polur I, Li Y, Xu L. Degeneração da cartilagem articular na articulação temporomandibular contralateral não cirúrgica em camundongos com discectomia parcial unilateral. J Oral Pathol Med 2014 Feb;43(2):162-165. [doi: 10.1111/jop.12113] [Medline: 24044578]
- Ahtiainen K, Mauno J, Ellä V, Hagström J, Lindqvist C, Miettinen S, et al. Células-tronco adiposas autólogas e discos de polilactídeo na substituição do disco da articulação temporomandibular do coelho. J R Soc Interface 2013 Aug 06;10(85):20130287 [FREE Full text] [doi: 10.1098/rsif.2013.0287] [Medline: 23720535]
- Brown B, Chung W, Almarza A, Pavlick M, Reppas S, Ochs M. Abordagem regenerativa baseada em indução e suporte para a reconstrução do disco da articulação temporomandibular. J Oral Maxillofac Surg 2012 Nov;70(11):2656-2668. [doi: 10.1016/j.joms.2011.12.030]
- Xu L, Polur I, Lim C, Servais J, Dobeck J, Li Y, et al. Osteoartrite de início precoce da articulação temporomandibular em camundongos induzida por discectomia parcial. Osteoarthritis Cartilage 2009 Jul;17(7):917-922. [doi: 10.1016/j.joca.2009.01.002] [Medline: 19230720]
- Lai WT, Tsai Y, Su S, Su C, Stockstill JW, Burch JG. Análise histológica da regeneração dos discos da articulação temporomandibular em coelhos utilizando um template de colágeno reconstituído. Int J Oral Maxillofac Surg 2005 May;34(3):311-320. [doi: 10.1016/j.ijom.2004.05.003] [Medline: 15741041]
- Sato S, Goto S, Koeda S, Motegi K. Mudanças na rede de fibras elásticas da articulação temporomandibular do coelho após discectomia. J Oral Rehabil 2002 Sep;29(9):847-852. [Medline: 12366539]
- Sato S, Goto S, Motegi K. Mudanças na disposição das fibras de colágeno da articulação temporomandibular do coelho após discectomia. J Craniomaxillofac Surg 2002 Jun;30(3):178-183. [Medline: 12220997]
- Bjørnland T, Haanaes HR. Discectomia da articulação temporomandibular: um estudo experimental em macacos. J Craniomaxillofac Surg 1999 Apr;27(2):113-116. [Medline: 10342149]
- Ogi N, Kurita K, Ishimaru JI, Goss AN. Efeito a curto prazo do uso de um aloenxerto de disco congelado para reparo da articulação temporomandibular osteoartrítica do carneiro: um relatório preliminar. J Oral Maxillofac Surg1999 Feb;57(2):139-144; discussão 144. [Medline: 9973121]
- Hinton R, Stinson J. Efeito da dieta pós-operatória na resposta da cartilagem condilar à discectomia. J Oral Maxillofac Surg 1997 Nov;55(11):1259-1264. [Medline: 9371117]
