Avaliação das propriedades físico-químicas de quatro selantes de canal radicular
Tradução automática
O artigo original está escrito em EN language (link para lê-lo) .
Resumo
Objetivo: Avaliar as propriedades físico-químicas e a morfologia da superfície dos selantes de canal radicular AH Plus, GuttaFlow, RoekoSeal e Activ GP.
Metodologia: Cinco amostras de cada material foram avaliadas quanto ao tempo de presa, alteração dimensional, solubilidade e testes de radiopacidade, de acordo com a Especificação ANSI/ADA 57. Um total de 50 mL de água destilada deionizada dos testes de solubilidade foi utilizado para medir a solubilidade metálica por espectrometria de absorção atômica. As morfologias da superfície externa e da seção transversal das amostras foram analisadas por meio de um microscópio eletrônico de varredura (SEM). A análise estatística foi realizada utilizando ANOVA de uma via e testes post hoc Tukey–Kramer com a hipótese nula estabelecida em 5%.
Resultados: O AH Plus teve o maior tempo de presa (580,6 ± 3,05 min) (P< 0,05). O Activ GP não apresentou um valor médio nos testes de radiopacidade e solubilidade (1,31 ± 0,35 mm e 11,8 ± 0,43%, respectivamente) de acordo com a ANSI/ADA, sendo significativamente diferente dos outros materiais (P< 0,05), que tiveram valores médios para esses testes em conformidade com os requisitos da ADA. O GuttaFlow foi o único selante que atendeu à Especificação 57 em relação ao teste de alteração dimensional (0,44 ± 0,16%) (P< 0,05). O teste de espectrometria revelou liberação significativa de íons Ca2+, K+, Zn2+ do selante Activ GP (32,57 ± 5,0, 1,57 ± 0,22 e 8,20 ± 1,74 μg mL–1, respectivamente). Na análise SEM, a perda de matriz foi evidente e as partículas de enchimento eram mais distinguíveis em todos os grupos.
Conclusões: O tempo de configuração de todos os selantes estava de acordo com os requisitos da ANSI/ADA. O Activ GP não atendeu aos protocolos da ANSI/ADA em relação à radiopacidade, alteração dimensional e solubilidade. O Gutta-Flow foi o único selante que se conformou à Especificação 57 em todos os testes. A análise de MEV revelou que as superfícies de todos os selantes apresentaram alterações micromorfológicas após o teste de solubilidade.
Introdução
No tratamento de canal radicular, o selamento completo do sistema de canal radicular após a limpeza e modelagem é crítico para prevenir que patógenos orais colonizem e reinfectem os tecidos radiculares e periapicais. Embora a guta-percha ainda seja o material de preenchimento de canal radicular mais comumente utilizado, várias novas técnicas e materiais com diferentes propriedades físico-químicas foram desenvolvidos (Ørstavik 2005, Versiani et al. 2006, Resende et al. 2009).
Durante os procedimentos de preenchimento de canal, o selante endodôntico desempenha várias funções, incluindo o preenchimento de irregularidades nas paredes do canal radicular, como ramificações apicais e deltóides, bem como espaços onde a guta-percha não conseguiu se adaptar (Kontakiotis et al. 2007). Como os materiais de preenchimento convencionais não selam efetivamente o espaço do canal radicular, novos selantes endodônticos foram desenvolvidos (Bouillaguet et al. 2008).
Embora o AH Plus tenha uma estabilidade dimensional adequada a longo prazo, sua capacidade de selagem permanece controversa, em parte porque o AH Plus não adere à guta-percha (Ørstavik et al. 2001). O RoekoSeal Automix (Coltène Whaledent, Langenau, Alemanha) é um selante que contém dimetilpolissiloxano, com dados limitados disponíveis sobre suas propriedades físico-químicas (Gençoglu et al. 2003). Apesar dos dados clínicos e laboratoriais promissores relatados para o selante à base de silicone, o RoekoSeal foi testado em vários estudos com resultados contraditórios (De-Deus et al. 2007). O GuttaFlow (Coltène Whaledent, Alstätten, Suíça) é um selante à base de polivinilsiloxano e foi introduzido com a intenção de reduzir as desvantagens das técnicas de guta-percha quente (Eldeniz & Ørstavik 2009). Foi afirmado que o GuttaFlow poderia melhorar o selamento devido ao aumento da fluidez e ao fato de que o material se expande ligeiramente ao endurecer (Bouillaguet et al. 2008, Eldeniz & Ørstavik 2009, Roggendorf et al. 2010).
As aplicações dentais de selantes de ionômero de vidro aproveitam sua adesão ao dentina, liberação de flúor, atividade antimicrobiana e biocompatibilidade (Ørstavik 2005). No entanto, alguns testes laboratoriais indicaram uma propensão para vazamentos e desintegração (Carvalho-Júnior et al. 2003, Schäfer & Zandbiglari 2003). Recentemente, o Sistema de Obturacão Activ GP Precision (Brasseler USA, Savannah, GA, EUA) foi comercializado como um sistema monobloco de preenchimento radicular, utilizando cones de guta-percha convencionais que são revestidos na superfície com preenchimentos de ionômero de vidro (Roggendorf et al. 2010). O fabricante afirma que o produto é superior aos sistemas anteriores à base de ionômero de vidro em termos de características de manuseio, tempo de trabalho, radiopacidade (Fransen et al. 2008) e vedação, devido ao aumento da fluidez e ao fato de que o material se expande ligeiramente ao endurecer (Kontakiotis et al. 2007).
Embora vários tipos de selantes endodônticos tenham sido propostos como materiais de preenchimento inovadores, o selante ideal para canal radicular ainda não foi encontrado (Ørstavik 1983, 2005, Ørstavik et al. 2001, Versiani et al. 2006, Resende et al. 2009). Portanto, o objetivo deste estudo laboratorial foi comparar o tempo de endurecimento, radiopacidade, mudança dimensional e solubilidade de selantes à base de silicone (GuttaFlow e RoekoSeal) e um selante à base de ionômero (Activ GP) com um selante à base de resina epóxi bem estabelecido (AH Plus), de acordo com os padrões ANSI/ADA (2000).
Materiais e métodos
O tempo de configuração, radiopacidade, mudanças dimensionais e solubilidade, após a configuração para AH Plus (grupo I), GuttaFlow (grupo II), RoekoSeal (grupo III) e Activ GP (grupo IV) selantes de canais radiculares foram medidos de acordo com os padrões ANSI/ADA (2000) para materiais de selagem de canais radiculares. Os materiais testados (Tabela 1) foram manipulados de acordo com as instruções do fabricante. As análises foram realizadas por um único examinador que estava cego para os materiais experimentais. Para padronizar e homogeneizar a quantidade de material, 0,3 g de selante foi dispensado em uma placa de mistura e espatulada por 15 s para cada amostra testada. Para os testes físico-químicos, a média aritmética de cinco réplicas para cada selante foi registrada e considerada como o resultado do teste.
Tempo de definição
Cinco anéis de gesso, com um diâmetro interno de 10 mm e uma espessura de 2 mm foram preparados. As bordas externas dos moldes foram fixadas com cera em uma placa de vidro (75 x 25 x 1 mm). Os moldes foram então preenchidos com o material e transferidos para uma câmara com 95% de umidade relativa (UR) e uma temperatura de 37 °C. Após 150 ± 10 s do início da mistura do selante, uma agulha do tipo Gilmore com uma massa de 100 ± 0,5 g, tendo uma extremidade plana de 2,0 ± 0,1 mm de diâmetro, foi cuidadosamente abaixada verticalmente sobre a superfície horizontal de cada amostra. A ponta da agulha foi limpa e a sondagem foi repetida até que as impressões deixadas parassem de ser visíveis. Se os resultados diferissem em mais de ±5%, o teste foi repetido.
Teste de radiopacidade
Cinco placas de acrílico (2,2 cm x 4,5 cm x 1 mm), contendo quatro poços medindo 1 mm de profundidade e 5 mm de diâmetro, foram preparadas e colocadas sobre uma placa de vidro coberta por uma folha de celofane. Cada poço foi preenchido com um dos selantes, seguindo uma sequência de acordo com o tempo de definição do material, do mais longo para o mais curto, de modo que as amostras estivessem prontas para avaliação radiográfica após a definição final de todos os materiais. Para evitar a formação de bolhas, o selante recém-misturado foi introduzido nos poços usando uma seringa. Outra placa de vidro coberta com celofane foi colocada por cima até a definição completa e qualquer excesso de selante foi removido. Cada placa foi mantida em um incubador (37°C, 95% UR) por um período correspondente a três vezes o tempo de definição.
Cada uma das placas de acrílico contendo os selantes foi posicionada, no momento da exposição radiográfica, ao lado de outra placa de acrílico (1,3 cm x 4,5 cm x 1 mm), contendo um degrau de alumínio, feito de liga 1100, com a espessura variando de 1 a 10 mm, em passos uniformes de 1 mm cada (Margraf Dental MFG Inc., Jenkintown, PA, EUA). Este conjunto de placas de acrílico foi colocado em frente a esta placa de fósforo, ao lado do degrau de alumínio, e uma radiografia digital foi realizada (sistema Digora™; Soredex Orion Corporation, Helsinque, Finlândia). Imagens radiográficas foram obtidas usando a máquina de raios X Spectro 70X (Dabi Atlante, Ribeirão Preto, SP, Brasil), a 70 kVp e 8 mA. A distância objeto-foco foi de 30 cm e o tempo de exposição foi de 0,2 s. As placas de imagem expostas das amostras de teste foram imediatamente digitalizadas após a exposição (Scanner Digora™) e analisadas usando o software Digora™ para Windows 5.1.
Alteração dimensional
Cinco moldes de Teflon® (Politetrafluoretileno, DuPont, HABIA, Knivsta, Suécia), preparados para a produção de corpos de teste cilíndricos de 3,58 mm de altura medindo 3 mm de diâmetro, foram colocados sobre uma placa de vidro envolta em uma fina folha de celofane. Os moldes foram preenchidos com um leve excesso de selantes recém-misturados e uma lâmina de microscópio, também envolta em celofane, foi pressionada sobre a superfície superior do molde. O grupo montado foi mantido firmemente unido com uma braçadeira em forma de C e transferido para um incubador (37 °C, 95% UR) deixado em repouso por um período correspondente a três vezes o tempo de endurecimento. Após esse período, as extremidades planas dos moldes, contendo as amostras, foram lixadas com papel de lixa molhado de grão 600. As amostras foram removidas do molde, medidas com um paquímetro digital, armazenadas em um recipiente de 50 mL contendo 2,24 mL de água destilada deionizada, e mantidas em um incubador (37 °C, 95% UR) por 30 dias. A amostra foi então removida do recipiente, seca em papel absorvente e medida novamente para comprimento. A porcentagem das alterações dimensionais foi calculada usando a fórmula:
((L30 — L )/ L) x 100
onde L30 é o comprimento da amostra após 30 dias de armazenamento e L é o comprimento inicial da amostra.
Solubilidade
Um molde cilíndrico de Teflon® com 1,5 mm de espessura e 7,75 mm de diâmetro interno foi preenchido com selante recém-misturado. O molde foi apoiado por uma placa de vidro maior e coberto com uma folha de celofane. Um fio de nylon impermeável foi colocado dentro do material e outra placa de vidro, também coberta com filme de celofane, foi posicionada sobre o molde e pressionada manualmente de forma que as placas tocassem todo o molde de maneira uniforme. O conjunto foi colocado em um incubador (37 °C, 95% UR) e deixado em repouso por um período correspondente a três vezes o tempo de endurecimento. Assim que as amostras foram removidas do molde, foram pesadas três vezes cada uma (HM-200, A & D Engineering, Inc., Bradford, MA, EUA), e a média das leituras registrada. As amostras foram suspensas por fio de nylon e colocadas duas a duas dentro de um recipiente plástico com uma abertura larga contendo 7,5 mL de água destilada deionizada, tomando cuidado para evitar qualquer contato entre elas e a superfície interna do recipiente. Os recipientes foram selados e deixados por 7 dias em um incubador (37 °C, 95% UR). Após esse período, as amostras foram removidas dos recipientes, enxaguadas com água destilada deionizada, secas com papel absorvente e colocadas em um desumidificador por 24 h. Em seguida, foram pesadas novamente. A perda de peso de cada amostra (massa inicial menos massa final), expressa como uma porcentagem da massa original (m% = mi – mf), foi considerada como a solubilidade do selante.
Um volume de 7,5 mL de água destilada de cada amostra foi despejado em um crisol de porcelana limpo e seco. Cada crisol foi colocado em um mufla e queimado a 550 °C. As cinzas foram dissolvidas em 10 mL de ácido nítrico concentrado (Merck KGaA, Darmstadt, Alemanha) usando uma vara de vidro. Em seguida, as amostras foram colocadas em frascos volumétricos de 50 mL e o volume completado com água deionizada ultrapura (MilliQ, Millipore, Billerica, MA, EUA). As soluções obtidas foram pulverizadas no espectrofotômetro de absorção atômica (Perkin Elmer, Überlingen, Alemanha) para verificar a presença de íons Ca2+, K+, Zn2+ e Ag+. A média aritmética de três réplicas para cada espécime foi registrada e considerada como o resultado, expresso em μg mL–1.
Exame de microscopia eletrônica de varredura
Para o exame de microscopia eletrônica de varredura (SEM), moldes cilíndricos de Teflon® (3 x 4 mm) foram preenchidos com selantes recém-misturados. Os moldes foram apoiados em uma placa de vidro coberta com uma folha de celofane e colocados em uma câmara (37 °C, 95% UR) por um período correspondente a três vezes o tempo de endurecimento. Após isso, as amostras foram seccionadas com uma lâmina de bisturi cirúrgico descartável número 15, fixadas em um suporte metálico (10 x 5 mm) e revestidas com uma camada de ouro-páladio (Bal-Tec AG, Balzers, Alemanha) a 20 mA. As morfologias da superfície externa e da seção transversal das amostras foram analisadas qualitativamente sob um SEM de emissão de campo (Jeol JSM 5410; Jeol Technic Co., Tóquio, Japão) a uma tensão de aceleração de 15 kV, uma distância de trabalho de 6 a 10 mm e em diferentes ampliações.
Análise estatística
Cinco espécimes de cada grupo foram testados e as médias foram comparadas estatisticamente. O teste de Kolmogorov–Smirnov mostrou que os resultados eram consistentes com uma curva de distribuição normal, assim, a análise estatística paramétrica foi possível (anova de um fator e post hoc teste de Tukey–Kramer), e a hipótese nula foi estabelecida em 5% (spss 17.0 para Windows; SPSS Inc., Chicago, IL, EUA).
Resultados
Tempo de configuração
A especificação ANSI/ADA (2000) exige que o tempo de configuração de um selante esteja dentro de 10% do que é declarado pelos fabricantes. De acordo com eles, os tempos de configuração do AH Plus, RSA RoekoSeal e Gutta-Flow são 480, 50 e 30 min, respectivamente. Por outro lado, o fabricante do Activ GP não fornece essa informação e apenas afirma que foi formulado com um tempo de trabalho estendido de 15 minutos.
Uma diferença estatisticamente significativa foi observada entre os grupos AH Plus (580,6 ± 3,05 min), GuttaFlow (24,0 ± 2,0 min), RoekoSeal (40,0 ± 1,58 min) e Activ GP (15,2 ± 1,30 min) (P< 0,05). No entanto, os valores médios mostraram concordância com a padronização ANSI/ADA (Tabela 2).
Teste de radiopacidade
AH Plus (6.0 ± 0.12 mmAl), GuttaFlow (3.0 ± 0.04 mmAl) e RoekoSeal (4.17 ± 0.45 mmAl) apresentaram radiopacidade acima de 3 mm de alumínio, conforme recomendado pela Especificação ANSI/ADA 57, enquanto Activ GP (1.31 ± 0.35 mmAl) não atendeu a esse requisito. A análise estatística demonstrou diferença entre os grupos experimentais (P < 0.05) (Tabela 2).
Alteração dimensional
A padronização ANSI/ADA (2000) afirma que a contração linear média do selante não deve exceder 1% ou 0,1% em expansão. Exceto pelo GuttaFlow (0,44 ± 0,16%), nenhum selante estava em conformidade com a Especificação 57 (ANSI/ADA 2000). Todos os grupos exibiram expansão pós-configuração, exceto o RoekoSeal, que mostrou contração na configuração (-1,33 ± 0,12%). A análise estatística revelou diferença significativa entre os grupos experimentais (P < 0,05) (Tabela 2).
Solubilidade
A Especificação 57 da ANSI/ADA (2000) afirma que um selante de canal radicular não deve exceder 3% em massa quando a solubilidade do material definido é testada. Exceto pelo Activ GP (11,8 ± 0,43%), todos os selantes estavam em conformidade com a padronização ANSI/ADA (P < 0,05) (Tabela 2). A água destilada deionizada utilizada para o teste de solubilidade e submetida à espectrometria de absorção atômica mostrou um nível significativo de liberação de íons Ca2+, K+ e Zn2+ no grupo Activ GP em comparação com AH Plus, Gutta-Flow e RoekoSeal (P < 0,05). Níveis significativos de liberação de Ag+ não foram observados em nenhum grupo (Tabela 3).

Exame SEM
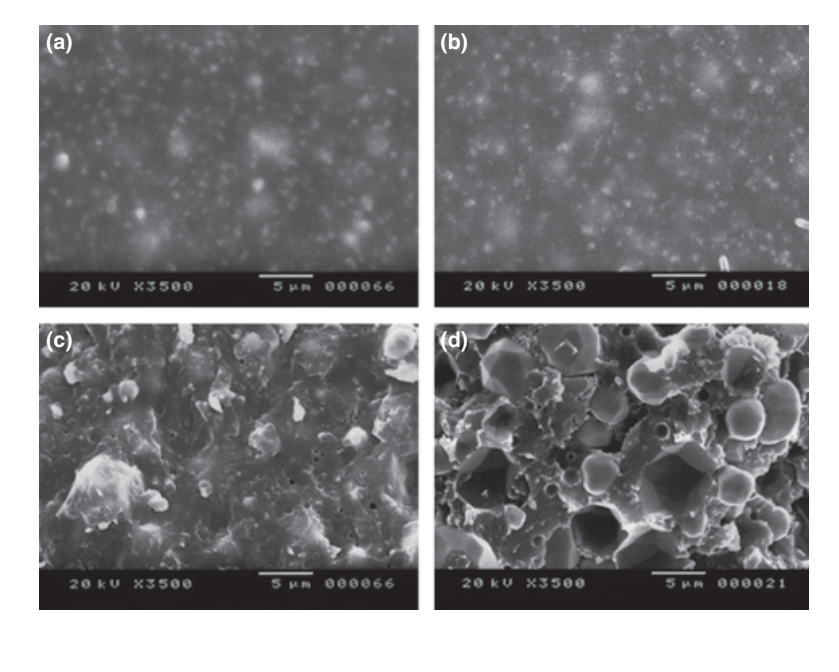
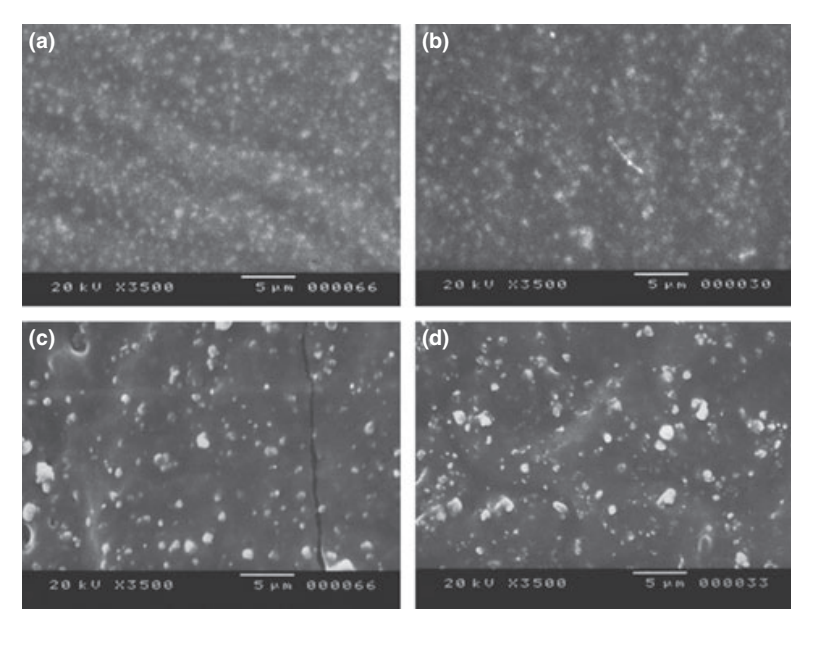
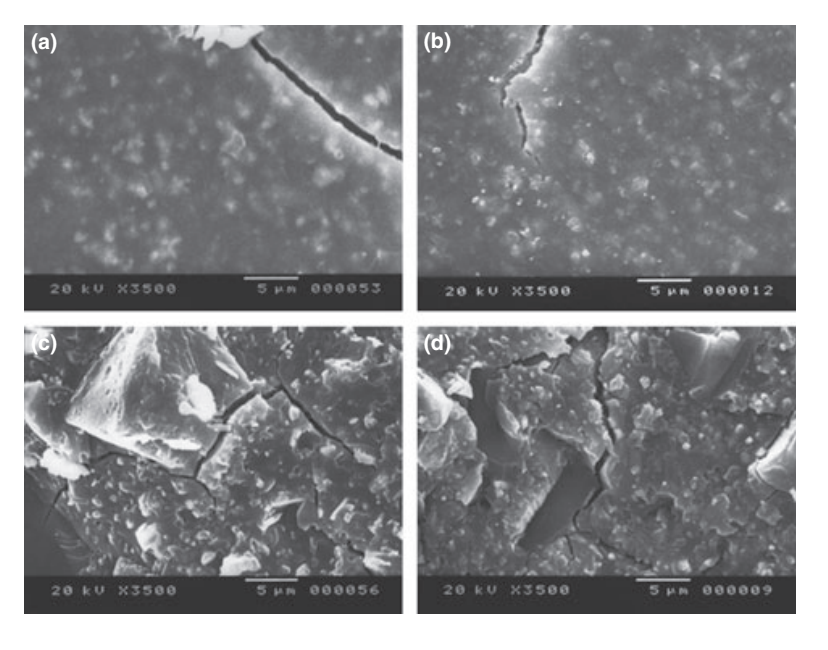
Fotomicrografias selecionadas das amostras polimerizadas obtidas antes e depois do armazenamento em água por 7 dias são apresentadas nas Figuras 1–4. No geral, observou-se que todas as superfícies apresentaram alterações micromorfológicas após o teste de solubilidade. A perda da matriz foi evidente e as partículas de preenchimento eram mais distinguíveis. Os grupos AH Plus (Fig. 1a,b), GuttaFlow (Fig. 2a,b) e RoekoSeal (Fig. 3a,b) tinham uma superfície externa que parecia ser principalmente superfícies ásperas homogêneas que diminuíram na rugosidade após o teste de solubilidade, com um subsequente aumento da aspereza da superfície. Fissuras não foram observadas nas amostras, exceto no grupo Activ GP. A superfície das amostras Activ GP era relativamente mais áspera quando comparada com os outros grupos e o material da superfície parecia estar mais danificado após o teste de solubilidade (Fig. 4a,b).
A microscopia eletrônica de varredura da superfície da seção transversal das amostras revelou a presença de polímeros em forma de esfera de diferentes tamanhos que estavam dispersos de maneira não homogênea. Após o teste de solubilidade, a superfície interna das amostras de AH Plus (Fig. 1c,d), GuttaFlow (Fig. 2c,d) e Activ GP (Fig. 4c,d) parecia ser muito mais irregular e áspera. Várias microfissuras foram observadas nas interfaces matriz polimérica-filler no grupo Activ GP antes e depois do teste de solubilidade (Fig. 4c,d). Por outro lado, o grupo RoekoSeal tinha uma camada mais uniforme e compacta composta por polímeros em forma de esfera com uma maior quantidade de matriz de resina (Fig. 3c,d).

Discussão
O tempo de configuração é principalmente um teste de controle sobre o comportamento estável de um produto e depende dos componentes constituintes, seu tamanho de partícula, a temperatura ambiente e a umidade relativa (Ørstavik 1983, 2005, Ørstavik et al. 2001). No presente estudo, todos os resultados estavam de acordo com a especificação ANSI/ADA. O maior tempo de configuração do AH Plus pode ser explicado por este selante ser um material de pasta de dois componentes baseado em uma reação de polimerização lenta de aminas de resina epóxi com alto peso molecular (Bisfenol A e Bisfenol F), onde a conversão de monômeros em polímeros ocorre gradualmente (Lin-Gibson et al. 2006, Resende et al. 2009). Esses resultados estavam em concordância com pesquisas anteriores (Versiani et al. 2006, Resende et al. 2009), no entanto, Garrido et al. (2010) relataram um tempo de configuração de 13 h para o AH Plus, que está acima da variação de 10% permitida pela Especificação Número 57 da ADA.
Os padrões ANSI/ADA (2000) para a radiodensidade de materiais de selagem de canais radiculares foram determinados usando filmes dentais convencionais onde as imagens radiográficas são obtidas pelo processamento químico (Taşdemir et al. 2008). No entanto, a radiografia digital está se tornando cada vez mais comum no estudo de selantes endodônticos (Baksi Akdeniz et al. 2007, Carvalho-Júnior et al. 2007a, Rasimick et al. 2007, Taşdemir et al. 2008). Assim, no presente estudo, imagens digitais de materiais de preenchimento radicular e etapas de um cunho de alumínio foram adquiridas usando um sistema de placa de fósforo e um sistema digital de escaneamento, captura e leitura.
Uma análise da composição dos materiais testados revelou que todos possuem agentes radiopacificadores (Tabela 1), exceto o selante Activ GP. De acordo com Tanomaru-Filho et al. (2008), a presença de pó de vidro de aluminosilicato de bário em sua composição não proporciona uma radiopacidade satisfatória. O AH Plus contém óxido de zircônio, óxido de ferro e tugstate de cálcio como radiopacificadores (Tanomaru-Filho et al. 2007) e teve o maior valor médio de radiopacidade (6,0 ± 0,12 mmAl), conforme relatado anteriormente (Tagger & Katz 2003, Carvalho-Júnior et al. 2007a, Tanomaru-Filho et al. 2007, Taşdemir et al. 2008). O selante RoekoSeal contém dióxido de zircônio como radiopacificador (Baksi Akdeniz et al. 2007) e o resultado presente (4,17 ± 0,45 mmAl) estava de acordo com descobertas anteriores que mostraram sua radiopacidade variando de 4,0 a 5,7 (Tagger & Katz 2003, Gambarini et al. 2006, Tanomaru-Filho et al. 2007, Rasimick et al. 2007). A menor radiopacidade do GuttaFlow (3,0 ± 0,04 mmAl) em comparação ao RoekoSeal também foi observada em estudos anteriores (Tagger & Katz 2003, Gambarini et al. 2006, Rasimick et al. 2007, Tanomaru-Filho et al. 2007). Como o fabricante não fornece o tipo químico e a concentração de nano-prata no GuttaFlow, é aparente que essas partículas não exerceram uma característica radiopaca. A alta solubilidade dos selantes de canal radicular é indesejável porque a dissolução pode causar a liberação de materiais que poderiam irritar os tecidos periapicais e também pode permitir a formação de lacunas entre os canais radiculares e os materiais de preenchimento, o que provavelmente aumentará a fuga bacteriana ao longo do tempo (Donnelly et al. 2007). Apesar das recomendações da ANSI/ADA, no presente estudo foi utilizada uma modificação previamente proposta para ambos os testes, que alcançou resultados semelhantes com uma diminuição no volume de material necessário para a produção das amostras de teste (Carvalho-Júnior et al. 2007b). No presente estudo, o AH Plus se expandiu no teste de mudança dimensional. O ganho lento de massa ao longo do tempo foi principalmente devido à energia de interação entre a água e os locais de adsorção para o sistema (ou seja, um grupo hidroxila, um grupo amino, a extremidade da cadeia polimérica, etc.), preenchendo as lacunas entre as cadeias poliméricas (McDermott 1993). Possivelmente, essa expansão compensou a contração sofrida pelo selante à base de resina após a polimerização (Phillips & Skinner 1991, Carvalho-Júnior et al. 2007b, Resende et al. 2009, Garrido et al. 2010).
A polimerização do AH Plus é alcançada através dos monômeros de poliaminas em sua composição (amina 1-adamantano, N,N’-dibenzil-5-oxa-nonandi-amina-1,9, TCD-Diamina). Quando os compostos de diepóxido e a pasta de poliaminas são misturados, os grupos amina reagem com os grupos epóxido para formar uma ligação covalente. A utilização de grupos amina alifáticos cíclicos promove modificações na taxa de cura, densidade de entrelaçamento e morfologia das resinas epóxi. Cada grupo NH pode reagir com um grupo epóxido, de modo que o polímero resultante é fortemente entrelaçado, sendo assim rígido e forte (McDermott 1993, Case et al. 2005). Isso pode explicar a superfície rugosa homogênea e compacta revelada na análise de SEM e os baixos resultados de solubilidade do AH Plus no presente estudo. Schäfer & Zandbiglari (2003) também mediram a solubilidade de resinas epóxi (AH Plus, AH 26), à base de silicone (RoekoSeal), hidróxido de cálcio (Apexit, Sealapex), óxido de zinco-eugenol (Aptal-Harz) e selantes à base de ionômero de vidro (Ketac Endo) em água e saliva artificial. De acordo com esses autores, o AH Plus teve a menor perda de peso de todos os selantes testados, independentemente do meio de solubilidade utilizado.
Descobertas anteriores mostraram que selantes à base de polidimetilsiloxano se expandem ligeiramente durante a cura e exibem mínima absorção de água e solubilidade (Donnelly et al. 2007, Monticelli et al. 2007). De acordo com esta afirmação, no presente estudo, os selantes GuttaFlow e RoekoSeal apresentaram baixa solubilidade com mínima liberação de íons metálicos. Considerando o teste de mudança dimensional, GuttaFlow foi o único selante que atendeu à Especificação 57 (ANSI/ADA 2000), apresentando uma expansão de aproximadamente 0,44%. O mesmo não foi observado com seu predecessor, RoekoSeal, que demonstrou encolhimento (1,33%). Por outro lado, este resultado não estava de acordo com Ørstavik et al. (2001), que relataram que o Roeko-Seal teve uma pequena expansão de cerca de 0,2% em 4 semanas, e foi estável a partir daí.
A presença de guta-percha e partículas de nano-prata no selante GuttaFlow confere melhor estabilidade à matriz polimérica devido à força de atração entre átomos de prata e moléculas de guta-percha na rede polimérica (Malynych et al. 2001). Essas interações podem explicar a baixa liberação de íons de prata do GuttaFlow observada na espectroscopia de absorção atômica. Além disso, a presença de guta-percha na rede polimérica do GuttaFlow resultou em maior adsorção de água do que o RoekoSeal (Gong et al. 2008), explicando as diferenças nos resultados do teste de mudança dimensional e a camada mais uniforme e compacta observada na superfície do RoekoSeal sob SEM.
Os maiores resultados de solubilidade e mudança dimensional do selante Activ GP podem estar relacionados à metodologia da ANSI/ADA que recomenda que uma amostra seja imersa em água após um período de três vezes o tempo de presa do material. De acordo com Wilson & McLean (1988), o tempo de presa do cimento ionomérico é completado apenas 24 h após a mistura. Durante o tempo de maturação dos cimentos de vidro-ionômero, a presença de umidade pode causar a dissolução de ânions e cátions que formam a matriz para as áreas ao redor do cimento (Monticelli et al. 2007). Essa dissolução de íons não permite que a água, que faz parte da composição do cimento, hidrate a matriz (Ca2+ e Al3+ formam polissais com grupos de COO-do ácido poliacrílico), tornando-a instável (Carvalho-Júnior et al. 2003, Schäfer & Zandbiglari 2003, Donnelly et al. 2007). Isso poderia explicar a superfície mais áspera observada em MEV e o nível significativo de liberação de íons de cálcio, potássio e zinco do Activ GP no presente estudo. Como as estruturas dos cimentos de vidro-ionômero provavelmente são influenciadas pela presença ou ausência de água, elas são sensíveis à desidratação no início do processo de presa (Wilson & McLean 1988). Para a avaliação por MEV, a desidratação da amostra é um processo essencial, o que pode explicar as microfissuras observadas na superfície das amostras de Activ GP. Portanto, os resultados obtidos com o Activ GP no presente estudo devem ser interpretados com cautela.
Conclusões
O tempo de configuração de todos os selantes estava de acordo com os requisitos da ANSI/ADA. O Activ GP não atendeu aos protocolos da ANSI/ADA em relação à radiopacidade, alteração dimensional e solubilidade. O GuttaFlow foi o único selante que se conformou à Especificação 57 em todos os testes. A análise de MEV revelou que as superfícies de todos os selantes apresentaram alterações micromorfológicas após o teste de solubilidade.
Autores: D. S. H. Flores, F. J. A. Rached-Júnior, M. A. Versiani, D. F. C. Guedes, M. D. Sousa-Neto, J. D. Pécora
Referências:
- ANSI/ADA (2000) Especificação n° 57 Material de Selagem Endodôntica. Chicago, EUA: ADA Publishing.
- Baksi Akdeniz BG, Eyuboglu TF, Sen BH, Erdilek N (2007) O efeito de três selantes diferentes na radiopacidade de obturações radiculares em canais simulados. Oral Surgery Oral Medicine Oral Pathology Oral Radiology and Endodontics 103, 138–41.
- Bouillaguet S, Shaw L, Barthelemy J, Krejci I, Wataha JC (2008) Capacidade de selagem a longo prazo do Selante de Canal Pulpar, AH-Plus, GuttaFlow e Epiphany. International Endodontic Journal 41, 219–26.
- Carvalho-Júnior JR, Guimarães LF, Correr-Sobrinho L, Pécora JD, Sousa-Neto MD (2003) Avaliação da solubilidade, desintegração e alterações dimensionais de um selante de canal radicular de ionômero de vidro. Brazilian Dental Journal 14, 114–8.
- Carvalho-Júnior JR, Correr-Sobrinho L, Correr AB, Sinhoreti MA, Consani S, Sousa-Neto MD (2007a) Radiopacidade de materiais de obturação radicular usando radiografia digital. International Endodontic Journal 40, 514–20.
- Carvalho-Júnior JR, Correr-Sobrinho L, Correr AB, Sinhoreti MA, Consani S, Sousa-Neto MD (2007b) Solubilidade e alteração dimensional após a configuração de selantes de canal radicular: uma proposta para dimensões menores de amostras de teste. Journal of Endodontics 33, 1110–6.
- Case SL, O’Brien EP, Ward TC (2005) Perfis de cura, densidade de entrelaçamento, tensões residuais e adesão em um modelo de epóxi. Polymer 46, 10831–40.
- De-Deus G, Brandão MC, Fidel RA, Fidel SR (2007) A capacidade de selagem do GuttaFlow em canais de formato oval: um estudo ex vivo usando um modelo de vazamento polimicrobiano. International Endodontic Journal 40, 794–9.
- Donnelly A, Sword J, Nishitani Y et al. (2007) Sorção de água e solubilidade de selantes de canal radicular à base de resina metacrilato. Journal of Endodontics 33, 990–4.
- Eldeniz AU, Ørstavik D (2009) Uma avaliação laboratorial do vazamento bacteriano coronal em canais radiculares preenchidos com selantes novos e convencionais. International Endodontic Journal 42, 303–12.
- Fransen JN, He J, Glickman GN, Rios A, Shulman JD, Honeyman A (2008) Avaliação comparativa do selante ActiV GP/Ionômero de Vidro, Resilon/Epiphany e Gutta-Percha/AH Plus: um estudo de vazamento bacteriano. Journal of Endodontics 34, 725–7.
- Gambarini G, Testarelli L, Pongione G, Gerosa R, Gagliani M (2006) Propriedades radiográficas e reológicas de um novo selante endodôntico. Australian Endodontic Journal 32, 31–4.
- Garrido ADB, Lia RCC, França EC, da Silva JF, Astolfi-Filho S, Sousa-Neto MD (2010) Avaliação laboratorial das propriedades físico-químicas de um novo selante de canal radicular à base de Copaifera multijuga óleo-resina. International Endodontic Journal 43, 283–91.
- Gençoglu N, Türkmen C, Ahiskali R (2003) Um novo selante de canal radicular à base de silicone (Roekoseal-Automix). Journal of Oral Rehabilitation 30, 753–7.
- Gong W, Zeng K, Wang L, Zheng S (2008) Poli(hidroxiéter de bisfenol A)-bloco-copolímero alternado de polidimetilsiloxano e suas misturas nanoestruturadas com resina epóxi. Polymer 49, 3318–26.
- Kontakiotis EG, Tzanetakis GN, Loizides AL (2007) Um estudo comparativo dos ângulos de contato de quatro selantes de canal radicular diferentes. Journal of Endodontics 33, 299–302.
- Lin-Gibson S, Landis FA, Drzal PL (2006) Investigação combinatória da caracterização de estrutura-propriedades de redes de dimetacrilato fotopolimerizadas. Biomaterials 27, 1711–7.
- Malynych S, Robuck H, Chumanov G (2001) Fabricação de montagens bidimensionais de nanopartículas de Ag e nano-cavidades em resina de poli(dimetilsiloxano). Nano Letters 1, 647–9.
- McDermott J (1993) A Estrutura da Indústria de Compósitos Avançados: Advance Composites Bluebook. Cleveland: Advanstar Communications.
- Monticelli F, Sword J, Martin RL et al. (2007) Propriedades de selagem de dois sistemas contemporâneos de obturação de cone único. International Endodontic Journal 40, 374–85.
- Ørstavik D (1983) Propriedades físicas de selantes de canal radicular: medição de fluxo, tempo de trabalho e resistência à compressão. International Endodontic Journal 16, 99–107.
- Ørstavik D (2005) Materiais utilizados para obturação de canal radicular: testes técnicos, biológicos e clínicos. Endodontic Topics 12, 25–38.
- Ørstavik D, Nordahl I, Tibballs JE (2001) Alteração dimensional após a configuração de materiais de selante de canal radicular. Dental Materials 17, 512–9.
- Phillips RW, Skinner EW (1991) A Ciência dos Materiais Dentários de Skinner, 9ª ed. Filadélfia: Saunders.
- Rasimick BJ, Shah RP, Musikant BL, Deutsch AS (2007) Radiopacidade de materiais endodônticos em filme e um sensor digital. Journal of Endodontics 33, 1098–101.
- Resende LM, Rached-Junior FJ, Versiani MA et al. (2009) Um estudo comparativo das propriedades físico-químicas dos selantes de canal radicular AH Plus, Epiphany e Epiphany SE. International Endodontic Journal 42, 785–93.
- Roggendorf MJ, Legner M, Ebert J, Fillery E, Frankenberger R, Friedman S (2010) Avaliação de micro-CT de material residual em canais preenchidos com Activ GP ou GuttaFlow após remoção com instrumentos de NiTi. International Endodontic Journal 43, 200–9.
- Schäfer E, Zandbiglari T (2003) Solubilidade de selantes de canal radicular em água e saliva artificial. International Endodontic Journal 36, 660–9.
- Tagger M, Katz A (2003) Radiopacidade de selantes endodônticos: desenvolvimento de um novo método para medição direta. Journal of Endodontics 29, 751–5.
- Tanomaru-Filho M, Jorge EG, Guerreiro Tanomaru JM, Goncalves M (2007) Avaliação da radiopacidade de novos materiais de preenchimento de canal radicular pela digitalização de imagens. Journal of Endodontics 33, 249–51.
- Tanomaru-Filho M, Jorge EG, Tanomaru JM, Goncalves M (2008) Avaliação da radiopacidade de selantes de canal radicular à base de hidróxido de cálcio e ionômero de vidro. International Endodontic Journal 41, 50–3.
- Tas¸demir T, Yesilyurt C, Yildirim T, Er K (2008) Avaliação da radiopacidade de novas pastas/selantes de canal radicular por radiografia digital. Journal of Endodontics 34, 1388–90.
- Versiani MA, Carvalho-Junior JR, Padilha MI, Lacey S, Pascon EA, Sousa-Neto MD (2006) Um estudo comparativo das propriedades físico-químicas dos selantes de canal radicular AH Plus e Epiphany. International Endodontic Journal 39, 464–71.
- Wilson AD, McLean JW (1988) Cimento de Ionômero de Vidro. Chicago: Quintessence Pub. Co.
