Microrganismos da placa dentária
Tradução automática
O artigo original está escrito em RU language (link para lê-lo) .
Atualmente, os microbiologistas alcançaram um sucesso significativo no estudo do papel da flora bacteriana na placa dentária no desenvolvimento de doenças periodontais.
Sobre o estudo da microflora oral em um webinar Cariologia: diagnóstico, avaliação de risco, tratamento não invasivo e minimamente invasivo em odontopediatria.
Placa Dentária
Poucas horas após uma limpeza cuidadosa dos dentes, a placa dentária começa a se formar novamente nos dentes devido a certos processos físico-químicos entre a superfície do esmalte e os componentes da saliva, o que causa a formação de um filme muito fino — a película.
O processo de sua formação passa pelas seguintes etapas:
- migração de bactérias,
- adesão,
- fixação,
- colonização.
As associações microbianas, na ausência de cuidados higiênicos adequados, crescem constantemente. Após 36 horas, a placa dentária, que é uma formação estruturada, macia, fixada ao dente, pode ser visualmente identificada durante um exame clínico e não pode ser removida com água.
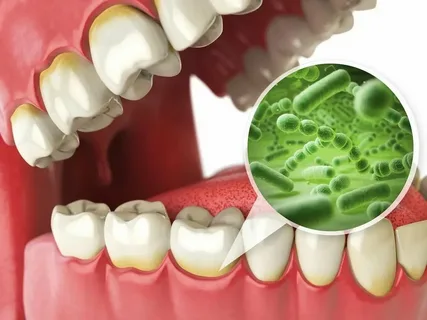
Figura 1. Micro-organismos da placa dentária.
A intensidade da formação da placa dentária é determinada por vários fatores, entre os quais podemos destacar:
- hábitos diários (frequência de alimentação, fumar, qualidade da higiene, uso de fluoretos, medicamentos antibacterianos),
- indicadores bioquímicos e biofísicos do fluido oral,
- características estruturais dos dentes,
- fatores de retenção,
- características da mordida.
A placa que permanece na superfície do dente por um longo tempo gradualmente mineraliza, formando tártaro dentário. A calcificação é o resultado da influência complexa de fatores bacterianos, biológicos e físico-químicos. Como resultado da penetração de cristais de fosfato de cálcio da saliva, estes começam a se depositar na base coloidal. Isso ocorre na placa supragengival, enquanto na placa subgengival, os minerais vêm do soro sanguíneo. A mineralização da placa dentária pode ocorrer dentro de 12 dias. O tártaro completo é formado após um mês.
O crescimento de tártaro na superfície do dente ocorre devido ao acúmulo de uma camada de placa bacteriana. O tártaro, tendo uma superfície áspera, favorece a adesão de microorganismos. Com o aumento da espessura da placa, sua composição microbiológica específica muda.
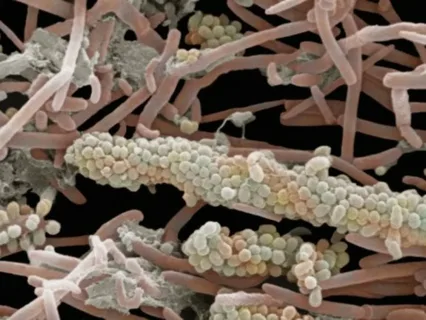
Figura 2. Placa dentária sob o microscópio.
Foram identificadas cerca de 600 variedades de bactérias que habitam a placa supra e subgengival. Nos segundo e terceiro dias, a placa inclui predominantemente aeróbios gram-positivos, principalmente estreptococos e actinomicetos.
O consumo de oxigênio por microrganismos aeróbicos reduz o potencial redox local, o que cria condições para o surgimento de representantes de anaeróbios gram-negativos no terceiro ou quarto dia.
Junto com as mudanças na microflora, observa-se uma interação complexa entre diferentes espécies. Por exemplo, St. Actinomyces realizam a fermentação de açúcares, aumentando a concentração de ácido lático, que é necessário para a vida dos cocos gram-negativos anaeróbicos Veillonella, e seu produto de metabolismo - menadiona é necessário para a vida de Prevotella intermedia e Porphyramonas gingivalis.
Os produtos do metabolismo de anaeróbios gram-negativos criam condições favoráveis para a ativação subsequente da colonização anaeróbica. Fusobacterium nucleatum provoca o acúmulo de cátion amônio; representantes do gênero Capnocytophaga produzem o ânion do ácido succínico; Campylobacter — pigmento orgânico vermelho que contém ferro. Os metabólitos descritos sustentam a vida de outras bactérias mais agressivas, que foram classificadas pelos cientistas como potencialmente patogênicas para a periodontite. Este fato destaca seu papel significativo na patogênese da periodontite, na formação de bolsas periodontais, na reabsorção do processo alveolar e na destruição do tecido conjuntivo.

Figura 3. Biofilme microbiano.
Para identificar os microrganismos que vivem na área periodontal, os seguintes critérios foram propostos para este grupo:
- associação com a doença – o número do microrganismo aumenta no local da lesão com a progressão da doença;
- o número do microrganismo diminui na área da lesão com o tratamento eficaz;
- a invasão dos representantes da espécie nos tecidos do periodonto provoca uma resposta imune humoral e celular;
- presença de mecanismos de virulência que podem causar a destruição dos tecidos do periodonto;
- capacidade do microrganismo de se tornar um fator etiológico da doença periodontal.
Virulência das bactérias do biofilme dental
Virulência é a capacidade de um microrganismo infectar um determinado organismo. Não deve ser confundida com patogenicidade – a capacidade de causar o desenvolvimento de uma doença, uma vez que o agente infeccioso após a infecção pode se tornar um simbionte do hospedeiro. A virulência depende das propriedades do próprio agente infeccioso – são os fatores de virulência e da susceptibilidade, sensibilidade do organismo hospedeiro.
Os fatores de virulência dos microrganismos do biofilme dental são divididos em dois grandes grupos:
- fatores que permitem às bactérias colonizar nos tecidos da cavidade oral e penetrar mais profundamente (adesão, colonização, invasividade);
- fatores que permitem aos microrganismos causar indiretamente ou diretamente a destruição dos tecidos do hospedeiro (antigenicidade, toxigenicidade, invisibilidade ao sistema imunológico).
Adesão e colonização
A habilidade do agente infeccioso de se fixar no ambiente periodontal é um fator de virulência. O bolsão periodontal, assim como o sulco gengival, contêm fluido gengival, que se move da base do bolsão ou sulco para fora. Representantes das bactérias que colonizam essa área se fixam às superfícies circundantes (raiz ou coroa do dente, biofilme existente, tecidos moles) de modo a evitar serem lavados pelo fluxo do fluido.

Figura 4. Colonização da superfície do dente.
Os primeiros a se fixarem na película localizada na superfície do dente são Streptococcus sanguis, oralis, mitis, que possuem receptores superficiais facilitando a adesão subsequente de outros tipos de bactérias (coagregação). Na literatura, a interação mais completamente descrita é a de Actinomyces viscosus, que se fixa através das fímbrias superficiais de Streptococcus sanguis graças aos receptores polissacarídeos destes últimos. Porphyromonas gingivalis se fixa a fibroblastos e células epiteliais por meio de fímbrias. P. gingivalis tem a capacidade de se ligar a outras bactérias, células epiteliais e estruturas do tecido conjuntivo, o que é um fator de virulência deste microrganismo.
Na base da colonização bacteriana está a capacidade das bactérias de se fixarem aos tecidos da cavidade oral e interagirem eficazmente entre si, o que é considerado como o estágio inicial de uma invasão bacteriana bem-sucedida.
Invasividade
Estudos histológicos descritos na literatura confirmam a presença de microorganismos nos tecidos periodontais de pacientes com periodontite progressiva e gengivite ulcerativa. Nestes estudos, bactérias gram-positivas e gram-negativas, incluindo cocos, bacilos, espiroquetas e filamentos, são encontradas nos tecidos gengivais, bem como nas proximidades do tecido ósseo. A capacidade das bactérias de penetrarem profundamente nos tecidos é devida a certas enzimas bacterianas que possuem atividade aumentada e ação diversificada, entre elas:
- hialuronidase,
- neuraminidase,
- colagenase,
- lecitinase.
Os microorganismos penetram no corpo do hospedeiro através de áreas ulceradas no epitélio de fixação, sendo observados no espaço intercelular da gengiva. Outra forma de invasão é a penetração direta do agente infeccioso nas células epiteliais do hospedeiro ou nas células do tecido conjuntivo. A segunda forma de penetração é característica dos seguintes microorganismos: P. gingivalis, A. actinomycetemcomitans, Treponema denticola e F. nucleatum.
Figura 5. Remoção de placa dentária.
Pesquisadores acreditam que a exacerbação da inflamação crônica dos tecidos do periodonto depende diretamente da fase de penetração bacteriana nos tecidos do periodonto. O bolsão periodontal é um reservatório de microrganismos, cuja recolonização provoca um surto agudo de atividade da doença. Essa hipótese foi confirmada clinicamente. No processo de tratamento de pacientes com periodontite progressiva, a limpeza mecânica do bolsão periodontal por si só não é suficiente para estabilizar o processo inflamatório. Nas áreas afetadas, não é possível reduzir a colonização de A. Actinomycetemcomitans, sendo frequentemente necessário prescrever antibióticos sistêmicos, muitas vezes em conjunto com tratamento cirúrgico.
Mecanismos microbianos de penetração nos tecidos do hospedeiro incluem a destruição direta dos tecidos, também mediada, causada pela ação de mediadores biológicos devido ao processo inflamatório nos tecidos periodontais.
Sobre aspectos anatômicos importantes dos tecidos periodontais no webinar Tratamento Avançado de Doenças Periodontais.