Выявление прогностических факторов развития сиаладенита у пациентов на фоне радиойодтерапии
Введение. Радиойодтерапия является современным методом лечения патологии щитовидной железы. Ее применение возможно как при злокачественных образования, так и при тиреотоксикозах. Однако, эта методика имеет осложнение в виде нарушение функции слюнных желез, которое вызывает сухость в полости рта, ее увеличение и болевой синдром.
Целью нашего исследования было выявление факторов риска развития функциональных нарушений слюнных желез у пациентов перенесших радиойодтерапию.
Материал и методы. Было проведено ретропроспективное открытое двуцентровое нерандомизированное исследование, в которое был включен 61 пациент, получивших райдиойодтерапию по поводу заболеваний щитовидной железы. У 33/61 пациента признаков развития сиаладенита на фоне и после радиойодтерапии зарегистрировано не было. У двадцати восьми пациентов (28/61) было выявлено поражение слюнных желез на фоне проводимой терапии. Проведен статистический анализ данных пола, возраста, основного клинического диагноза, стадии основного заболевания, полученной дозы I131, наличия или отсутствия сиаладенита, время развития сиаладенита.
Результаты. При анализе полученных данных было выявлено, что независимыми неблагоприятными факторами, увеличивающими риск развития поражения слюнных желез у пациентов, получивших как минимум один сеанс радиойодтерапии, явились: женский пол (р=0,0219; ОР 10,38: 95% ДИ 1,40–76,84) и возраст 61 год и моложе (р = 0,0004; ОР 1,04: 95% ДИ 1,02–1,06). А медиана суммарно накопленной дозы радиофармпрепарата не показала свою значимость в многофакторном анализе.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Заключение. Развитие хронического сиаладенита на фоне радиойодтерапии является многофакторной патологией. Эта патология требует динамического наблюдения и профилактических мероприятий особенно группа риска (женский пол и возраст 61 год и моложе).
Введение
Радиойодтерапия является одним из видов лечения патологии щитовидной железы. В основе данной методики лежит понимание механизмов транспорта I131 из крови посредством Na-I-симпортера в фолликулярный эпителий щитовидной железы. Однако, при проведении данного лечения возможно нарушение функции слюнных желез, в связи с работой тех же механизмов и физиологическом накоплений радиофармпрепарат в них. Частота развития хронического сиаладенита после терапии I131 доходит до 67%.
Потеря функции слюнной железы и формирование болевого синдрома влияет на качество жизни пациентов и может привести к нарушению их социальной жизни.
Постоянная сухость в полости рта затрудняет формирование пищевого комка и разговор, а так же способствует развитию патологических изменений слизистой оболочки полости рта и повреждению твердых тканей зубов.
На сегодняшний момент встречаются лишь единичные работы по анализу факторов риска развития патологии слюной железы. В статьях рассматриваются показатели кумулятивной дозы, пола, возраста, даже национальности, некоторые исследования направлены только на субъективные показатели пациента, напри-мер сухость в полости рта. Однако до сих пор не выявлены методы профилактики данного осложнения. Рекомендуют применение амифостина, селена, витаминов А и Е, слюногонной диеты, массажа слюнных желез. Данные об эффективности этих методик, вариантах их использования, а также о зависимости развития дисфункции слюнных желез от дозы получаемого препарата противоречивы.
Поэтому целью нашего исследования было выявление возможных прогностических факторов риска развития сиаладенита у больных, получавших радиойодтерапию по поводу заболеваний щитовидной железы.
Материал и методы
Было проведено ретро-проспективное открытое двуцентровое нерандомизированное исследование, в которое всего был включен 61 пациент. Все пациенты получи-ли радиойодтерапию по поводу заболеваний щитовидной железы в отделении радиохирургического лечения открытыми нуклидами Медицинского радиологического научного центра им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России в период с 2000 по 2022 год.У 33/61 пациента признаков развития сиаладенита на фоне и после радиойодтерапии зарегистрировано не было. Двадцать восемь пациентов (28/61), у которых было выявлено поражение слюнных желез на фоне проводимой терапии, были направлены в клинику челюстно-лицевой хирургии ФГБОУ ВО ПСПбГМУ им. И.П. Павлова Минздрава России по поводу поражения слюнных желез после проведения радиойодтерапии в период с 2017 по 2022 год. С целью дальнейшего анализа все пациенты были разделены на две группы в зависимости от факта наличия или отсутствия клинических признаков поражения слюнных желез. Пациенты группы 1 (основная; 28 пациентов) имели признаки поражения слюнных желез, пациенты группы 2 (контрольная; 33 пациента) какого-либо поражения слюнных желез не имели.
Пациенты проходили стандартный осмотр (жалобы, анамнез заболевания и жизни, пальпация слюнных желез, осмотр полости рта), сцинтиграфию для оценки накопления радиофармпрепарата в слюнных железах.
Изучаемыми переменными были пол, возраст, основной клинический диагноз, стадия основного заболевания, полученная доза I131, наличие или отсутствие сиаладенита, время от старта радионуклидов терапии до развития сиаладенита.
Основными критерии включения пациентов в исследование были:
- Возможность и согласие подписать форму добровольного информированного согласия на участия в исследовании.
- Возраст пациентов – старше 18 лет.
- Проведение радиойодтерапии по поводу заболеваний щитовидной железы.
Основные критерии невключения пациентов в исследование были:
- Зарегистрированное наличие любых сопутствующих состояний в стадии субкомпенсации и декомпенсации.
- Наличие заболеваний слюнных желез до радиойодтерапии
- Наличие любых нежелательных явлений после проведенного радионуклидного лечения, не разрешившихся до 1 степени токсичности, определяемо по шкале CTCAE ver. 5.0 (за исключением поражения слюнных желез).
На первом этапе статистического анализа произведена проверка количественных переменных на нормальность распределения с помощью теста Шапиро-Уилка. В том случае, когда данные подчинялись нормальному закону распределения, описательная статистика переменных производилась с помощью показателя среднего арифметического и стандартного отклонения (M±SD), в том случае, когда данные не подчинялись нормальному распределению – с помощью медианы и межквартильного размаха (Me [Q25–Q75]).
Сравнение численных переменных при нормальном распределении осуществляли с использованием t-критерия Стьюдента; в случае отклонения распределения от нормального сравнение независимых переменных осуществляли с помощью критерия Mann – Whitney, сравнение зависимых переменных – с помощью критерия Wilсoхon.
Сравнение больших групп больных по частоте встречаемости номинального признака проводили с использованием z-критерия (с поправкой Yates на непрерывность), теста χ2 (с поправкой Yates на непрерывность); сравнение групп больных малого объема (5 и менее) – с использованием точного критерия Fisher.
С целью выявления прогностической ценности рассматриваемых факторов проводился ROC-анализ с построением ROC-кривых, расчетом площади под кривой (AUC) и определением уровня чувствительности (доля истинно положительных случаев) и специфичности (доля истинно отрицательных случаев). С помощью ROC-анализа произведено определение оптимального порогового значения каждого из изучаемых показателей («точка cut-off»); оптимальность выбранного порогового значения определялось с помощью индекса Юдена (Youden’s J index).
Анализ развития поражения слюнных желез на фоне РЙТ проводился с использованием процедуры Капла-на-Майера. Сравнение кривых развития событий проводился с использованием логранк теста, а также с помощью построения регрессионной модели Cox с использованием в качестве метода регрессионного оценивания методику пошагового исключения (Backward) (в зависимости от выбранной статистической модели).
Статистическая обработка данных проводилась с по-мощью пакета прикладных статистических программ STATISTICA® (StatSoft, ver. 12.0), с помощью пакета статистических программ MedCalc® (ver. 20.118) и с помощью программы Microsoft® Excel (ver. 16.16.12).
Результаты исследования
Первично был проведен анализ общей характеристики пациентов. Группу 1 составили 3,57% мужчин и 96,43% женщин, в возрасте от 21 года до 77 лет, средний возраст составил 59,54±13,75 лет (95% ДИ 45,20–55,87). Группу 2 составили 39,39% мужчин и 60,61% женщин, в возрасте от 26 до 82 лет, медиана возраста составила 68 лет [59,75–75,00]. В группе 1 было значимо больше женщин, чем в контрольной группе (р = 0,0010) и все пациенты группы 1 были значимо моложе, чем пациенты группы 2 (контрольной) (р = 0,0001).
При анализе общей полученной дозы радиофармпрепарата при лечении первой группы пациентов медиана дозы, после которой у пациентов этой группы развилось поражение слюнных желез, составила 3,86 Гбк [3,50–4,00] (а общая суммарная доза варьировалась от 2,56 до 6,77 Гбк), что было значимо меньше, чем в контрольной группе – р < 0,0001.
Общая суммарная доза, полученная при лечении пациентов контрольной группы была значимо больше варьировалась от 37,00 до 100,00 Гбк, а медиана полученной дозы составила 51,90 Гбк [42,80–74,00] без признаков развития поражения слюнных желез.
При проведении ROC-анализа значимые модели были получены при определении влияния на риск развития поражения слюнных желез на фоне или после проведения радиойодтерапии пола пациентов, их возраста и суммарной полученной дозы (Гбк) (см. рисунок).
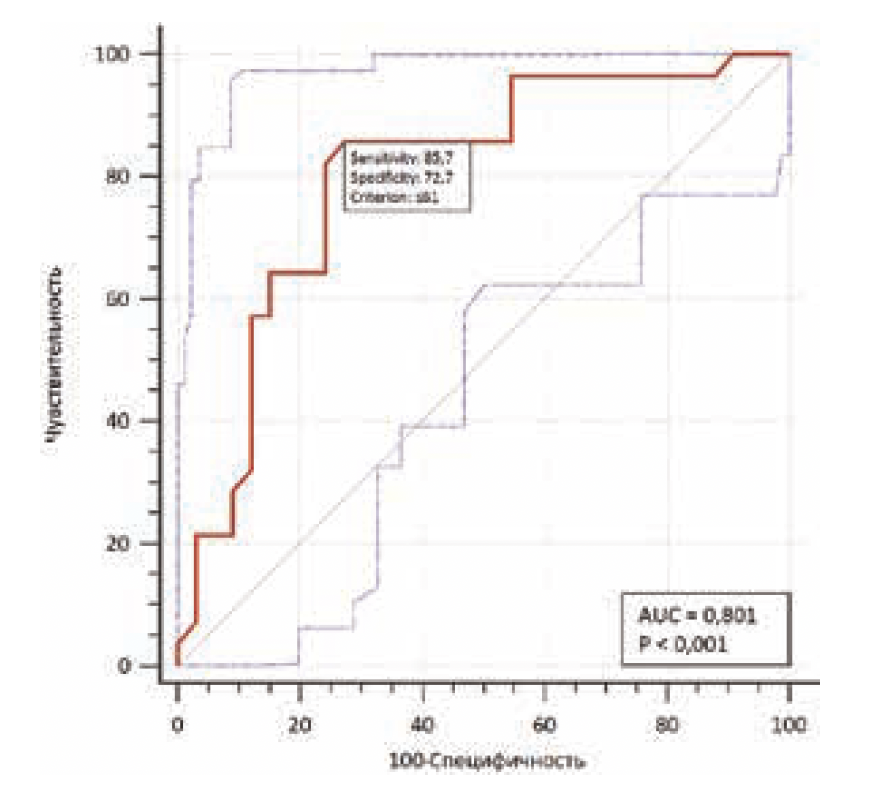
На основании выявленных путем проведенного ROC-анализа пороговых значений каждого из рассматриваемых показателе проводился однофакторный анализ их влияния на риск развития поражения слюнных желез у больных на фоне или после проведения радиойодтерапии.
Без учета влияния друг на друга, статистически значимое влияние на риск развития поражения слюнных желез у пациентов на фоне или после радиойодтерапии оказали все анализируемые показатели: пол, возраст и суммарная доза радиойодтерапии.
Однако, с целью определения истинной прогностической ценности рассматриваемых факторов на развития поражения слюнных желез у пациентов все значимые параметры были включены в многофакторную модель пропорциональных рисков Кокса (см. таблицу).
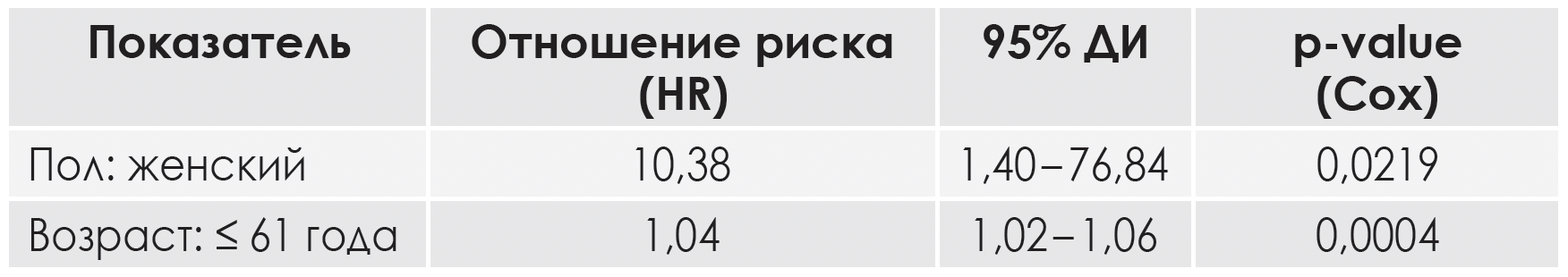
В модель, оценивающую влияние рассматриваемых факторов на сро-ки возникновения поражения слюнных желез после как минимум одного сеанса радиойодтерапии, были включены следующие показатели: пол, возраст пациентов с пороговым значением, не превышающим 61 год, и суммарная накопленная доза радиойодтерапи с пороговым значением, не превышающим 6,77 Гбк. В целом, построенная модель обладала статистической значимостью: р<0,0001, а качество построенной модели было хорошим.
Проведенный многофакторный анализ позволил установить, что независимыми показателями, имеющими статистически значимое негативное влияния на риск развития поражения слюнных желез у пациентов, получивших как минимум один сеанс радиойодтерапии, были женский пол и возраст 61 год и менее.
Обсуждение
Развитие дисфункции слюнных желез при проведении абляции радиоактивным йодом является актуальной проблемой для пациентов, так как они имеют работоспособный возраст, ведут активную социальную жизнь, имею длительные сроки выживаемости. На сегодняшний момент нет четкого алгоритма профилактики и лечения данной патологии, поэтому определения факторов риска может быть звеном в развитии алгоритма профилактики данного осложнения. Поражение слюнных желез может нести как острый характер, так и развиваться со временем, даже после однократного введения препарата. При анализе факторов без влияния друг на друга было выявлено, что нарушения слюнных желез возможно при дозе в более 3,86 Гбк. Что подтверждается в исследованиях различных авторов, которые определяли функции слюнных желез в условиях сцинтиграфии. Рядом авторов было отмечено отмечено, что при дозе 3,7 Гбк и меньше возможным сдерживающим фактором поражения слюнных желез, являлось включение их внутренних компенсаторных механизмов. Так как терапевтическая доза I131 рассчитывается индивидуально для каждого пациента и зависит от объема щитовидной железы, вида и стадии основного заболевания, можно сказать, что проведение лечение в дозе выше 3,86 Гбк должно насторожить прак-тикующих докторов и, в рамках алгоритма выявления не-желательных явлений, следует проводить дополнительные исследования слюнных желез.
При анализе источников литературы было выявлено, что большинство исследований были направлены только на один фактор вне зависимости о других, а некоторые авторы исследовали пациентов с уже развившейся ксе-ростомией до введения радиофармпрепаратов: например, ксеростомия, которая была зарегистрирована только по субъективным ощущениям пациента. В нашем исследовании мы провели многофакторный анализ, который показал, что истинными факторами риска может быть женский пол и возраст с 61 года и менее.
Заключение
Таким образом, полученные результаты свидетельству-ют о том, что женщины имеющие возраст 61 год и менее, в большей степени подверженны развитию сиаладенита на фоне проведенной радиойодтерапии. Таким образом необходимо выделять таких пациентов в отдельную группу с повышенным фактором риска осложнений и проводить дополнительные виды анализов в виде динамической сцинтиграфии и ультразвукового исследования слюнных желез на догоспитальном этапе для оценки первичного статуса пациента. А медиана суммарной на-копленной дозы радиойодтерапии, после которой возможно развитие поражения слюнных желез у данной группы составившая 3,86 Гбк [3,50–4,00], хоть и не показала свою значимость в многофакторном анализе, в однофакторном анализе увеличивала риск развития сиаладенита.
Так же необходимо динамическое наблюдение для минимизации развития обструкционной патологии слюн-ных желез, а также проведение сиалэндоскопии для уменьшение формирования структур протока.
Авторы
Разумова А.Я., Кутукова С.И., Яременко А.И., Бородавина Е.В., Петров Н.Л.
Список литературы
- Гарбузов П.И., Дроздовский Б.И., Родичев А.А. и др. Радиойодтерапия рака щитовидной железы . Практическая онкология. 2007; 1(29):42–45. Garbuzov P.I., Drozdovskij B.I., Rodichev A.A. i dr. Radiojodterapiya raka shchi-tovidnoj zhelezy . Prakticheskaya onkologiya. (In Russ) 2007; 1(29):42–45.
- Данилова Л.И., Валуевич В.В. Радиойодтерапия доброкачественных забо-леваний щитовидной железы. Проблемы Эндокринологии. 2006;52(2):43–47. https://doi.org/10.14341/probl200652243-47.
Danilova L.I., Valuyevich V.V. Radioiodine therapy for benign thyroid diseases. Problems of Endocrinology. 2006;52(2):43-47. (In Russ.)https://doi.org/10.14341/probl200652243-47. - Krčálová E., Horáček J., Gabalec F., Žák P., Doležal J. Scintigraphic evaluation of salivary gland function in thyroid cancer patients after radioiodine remnant ablation. Eur J Oral Sci. 2020;128(3):204-210. https://doi. org/: 10.1111/eos.12689
- Hollingsworth B., Senter L., Zhang X., Brock G.N., Jarjour W., Nagy R., Brock P., et al. Risk Factors of 131I-Induced Salivary Gland Damage in Thyroid Cancer Patients. J Clin Endocrinol Metab. 2016;101(11):4085-4093. doi: 10.1210/jc.2016-1605.
- Riachy R., Ghazal N., Haidar M.B., Elamine A., Nasrallah M.P. Early Sialadenitis After Radioactive Iodine Therapy for Differentiated Thyroid Cancer: Prevalence and Predictors. Int J Endocrinol. 2020;2020:8649794. doi: 10.1155/2020/8649794.
- Sánchez Barrueco A., González Galán F., Alcalá Rueda I., Santillán Coello J.M., Barrio Dorado M.P., Villacampa Aubá J.M., Escanciano Escanciano M. еt al. Incidence and risk factors for radioactive iodine-induced sialadenitis. Acta Otolaryngol. 2020 ;140(11):959-962. doi: 10.1080/00016489.2020.1802507.
- Jentzen W, Richter M, Nagarajah J, Poeppel TD, Brandau W, Dawes C, Bockisch A, Binse I. Chewing-gum stimulation did not reduce the absorbed dose to salivary glands during radioiodine treatment of thyroid cancer as inferred from pre-therapy (124)I PET/CT imaging. EJNMMI Physics 2014; 1: 100. doi: 10.1186/s40658-014-0100-1.
- Auttara-Atthakorn A., Sungmala J., Anothaisintawee T., Reutrakul S., Sriphrapra-dang C. Prevention of salivary gland dysfunction in patients treated with radio-iodine for differentiated thyroid cancer: A systematic review of randomized controlled trials. Front Endocrinol (Lausanne). 2022 ;13:960265. https://doi. org/ 10.3389/fendo.2022.960265.
- Ahn B.C. Reduction of Salivary Gland Damage During Radioiodine Therapy for Differentiated Thyroid Cancers. Nucl Med Mol Imaging. 2020 Jun;54(3):126–127. https://doi. org/ 10.1007/s13139-020-00643-w.
- Baudin C., Bressand A., Buffet C., Menegaux F., Soret M., et all. Dysfunction of the Salivary and Lacrimal Glands After Radioiodine Therapy for Thyroid Cancer: Results of the START Study After 6-Months of Follow-Up. Thyroid. 2023;33(9):1100-1109. https://doi. org/ 10.1089/thy.2023.0090.
- Upadhyaya A., Meng Z., Peng W., Guizhi Z., et all. J Effects of first radioiodine ab-lation on functions of salivary glands in patients with differentiated thyroid cancer. Medicine. 2017; 96(25):p e7164. https://doi. org/ 10.1097/MD.0000000000007164
- An YS, Yoon JK, Lee SJ, Song HS, Yoon SH, Jo KS. Symptomatic late-onset sialade-nitis after radioiodine therapy in thyroid cancer. Ann Nucl Med. 2013;27(4):386-91. https://doi. org/ 10.1007/s12149-013-0697-5.
- Horvath E., Skoknic V., Majlis S., Tala H., Silva C. et all. Radioiodine-Induced Salivary Gland Damage Detected by Ultrasonography in Patients Treated for Papillary Thyroid Cancer: Radioactive Iodine Activity and Risk. Thyroid. 2020 Nov;30(11):1646-1655. doi: 10.1089/thy.2019.0563.
